在实验室加热32.5g二氧化锰和氯酸钾的固体混合物制取氧气时,剩余固体物质的质量变化如下图所示。请计算:
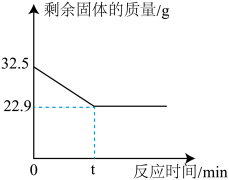
(1)完全反应时,生成氧气的质量为_____ g。
(2)完全反应后,剩余固体物质属_____ (填纯净物、混合物)。
(3)原固体混合物中氯酸钾的质量为多少?

(1)完全反应时,生成氧气的质量为
(2)完全反应后,剩余固体物质属
(3)原固体混合物中氯酸钾的质量为多少?
更新时间:2017-11-21 09:53:50
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】某补钙剂的主要成分是碳酸钙。欲测定该补钙剂中碳酸钙的质量分数,某同学进行了如图所示的操作(补钙剂中其它成分不参与反应;不考虑盐酸的挥发和水蒸气的逸出)。

(1)由图可知生成气体的质量为_______ g。
(2)该实验中,装置的气密性对测定结果_______ (填“有”或“无”)影响。
(3)计算该补钙剂中碳酸钙的质量分数(写出详细过程)。

(1)由图可知生成气体的质量为
(2)该实验中,装置的气密性对测定结果
(3)计算该补钙剂中碳酸钙的质量分数(写出详细过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组用氯酸钾与二氧化锰的混合物制取氧气,试管中固体的质量随时间变化的数据见下表。制取结束后,将剩余团体用适量水充分溶解后,过滤,回收二氧化锰固体。
请计算:
(1)共制得氧气___________ g。
(2)求所得剩余固体的各成分的质量。
| 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 26.0 | 23.4 | 16.4 | 16.4 |
(1)共制得氧气
(2)求所得剩余固体的各成分的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】小明同学加热实验室某不纯的KMnO4固体分解制备O2(杂质可溶于水且受热不分解),完全反应后测得相关数据如图所示。回答下列问题:
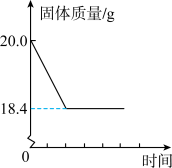
(1)将分解后剩余固体加水充分溶解,经过滤、洗涤、干燥得到的固体为______(填化学式),在另两种实验室制备O2的方法中,该物质被用作__________。
(2)该分解过程生成的O2的质量为________g。
(3)计算该固体中KMnO4的质量分数(写出计算过程)。

(1)将分解后剩余固体加水充分溶解,经过滤、洗涤、干燥得到的固体为______(填化学式),在另两种实验室制备O2的方法中,该物质被用作__________。
(2)该分解过程生成的O2的质量为________g。
(3)计算该固体中KMnO4的质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐2】向盛有一定质量氢氧化钠溶液的试管中加入1.6g白色硫酸铜粉末,恰好完全反应,过滤,得到10.0g溶液(操作带来的质量损失均忽略不计)。已知Cu的相对原子质量为64,请计算:(计算结果均保留2位小数)
(1)过滤得到的滤渣质量;
(2)所得溶液的溶质质量分数;
(3)原试管中氢氧化钠溶液的质量。
(1)过滤得到的滤渣质量;
(2)所得溶液的溶质质量分数;
(3)原试管中氢氧化钠溶液的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】如图是碳酸钙D3片标签的部分信息。化学社团为测定该药片中的碳酸钙的量是否与标签相符,进行实验:取8片药片,研碎后放入烧杯中,再把50g稀盐酸分五次加入,实验所得数据如下表所示(假设其他成分不含钙元素,也不参加反应):

(1)表中m的数值为______ 。
(2)第______ 次恰好完全反应。
(3)计算每片药片中碳酸钙的质量并且判断是否与标签相符。(写出计算过程)
(4)服用该钙片嚼食,可使钙片与胃酸充分反应,其原理是______ 。根据计算结果,某儿童按标签说明服用钙片,每天补充的钙元素的质量是______ g。

| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入稀盐酸的质量/g | 10 | 10 | 10 | 10 | 10 |
| 生成气体的总质量/g | 1.1 | 2.2 | m | 4.4 | 4.4 |
(1)表中m的数值为
(2)第
(3)计算每片药片中碳酸钙的质量并且判断是否与标签相符。(写出计算过程)
(4)服用该钙片嚼食,可使钙片与胃酸充分反应,其原理是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】医学上常用双氧水(过氧化氢的水溶液)来清洗创口和局部抗菌,小美同学从家庭小药箱中取68g某医用双氧水溶液放入烧杯中,然后加入2g二氧化锰,每隔一分钟观察一次并记录产生的氧气的质量如表所示,直到实验结束。请回答下列问题:
(1)双氧水属于__________ (填“混合物”或“纯净物”或“氧化物”)。
(2)在此实验中,二氧化锰的作用是________ ,在称量时间为 5 分钟时,二氧化锰的质量为________ 。
(3)从表格可知,该实验生成氧气的总质量为________ 。
(4)请计算该双氧水中过氧化氢的质量(写出具体计算过程)。
| 称量时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| 产生氧气的质量/g | 0 | 0.7 | 1.1 | 1.4 | 1.6 | 1.6 |
(2)在此实验中,二氧化锰的作用是
(3)从表格可知,该实验生成氧气的总质量为
(4)请计算该双氧水中过氧化氢的质量(写出具体计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】下图是某生理盐水的标签,根据标签给出的数据回答下列问题。

(1)生理盐水属于
(2)在氯化钠中,钠元素与氯元素的质量比为
(3)假设生理盐水的密度为1.0g/cm3,则这瓶生理盐水的溶质质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组取26.5g氯酸钾和二氧化锰的混合物制取氧气。加热到不再产生气体为止,得到如下数据,请计算:
(1)混合物完全反应后生成氧气的质量为_____ g。
(2)求所取的26.5g混合物中氯酸钾的质量(请写出计算过程)。
| 反应时间t/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
| 剩余固体的质量m/g | 26.5 | 24.9 | 23.3 | 21.7 | 20.1 | 18.5 | 16.9 | 16.9 | 16.9 |
(2)求所取的26.5g混合物中氯酸钾的质量(请写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐2】实验室制取氧气所用的氯酸钾通常含一定量的杂质。小明同学称取6.00g样品与2.00g二氧化锰混合,加热使其完全反应,冷却至室温。将剩余固体与17.02g水充分溶解,过滤,得到的不饱和溶液中溶质的质量分数为14.9%。 若不考虑实验中药品的损耗,氯酸钾样品中的杂质不参与反应,也不溶于水。请回答下列问题。(结果精确到0.01g)
(1)要完全回收反应生成的氯化钾,还需进行的操作是________,可回收氯酸钾的质量为________;
(2)计算样品中氯酸钾的质量是多少?
(可能用到的相对原子质量:O-16 Cl-35.
(1)要完全回收反应生成的氯化钾,还需进行的操作是________,可回收氯酸钾的质量为________;
(2)计算样品中氯酸钾的质量是多少?
(可能用到的相对原子质量:O-16 Cl-35.
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】实验室用氯酸钾和二氧化锰的固体混合物共33.2g加热制取氧气,记录产生氧气的质量与加热时间如图所示,请回答下列问题:
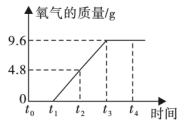
(1)t3~t4时段内剩余固体物质的质量为______ g。
(2)根据图中数据计算原混合物中氯酸钾的质量分数。(写出计算过程,结果精确到0.1%)

(1)t3~t4时段内剩余固体物质的质量为
(2)根据图中数据计算原混合物中氯酸钾的质量分数。(写出计算过程,结果精确到0.1%)
您最近一年使用:0次



