实验室取15.0克氯酸钾和二氧化锰混合物,加热该混合物,冷却,称量剩余固体质量.重复以上操作,依次加热t1、t2、t3、t4时间后称量剩余固体的质量,记录数据如下表:
①完全反应后产生氧气的质量 ______ .
②求该混合物中氯酸钾的质量为__________.
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(克) | 14.4 | 12.6 | 10.2 | 10.2 |
①完全反应后产生氧气的质量 ______ .
②求该混合物中氯酸钾的质量为__________.
更新时间:2017-12-19 09:12:53
|
相似题推荐
计算题
|
适中
(0.65)
真题
名校
【推荐1】 如下图所示,实验室用过氧化氢溶液和二氧化锰制取氧气,实验的相关数据如下表。
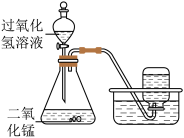
(l)反应中二氧化锰的作用是 。
(2)反应生成氧气的质量为 g(结果精确到0. 1 g,下同)。
(3)计算参加反应的过氧化氢的质量,写出必要的计算过程。

| 气体发生装置内物质的总质量 | |
| 反应前 | 35.6 |
| 反应后 | 34.8 |
(2)反应生成氧气的质量为 g(结果精确到0. 1 g,下同)。
(3)计算参加反应的过氧化氢的质量,写出必要的计算过程。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】小明用如图1所示装置进行实验,他将碳粉和过量氧化铜混合充分加热,试管中固体总质量与加热时间的变化关系如图2所示。
(1)该反应中氧化铜发生了___________ (填“氧化”或“还原”)反应。
(2)根据化学方程式计算实验前混合物中碳粉的质量________ (结果精确到0.1g)。

(1)该反应中氧化铜发生了
(2)根据化学方程式计算实验前混合物中碳粉的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某菱铁矿石样品中FeCO3的质量分数为80%,兴趣小组进行了如下实验。

已知:FeCO3+2HCl=FeCl2+H2O+CO2↑,杂质不溶于水,也不与其他物质反应。
(1)若用溶质质量分数为36.5%的浓盐酸配制实验所用的稀盐酸,需要加入___________ g水。
(2)反应后所得“固液混合物”的质量为___________ g
(3)若要冶炼含铁80%的生铁560t,试求理论上需要这种矿石的质量。(请写出计算过程)

已知:FeCO3+2HCl=FeCl2+H2O+CO2↑,杂质不溶于水,也不与其他物质反应。
(1)若用溶质质量分数为36.5%的浓盐酸配制实验所用的稀盐酸,需要加入
(2)反应后所得“固液混合物”的质量为
(3)若要冶炼含铁80%的生铁560t,试求理论上需要这种矿石的质量。(请写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】浩瀚的海洋蕴藏着丰富的化学资源,海水晒盐的主要流程如图所示。

(1)海水晒盐后的“母液”是氯化钠的___________ (填"饱和”或“不饱和”)溶液。
(2)利用"卤水”也可以制得金属铁等化工原料。下图某盐场1000g“卤水”中部分成分含量柱形图。

试计算:
①若使1000g该“卤水”中的氯化镁和硫酸镁完全转化为Mg(OH)2沉淀,至少需要20%NaOH溶液多少克?计算过程:___________ 。
②将上述沉淀完全转化为无水MgCl2,并在熔融状态下进行电解,理论上最多可得到金属镁___________ 克。

(1)海水晒盐后的“母液”是氯化钠的
(2)利用"卤水”也可以制得金属铁等化工原料。下图某盐场1000g“卤水”中部分成分含量柱形图。

试计算:
①若使1000g该“卤水”中的氯化镁和硫酸镁完全转化为Mg(OH)2沉淀,至少需要20%NaOH溶液多少克?计算过程:
②将上述沉淀完全转化为无水MgCl2,并在熔融状态下进行电解,理论上最多可得到金属镁
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某工厂需要200kg氢气制备高纯度硅( )。若用电解水的方法制取这些氢气,请计算:
)。若用电解水的方法制取这些氢气,请计算:
(1)需消耗水的质量是多少千克?
(2)能制备多少千克硅?
 )。若用电解水的方法制取这些氢气,请计算:
)。若用电解水的方法制取这些氢气,请计算:(1)需消耗水的质量是多少千克?
(2)能制备多少千克硅?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】长久使用的热水壶底部有一层水垢,主要成分是碳酸钙(CaCO3),某化学兴趣小组为了测定水垢中碳酸钙的百分含量,把25g水垢与盛有过量稀盐酸的烧杯,放在电子称上称其质量,每分钟读一次数。结果如下表,试回答下列问题:
(1)反应生成的二氧化碳的质量是多少?
(2)该水垢中CaCO3的百分含量是多少?
| 时间/min | 0 | 1 | 2 | 3 | 4 |
| 总质量/g | 100g | 95g | 92g | 91.2g | 91.2g |
(1)反应生成的二氧化碳的质量是多少?
(2)该水垢中CaCO3的百分含量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
名校
【推荐2】某工厂排放的废水中含有亚硫酸钠(Na2SO3)未经处理,会造成污染。化学兴趣小组的同学对废水处理设计了如图所示的实验方案:

试计算:
(l)反应完后生成亚硫酸钙沉淀的质量为_______g。
(2)废水中亚硫酸钠的质量分数为_________(请写出计算过程)。(温馨提示:Na2SO3+CaCl2=CaSO3↓+2NaCl;氯化钙不与废水中的其它杂质反应)

试计算:
(l)反应完后生成亚硫酸钙沉淀的质量为_______g。
(2)废水中亚硫酸钠的质量分数为_________(请写出计算过程)。(温馨提示:Na2SO3+CaCl2=CaSO3↓+2NaCl;氯化钙不与废水中的其它杂质反应)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】钙是生物体骨骼的重要组成元素。鱼骨中含有碳酸钙,现设计图甲实验测定鱼骨中的碳酸钙含量,并将测得的数据绘制成图乙。

【提示】鱼骨中其它成分与盐酸不反应,浓硫酸有吸水性。
(1)该实验中浓硫酸的作用是______ 。
(2)由图乙中的 AB 曲线,可知锥形瓶中反应速率的变化情况是______ (填“逐渐 变大”、“ 逐渐变小”或“不变”),其原因是______ 。
(3)生成气体的质量______ g。
(4)根据图中的数据计算鱼骨中碳酸钙的质量分数。

【提示】鱼骨中其它成分与盐酸不反应,浓硫酸有吸水性。
(1)该实验中浓硫酸的作用是
(2)由图乙中的 AB 曲线,可知锥形瓶中反应速率的变化情况是
(3)生成气体的质量
(4)根据图中的数据计算鱼骨中碳酸钙的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
【推荐1】某简易制氧装置的示意图如图,其原理是通过撞击火帽触发启动装置产生热量,使产氧药块分解而持续释放氧气。

(1)装置中过滤层的作用是______。
(2)若产氧药块由氯酸钾(KClO3)和二氧化锰等组成,为得到一个人呼吸2小时所需氧气的量(折算后质量为48g),计算产氧药块中至少含氯酸钾的质量(写出计算过程)。

(1)装置中过滤层的作用是______。
(2)若产氧药块由氯酸钾(KClO3)和二氧化锰等组成,为得到一个人呼吸2小时所需氧气的量(折算后质量为48g),计算产氧药块中至少含氯酸钾的质量(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】小明同学在实验室用15克氯酸钾和二氧化锰的混合物加热制取氧气,完全反应后剩余固体质量为10.2克。请你帮助小明同学计算:
(1)生成氧气的质量为_____ 克?
(2)原混合物中氯酸钾的质量分数。_____
(1)生成氧气的质量为
(2)原混合物中氯酸钾的质量分数。
您最近一年使用:0次




