金属材料在生产、生活中有着广泛的应用.
(1)用铜丝做电线是利用了铜的_______ 性。
(2)炼铁的原理是利用一氧化碳与氧化铁反应,实验装置见图甲:
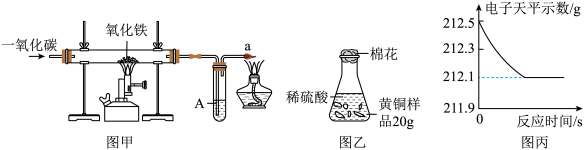
①对实验进行分析并回答:实验中硬质玻璃管里发生反应的现象是________________ ,其中A处发生反应的化学方程式是____________ 。
②实验要在装置末端a处燃着一盏酒精灯,其作用是____________ 。
(3)工业生产中,切割铁板时用硫酸铜溶液在铁板上画线可留下红色的印迹.有关反应的化学方程式为____________________________ ,属于____ 反应。
(4)要比较铁、银、铜的金属活动性强弱,选择的药品除了铁、银外,还需要__ 溶液。
(5)某研究性学习小组为了测定黄铜(铜、锌合金)的组成,用电子天平分别称得锥形瓶与棉花的质量为44.1g,称取黄铜样品20.0g。在锥形瓶中加入该样品和足量稀硫酸后瓶口塞上棉花,如图乙所示.将电子天平称量的数据绘成图丙。
请结合实验及实验数据回答:①该反应生成氢气的质量为_________________ ;
②样品中铜的质量分数是__________ ?(写出计算过程)
(1)用铜丝做电线是利用了铜的
(2)炼铁的原理是利用一氧化碳与氧化铁反应,实验装置见图甲:

①对实验进行分析并回答:实验中硬质玻璃管里发生反应的现象是
②实验要在装置末端a处燃着一盏酒精灯,其作用是
(3)工业生产中,切割铁板时用硫酸铜溶液在铁板上画线可留下红色的印迹.有关反应的化学方程式为
(4)要比较铁、银、铜的金属活动性强弱,选择的药品除了铁、银外,还需要
(5)某研究性学习小组为了测定黄铜(铜、锌合金)的组成,用电子天平分别称得锥形瓶与棉花的质量为44.1g,称取黄铜样品20.0g。在锥形瓶中加入该样品和足量稀硫酸后瓶口塞上棉花,如图乙所示.将电子天平称量的数据绘成图丙。
请结合实验及实验数据回答:①该反应生成氢气的质量为
②样品中铜的质量分数是
更新时间:2018/01/05 09:50:41
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】“斑铜”是云南特有的铜制工艺品,妙在有斑,贵在浑厚。
(1)“斑铜”制品分为“生斑”和“熟斑”。
①“生斑”是直接利用天然铜经手工锻打成片等工序制作而成的工艺品。天然铜能锻打成片,说明天然铜具有良好的_______ 性。“生斑”放置在空气中一段时间会生成铜绿[Cu2(OH)2CO3],据此推测“生斑”变为铜绿是铜与空气中的O2和_______ (填化学式)接触导致。
②“熟斑”指在熔化的铜中加入适当比例的铁、银等形成合金,高温浇铸成型、打磨、着色而成的工艺品。“熟斑”的抗腐蚀性能比纯铜_______ (填“强”或“弱”)。
(2)铜矿是制备“斑铜”的重要原料。
①下列可用于炼铜的矿石是_______ (填标号)。
A.辉铜矿(主要成分是Cu2S)
B.铝土矿(主要成分是Al2O3)
C.磁铁矿(主要成分是Fe3O4)
②在《梦溪笔谈》中记载“熬胆矾铁釜,久之亦化为铜”,叙述的是硫酸铜溶液与铁反应生成铜,该反应的化学方程式为_______ 。
(3)制作“熟斑”的废料经处理后得到Fe(NO3)2和Cu(NO3)2的混合溶液。向其中加入一定量的Mg,充分反应后过滤,得到滤液和滤渣。下列说法正确的是_______(填标号)。
(1)“斑铜”制品分为“生斑”和“熟斑”。
①“生斑”是直接利用天然铜经手工锻打成片等工序制作而成的工艺品。天然铜能锻打成片,说明天然铜具有良好的
②“熟斑”指在熔化的铜中加入适当比例的铁、银等形成合金,高温浇铸成型、打磨、着色而成的工艺品。“熟斑”的抗腐蚀性能比纯铜
(2)铜矿是制备“斑铜”的重要原料。
①下列可用于炼铜的矿石是
A.辉铜矿(主要成分是Cu2S)
B.铝土矿(主要成分是Al2O3)
C.磁铁矿(主要成分是Fe3O4)
②在《梦溪笔谈》中记载“熬胆矾铁釜,久之亦化为铜”,叙述的是硫酸铜溶液与铁反应生成铜,该反应的化学方程式为
(3)制作“熟斑”的废料经处理后得到Fe(NO3)2和Cu(NO3)2的混合溶液。向其中加入一定量的Mg,充分反应后过滤,得到滤液和滤渣。下列说法正确的是_______(填标号)。
| A.滤渣中一定含有的金属是Fe、Cu |
| B.滤液中可能含有的溶质是Fe(NO3)2和Cu(NO3)2 |
| C.若滤渣中有两种金属,则滤液中的溶质一定有两种 |
| D.若滤液中有两种溶质,则滤液质量一定比反应前的混合溶液质量小 |
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐2】阅读下列短文,回答问题。
钠呈银白色,质软,密度比水的小,具有可燃性。钠一般保存在煤油中。
钠曝露在空气中,常温下会与氧气反应生成氧化钠。取一大块冰,在其表面挖一个较深的坑(如图所示)。用遥控车将钠放入冰坑底部,冰火两重天的壮美奇观瞬时产生,钠变成了一个大火球,噼里啪啦听巨响,火光四射、火花飞溅。钠用它火一般的“热情”熔化了寒冷的坚冰。金属钠及其合金的用途广泛。钠和钾形成的钠钾合金熔点低,常温下呈液态,可用作快中子反应堆的热交换剂。_______ (选填“物理”或“化学”)性质。
(2)钠不能保存在水中的原因是_______ 。
(3)写出钠在曝露在空气中发生反应化学方程式:_______ 。
(4)钠钾合金用作快中子反应堆的热交换剂,是利用了钠钾合金具有良好的_______(填字母)。
钠呈银白色,质软,密度比水的小,具有可燃性。钠一般保存在煤油中。
钠曝露在空气中,常温下会与氧气反应生成氧化钠。取一大块冰,在其表面挖一个较深的坑(如图所示)。用遥控车将钠放入冰坑底部,冰火两重天的壮美奇观瞬时产生,钠变成了一个大火球,噼里啪啦听巨响,火光四射、火花飞溅。钠用它火一般的“热情”熔化了寒冷的坚冰。金属钠及其合金的用途广泛。钠和钾形成的钠钾合金熔点低,常温下呈液态,可用作快中子反应堆的热交换剂。

(2)钠不能保存在水中的原因是
(3)写出钠在曝露在空气中发生反应化学方程式:
(4)钠钾合金用作快中子反应堆的热交换剂,是利用了钠钾合金具有良好的_______(填字母)。
| A.导电性 | B.导热性 | C.延展性 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
【推荐3】金属和金属材料在人类的生产、生活中有着重要的作用。

(1)冬天取暖用的暖气片有铸铁材料、铜铝材料等多种。这主要利用了金属的_____ 性。
(2)生产、生活中对钢铁的需求量特别大,在炼铁炉中,CO 还原氧化铁的化学方程式为_____ 。
(3)新型材料纳米铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备的主要流程如下图所示。

①纳米级铁粉遇氧气无需加热就能燃烧,生成物的化学式为______________ 。
②高温反应器中发生反应的化学方程式为_______________ 。

(1)冬天取暖用的暖气片有铸铁材料、铜铝材料等多种。这主要利用了金属的
(2)生产、生活中对钢铁的需求量特别大,在炼铁炉中,CO 还原氧化铁的化学方程式为
(3)新型材料纳米铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备的主要流程如下图所示。

①纳米级铁粉遇氧气无需加热就能燃烧,生成物的化学式为
②高温反应器中发生反应的化学方程式为
您最近一年使用:0次
【推荐1】实验创新可以使现象更明显,操作更简便。Y形管的使用能增强实验的对比性,增添实验的趣味性。某化学兴趣小组同学利用Y形管设计了以下三个实验进行探究活动,请回答下列问题。
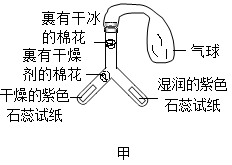
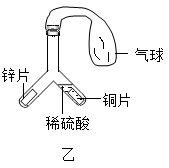
(1)据图甲所示实验,其设计的目的是_________ ,一段时间后,观察到Y形管右侧湿润的紫色石蕊试纸变红,写出发生反应的化学方程:__________ 。
(2)图乙所示实验中,一段时间后,缓慢倾斜Y形管,将右侧的稀硫酸部分倒入左侧,依据___ (填实验现象),可得出结论:Zn的金属活动性比Cu强。
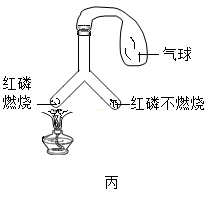
(3)图丙所示实验中,根据Y形管左右两侧现象对比,可得到的实验结论是________ ;该实验中,Y形管顶端气球的主要作用是_______ 。



(1)据图甲所示实验,其设计的目的是
(2)图乙所示实验中,一段时间后,缓慢倾斜Y形管,将右侧的稀硫酸部分倒入左侧,依据
(3)图丙所示实验中,根据Y形管左右两侧现象对比,可得到的实验结论是
您最近一年使用:0次
【推荐2】2021年10月16至2022年4月16日,我国的3名航天员进驻天和核心舱,进行了为期6个月的太空生活与实验。航空航天科学研究涉及许多化学知识,请回答下列问题。

(1)舱内生活。
①航天员每天的食品都要经过科学地计算和设计。航天团队为航天员准备了鲅鱼饺子、黄花菜饺子等春节食品,鲅鱼肉富含的营养素是_____ 。
②长期驻留空间实验室会导致航天员肌肉萎缩、骨钙丢失。可在航天食品中添加______ (填字母代号)来预防骨质疏松。
a.C12H22O14Ca b.FeC6H6O7 c.KIO3
③铁酸镍(化学式NiFe2O4)可将航天员呼出的废气转化为航天员需要的气体,而本身的质量和化学性质都不变化。NiFe2O4中若铁元素的化合价是+3价,则镍(Ni)元素的化合价是____ 。
(2)天宫课堂。
①如图所示,太空老师王亚平用注射器向制作好的的水球内注入少量蓝色液体,水球变成一个“蓝宝石”,这表明分子在_____ 。

②将半片泡腾片(含某种有机酸和碳酸氢钠,类似盐酸与碳酸氢钠反应)塞入蓝色水球里,水球里立即产生很多气泡,该气体的化学式是_____ ,这是因为泡腾片中的酸和碳酸氢钠在水球里溶解形成溶液,二者快速反应,在形成的溶液中,水作_____ 。
(3)出舱任务。舱外航天服硬体部分采用铝合金和不锈钢材料,软体部分采用聚氨酯涂层的纺织材料制成。

①使用的聚氨酯涂层属于______ 材料,外衣表面的铝合金硬度与纯铝相比更_____ (填“大”或“小”)。
②背包中的呼吸循环系统利用活性炭除臭,再用氢氧化锂(LiOH)吸收CO2(LiOH与NaOH化学性质相似),写出反应的化学方程式_____ 。
③铝合金中主要含有铝、铜、镁三种金属,对这三种金属的活动性顺序进行探究,下列各组试剂中,能达到目的的是_____ (填字母代号)。
a. Mg、AlCl3溶液、Cu(NO3)2溶液 b. Cu、Mg、AlCl3溶液 c.Cu、MgCl2溶液、AlCl3溶液

(1)舱内生活。
①航天员每天的食品都要经过科学地计算和设计。航天团队为航天员准备了鲅鱼饺子、黄花菜饺子等春节食品,鲅鱼肉富含的营养素是
②长期驻留空间实验室会导致航天员肌肉萎缩、骨钙丢失。可在航天食品中添加
a.C12H22O14Ca b.FeC6H6O7 c.KIO3
③铁酸镍(化学式NiFe2O4)可将航天员呼出的废气转化为航天员需要的气体,而本身的质量和化学性质都不变化。NiFe2O4中若铁元素的化合价是+3价,则镍(Ni)元素的化合价是
(2)天宫课堂。
①如图所示,太空老师王亚平用注射器向制作好的的水球内注入少量蓝色液体,水球变成一个“蓝宝石”,这表明分子在

②将半片泡腾片(含某种有机酸和碳酸氢钠,类似盐酸与碳酸氢钠反应)塞入蓝色水球里,水球里立即产生很多气泡,该气体的化学式是
(3)出舱任务。舱外航天服硬体部分采用铝合金和不锈钢材料,软体部分采用聚氨酯涂层的纺织材料制成。

①使用的聚氨酯涂层属于
②背包中的呼吸循环系统利用活性炭除臭,再用氢氧化锂(LiOH)吸收CO2(LiOH与NaOH化学性质相似),写出反应的化学方程式
③铝合金中主要含有铝、铜、镁三种金属,对这三种金属的活动性顺序进行探究,下列各组试剂中,能达到目的的是
a. Mg、AlCl3溶液、Cu(NO3)2溶液 b. Cu、Mg、AlCl3溶液 c.Cu、MgCl2溶液、AlCl3溶液
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】铬(Cr)为不锈钢主要的添加的元素,含量一般在12%以上。铬的表面上生成一薄层致 密的钝态氧化物保护膜是不锈钢具有耐蚀性主要原因。请回答下列问题:
(1)铁生锈的主要条件是铁与_______ 和_______ 直接接触。
(2)不锈钢属于_________ (填“合成材料”或“金属材料”)。
(3)相同温度下,取大不相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(生成物中Cr显+2价),现象如下:
①上述三种金属的活动性由强到弱的顺序是_____________ 。
②从上述实验可知,Cr能跟CuSO4溶液反应,请写出反应的化学程式________ 。
(1)铁生锈的主要条件是铁与
(2)不锈钢属于
(3)相同温度下,取大不相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(生成物中Cr显+2价),现象如下:
| 金属 | Cr | Mg | Cu |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 | 无明显现象 |
②从上述实验可知,Cr能跟CuSO4溶液反应,请写出反应的化学程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】A~I是初中化学常见的物质,其中B和G是红色固体,I是黑色固体,A和D的组成元素相同,它们之间的转化关系如图所示(部分反应条件已略去)。请回答下列问题。
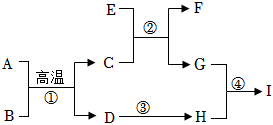
(1)A的化学式为___________ 。
(2)H的一种用途是___________ 。
(3)反应②的基本反应类型为___________ 。
(4)反应①的化学方程式为___________ 。

(1)A的化学式为
(2)H的一种用途是
(3)反应②的基本反应类型为
(4)反应①的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】根据对金属和金属材料的认识,回答下列问题:
(1)铁生锈实际上是铁与空气中的________ 发生反应的结果,洗净后的铁锅要擦干,理由是________________________________________________________ 。
(2)炼铁的主要原理是:高温下,一氧化碳与氧化铁(Fe2O3)反应生成铁。其反应的化学方程式为______________________________ 。
(3)2010年5月,在明代古沉船“南澳Ⅰ号”打捞出水的文物中,铜器的表面仅有铜锈,而铁器却锈迹斑斑或烂掉.这说明铁的金属活动性比铜的________ (填“弱”或“强”),写出一个用金属与盐溶液反应验证铁与铜金属活动性强弱的化学方程式:______________________________________________ 。
(1)铁生锈实际上是铁与空气中的
(2)炼铁的主要原理是:高温下,一氧化碳与氧化铁(Fe2O3)反应生成铁。其反应的化学方程式为
(3)2010年5月,在明代古沉船“南澳Ⅰ号”打捞出水的文物中,铜器的表面仅有铜锈,而铁器却锈迹斑斑或烂掉.这说明铁的金属活动性比铜的
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、X、Y、Z都是初中化学中常见物质,其中A是天然气的主要成分,X、Y、Z是单质,B、C、D是氧化物,常温下C是液体,Y是黑色固体,E是红色粉末。它们之间有如下反应关系:

请根据以上信息回答下列问题:
(1)写出有关物质的化学式:A_______ ;E ________ 。
(2)X的一种用途_________ 。
(3)D与E反应的化学方程式________ ,该反应_____ (填“是”或“不是”)置换反应。

请根据以上信息回答下列问题:
(1)写出有关物质的化学式:A
(2)X的一种用途
(3)D与E反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】早在春秋战国时期我国就开始生产和使用铁器,工业上炼铁的原理是利用一氧化碳和氧化铁反应,实验装置如图所示,回答下列问题。___________ 。
(2)实验一段时间后,玻璃管中观察到的现象是___________ ,发生反应的化学方程式为___________ 。
(3)右边导气管口放置点燃的酒精灯的目的是___________ 。
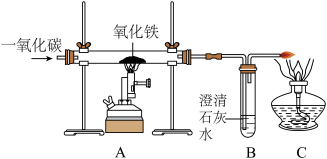
(2)实验一段时间后,玻璃管中观察到的现象是
(3)右边导气管口放置点燃的酒精灯的目的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】在浓硫酸催化作用下,固体草酸(H2C2O4)受热分解生成水和碳的氧化物。
某化学课外兴趣小组对生成物中碳的氧化物的种类进行了如下探究。
【提出问题】生成物中有哪几种碳的氧化物?
【猜想与假设】
(1)猜想1:只有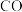 ;
;
猜想2:只有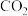 ;
;
猜想3:含有______ 。
【设计实验】兴趣小组同学设计了如图装置:
(2)实验过程中观察到装置A中澄清石灰水变浑浊,证明有______ 气体。
(3)装置B中盛放的药品名称为______ 。装置C的作用为______ 。
(4)如果发现C中澄清石灰水不变浑浊,E装置中黑色粉末变______ ,F中澄清石灰水______ ,证明有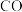 气体。E中反应的化学方程式为
气体。E中反应的化学方程式为______ 。
(5)装置最后酒精灯的作用是______ 。
【实验结论】通过探究证明:猜想3成立。
某化学课外兴趣小组对生成物中碳的氧化物的种类进行了如下探究。
【提出问题】生成物中有哪几种碳的氧化物?
【猜想与假设】
(1)猜想1:只有
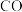 ;
;猜想2:只有
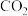 ;
;猜想3:含有
【设计实验】兴趣小组同学设计了如图装置:

(2)实验过程中观察到装置A中澄清石灰水变浑浊,证明有
(3)装置B中盛放的药品名称为
(4)如果发现C中澄清石灰水不变浑浊,E装置中黑色粉末变
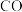 气体。E中反应的化学方程式为
气体。E中反应的化学方程式为(5)装置最后酒精灯的作用是
【实验结论】通过探究证明:猜想3成立。
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】碳酸钠广泛用于造纸、纺织、玻璃、洗涤剂、肥皂、制革等工业,是一种重要的化工原料。吕布兰、索尔维和侯德榜为碳酸钠的工业化生产作出了巨大贡献。
Ⅰ、吕布兰法1789年,法国医生吕布兰(N.Leblanc,1742—1806)以食盐、浓硫酸,木炭和石灰石为原料,开创了规模化工业制取碳酸钠的先河,具体流程如下:
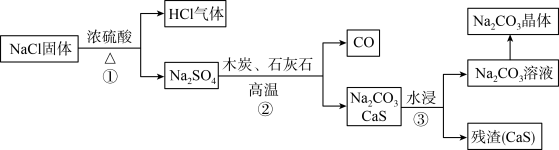
(1)在高温条件下,②中发生两步反应,其中一步是Na2SO4和木炭生成Na2S和CO,该反应的化学方程式为_______ 。
(2)不断有科学家对吕布兰法进行改进,是因为此法有明显不足,请写出一条不足之处____ 。
Ⅱ.索尔维法
1892年,比利时工程师索尔维发明氨碱法制碳酸钠,又称索尔维法。原理如下:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,2NaHCO3 Na2CO3+CO2↑+H2O。某兴趣小组采用下列装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。
Na2CO3+CO2↑+H2O。某兴趣小组采用下列装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。
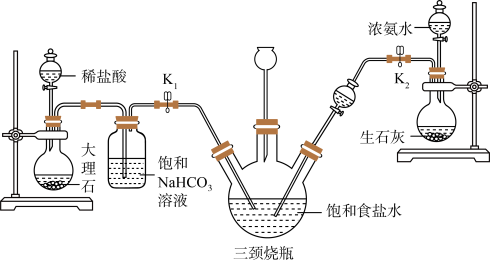
实验操作如下:
①关闭K1,打开K2通入NH3,调节气流速率,待其稳定后,打开K1通入CO2;
②待三颈烧瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭K1停止通CO2;
③将三颈烧瓶内的反应混合物过滤、洗涤、低温干燥,并将所得固体置于敞口容器中加热,记录剩余固体质量。
请回答下列问题:
(3)饱和NaHCO3溶液的作用是除去CO2中混有的HCl,反应的化学方程式为_______ 。
(4)有同学认为应该在长颈漏斗内放置一团蘸有酸液的棉花,理由是_______ ;关闭K2停止通NH3后,还要继续通一段时间CO2,其目的是_______ 。
(5)根据实验记录,计算t2时NaHCO3固体的分解率____ (已分解的NaHCO3质量与加热前原NaHCO3质量的比值),请写出计算过程。若加热前NaHCO3固体中还存在少量NaCl,上述计算结果将____ (填“偏大”、“偏小”或“无影响”)。
Ⅰ、吕布兰法1789年,法国医生吕布兰(N.Leblanc,1742—1806)以食盐、浓硫酸,木炭和石灰石为原料,开创了规模化工业制取碳酸钠的先河,具体流程如下:

(1)在高温条件下,②中发生两步反应,其中一步是Na2SO4和木炭生成Na2S和CO,该反应的化学方程式为
(2)不断有科学家对吕布兰法进行改进,是因为此法有明显不足,请写出一条不足之处
Ⅱ.索尔维法
1892年,比利时工程师索尔维发明氨碱法制碳酸钠,又称索尔维法。原理如下:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,2NaHCO3
 Na2CO3+CO2↑+H2O。某兴趣小组采用下列装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。
Na2CO3+CO2↑+H2O。某兴趣小组采用下列装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。
实验操作如下:
①关闭K1,打开K2通入NH3,调节气流速率,待其稳定后,打开K1通入CO2;
②待三颈烧瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭K1停止通CO2;
③将三颈烧瓶内的反应混合物过滤、洗涤、低温干燥,并将所得固体置于敞口容器中加热,记录剩余固体质量。
| 加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
| 剩余固体质量/g | 未记录 | 15.3 | 13.7 | 11.9 | 10.6 | 10.6 |
(3)饱和NaHCO3溶液的作用是除去CO2中混有的HCl,反应的化学方程式为
(4)有同学认为应该在长颈漏斗内放置一团蘸有酸液的棉花,理由是
(5)根据实验记录,计算t2时NaHCO3固体的分解率
您最近一年使用:0次



