(1)据报道,一辆载有20多吨浓硝酸的罐车不慎侧翻,造成大量硝酸泄漏,有关部门调来大量熟石灰粉[主要成分Ca(OH)2]和沙土用于清除泄漏的硝酸.试写出硝酸和熟石灰反应的化学方程式_______________ 。
(2)陕西紫阳富硒茶历史悠久,现用pH试纸测定种植富硒茶土壤溶液的pH,测定的具体方法是_____________ 。
(3)硒(Se)是人体所需要的重要矿物质营养素,有“抗癌之王”的美称,硒的原子序数为34,其相对原子质量为79,硒原子最外电子层上有6个电子,则下列说法中,不正确的是______ (填选项序号)
①硒为非金属元素
②一个硒原子的原子核内有34个质子
③硒原子很容易失去电子
④富硒茶中的硒元素以化合物形态存在
(2)陕西紫阳富硒茶历史悠久,现用pH试纸测定种植富硒茶土壤溶液的pH,测定的具体方法是
(3)硒(Se)是人体所需要的重要矿物质营养素,有“抗癌之王”的美称,硒的原子序数为34,其相对原子质量为79,硒原子最外电子层上有6个电子,则下列说法中,不正确的是
①硒为非金属元素
②一个硒原子的原子核内有34个质子
③硒原子很容易失去电子
④富硒茶中的硒元素以化合物形态存在
更新时间:2018-03-31 04:26:49
|
相似题推荐
【推荐1】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)工业上生产尿素[CO(NH2)2]的反应微观示意图如图:
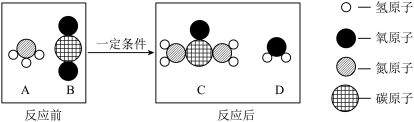
①从宏观的角度看,图中四种物质属于氧化物的有_____ (填字母序号)
②写出工业上生产尿素的化学方程式_____ 。
(2)如表是元素周期表中第2、3周期的元素,请回答有关问题。
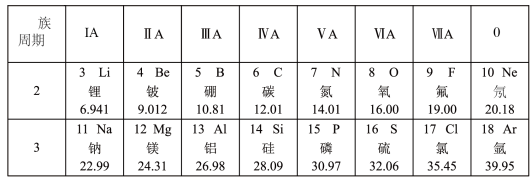
①下列各组具有相似化学性质的元素是______ (填字母序号);
A.Na、Cl B.O、S C.F、Cl D.Cl、Ar
②写出一条第三周期元素原子的核外电子排布规律______
③某粒子的结构示意图为 ,当x﹣y=8时,该粒子的符号为
,当x﹣y=8时,该粒子的符号为_____ ;
④具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是_____ (填字母序号)。
A.NO和O2 B.CO和N2 C.SO2和CO2 D. 和
和
(1)工业上生产尿素[CO(NH2)2]的反应微观示意图如图:

①从宏观的角度看,图中四种物质属于氧化物的有
②写出工业上生产尿素的化学方程式
(2)如表是元素周期表中第2、3周期的元素,请回答有关问题。

①下列各组具有相似化学性质的元素是
A.Na、Cl B.O、S C.F、Cl D.Cl、Ar
②写出一条第三周期元素原子的核外电子排布规律
③某粒子的结构示意图为
 ,当x﹣y=8时,该粒子的符号为
,当x﹣y=8时,该粒子的符号为④具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组粒子中属于等电子体的是
A.NO和O2 B.CO和N2 C.SO2和CO2 D.
 和
和
您最近半年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】核电荷数为1~18的元素的原子结构示意图等信息如下,回答有关问题:
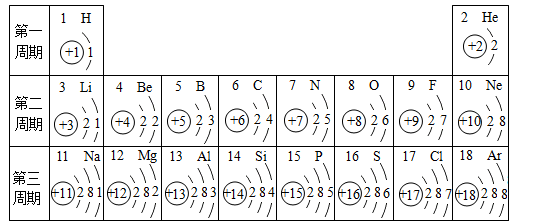
(1)含氟物质的合成,对推动科技进步发挥着巨大作用,由上图可知,氟原子在化学反应中易______ 电子(选填“失去”或“得到”);氟元素与氯元素位于同一纵行的原因是________________ 。
(2)在点燃的条件下,1号元素组成的单质能在17号元素组成的单质中燃烧,请写出该反应的化学方程式_____________ 。
(3)以钠和氯为例,简述结构与性质的关系______________ 。
(4)钠在氯气中燃烧生成氯化钠,4.6g钠完全转化为氯化钠,至少需要氯气的质量是_________ ?(写出计算过程)

(1)含氟物质的合成,对推动科技进步发挥着巨大作用,由上图可知,氟原子在化学反应中易
(2)在点燃的条件下,1号元素组成的单质能在17号元素组成的单质中燃烧,请写出该反应的化学方程式
(3)以钠和氯为例,简述结构与性质的关系
(4)钠在氯气中燃烧生成氯化钠,4.6g钠完全转化为氯化钠,至少需要氯气的质量是
您最近半年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】“宏观辨识与微观探析”是化学的核心素养之一、请回答下列问题:
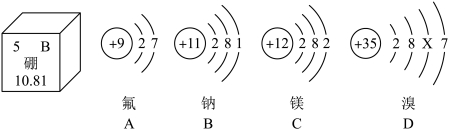
(1)从图中可知,硼元素的原子序数是______ 。
(2)钠元素位于元素周期表第______ 周期,该元素在反应中易______ (填“得到”或“失去”)电子,形成的离子符号为______ 。
(3)溴(Br)原子的原子结构示意图如图所示,A﹣D四种元素中,与溴元素化学性质相似的是______ (填写元素符号)。
(4)近年来,科学家在宇宙深处发现了H3和 粒子。下列有关说法正确的是______。
粒子。下列有关说法正确的是______。

(1)从图中可知,硼元素的原子序数是
(2)钠元素位于元素周期表第
(3)溴(Br)原子的原子结构示意图如图所示,A﹣D四种元素中,与溴元素化学性质相似的是
(4)近年来,科学家在宇宙深处发现了H3和
 粒子。下列有关说法正确的是______。
粒子。下列有关说法正确的是______。A.H3和 具有相同的质子数和电子数 具有相同的质子数和电子数 |
| B.一个H3分子是由3个氢原子构成 |
| C.由于H3和H2组成元素相同,所以它们性质相同 |
D.构成H3分子的原子的结构示意图为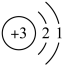 |
您最近半年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】酸与碱发生中和反应,其实质是酸溶液中大量自由移动的H+和碱溶液中大量自由移动的OH-结合生成水分子的过程。请根据以下稀盐酸与稀氢氧化钠溶液反应的实验,回答问题。
(1)向一试管中倒入约2mL稀氢氧化钠溶液,滴加3滴酚酞试液,振荡,再逐滴滴入稀盐酸,边滴边振荡,直至溶液刚好变为________ 色为止,说明它们之间发生了中和反应。
【实验二】用温度计
(2)向一烧杯中加入一定量的稀氢氧化钠溶液,再逐滴匀速加入稀盐酸,并用数字化仪器对反应过程中溶液的温度实时测定,得到的曲线如图-1。
①约0-50s温度上升是因为中和反应放热,50s后溶液温度下降的原因是__________ 。
②不能用氢氧化钠固体与稀盐酸反应测定中和反应放热的原因是__________ 。

【实验三】用pH计
(3)向一锥形瓶中加入20g质量分数为4%的稀氢氧化钠溶液,再逐滴匀速加入一定质量分数的稀盐酸,并用数字化仪器对反应过程中溶液的pH测定,得到的曲线如图-2。列式计算:
①所取稀盐酸的质量分数为多少__________ ?(精确到0. 0 l %,下同)
②当恰好完全反应时所得溶液的溶质质量分数为多少__________ ?
(1)向一试管中倒入约2mL稀氢氧化钠溶液,滴加3滴酚酞试液,振荡,再逐滴滴入稀盐酸,边滴边振荡,直至溶液刚好变为
【实验二】用温度计
(2)向一烧杯中加入一定量的稀氢氧化钠溶液,再逐滴匀速加入稀盐酸,并用数字化仪器对反应过程中溶液的温度实时测定,得到的曲线如图-1。
①约0-50s温度上升是因为中和反应放热,50s后溶液温度下降的原因是
②不能用氢氧化钠固体与稀盐酸反应测定中和反应放热的原因是

【实验三】用pH计
(3)向一锥形瓶中加入20g质量分数为4%的稀氢氧化钠溶液,再逐滴匀速加入一定质量分数的稀盐酸,并用数字化仪器对反应过程中溶液的pH测定,得到的曲线如图-2。列式计算:
①所取稀盐酸的质量分数为多少
②当恰好完全反应时所得溶液的溶质质量分数为多少
您最近半年使用:0次
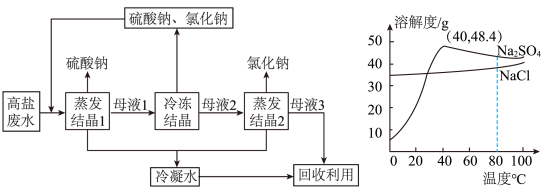
【推荐2】为研究溶解度曲线的应用,学习小组查得资料:某钢铁厂处理高盐废水(含氯化钠、硫酸钠及微量的其他盐)的流程、相关物质的溶解度曲线如图所示。请和小组同学一起研究。
(1)废水中的硫酸钠是氢氧化钠和硫酸反应的生成物,化学方程式为______ 。
(2)40℃时,将50g硫酸钠固体加入100g水中,充分搅拌后所得溶液的溶质质量分数为______ (列出计算式即可)。
(3)降温至0℃的“冷冻结晶”过程,析出的两种物质中较多的是______ 。
(4)将“高盐废水”在80℃蒸发浓缩至有少量固体析出。该小组分析溶解度曲线,推测析出的少量固体是NaCl,但检验后却发现是Na2SO4。请作出合理解释:______ 。
(5)结合流程图和溶解度曲线解释,“蒸发结晶2”主要得到氯化钠的原因是______ 。
(6)“蒸发结晶!”后,该小组停止蒸发浓缩,经冷冻结晶、______ ,得到大量Na2SO4固体及母液1;“蒸发结晶2”后将母液3中的NaCl分离出来,操作是:加热至有大量晶体析出,趁热过滤,______ 。

(1)废水中的硫酸钠是氢氧化钠和硫酸反应的生成物,化学方程式为
(2)40℃时,将50g硫酸钠固体加入100g水中,充分搅拌后所得溶液的溶质质量分数为
(3)降温至0℃的“冷冻结晶”过程,析出的两种物质中较多的是
(4)将“高盐废水”在80℃蒸发浓缩至有少量固体析出。该小组分析溶解度曲线,推测析出的少量固体是NaCl,但检验后却发现是Na2SO4。请作出合理解释:
(5)结合流程图和溶解度曲线解释,“蒸发结晶2”主要得到氯化钠的原因是
(6)“蒸发结晶!”后,该小组停止蒸发浓缩,经冷冻结晶、
您最近半年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组在实验室制取二氧化碳,并对产生的酸性废液进行处理。
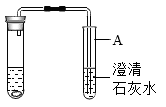
(1)实验室制取二氧化碳并进行检验。
①实验室制取二氧化碳的化学方程式为_______ 。
②实验中试管A中溶液可能出现不同现象。若A中出现白色浑浊,则其反应的化学方程式为_______ 。若A中未出现白色浑浊,则发生装置导出的二氧化碳中混有的气体为_______ (填“一氧化碳”或“氯化氢”)。
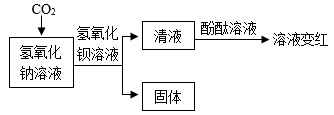
(2)若制取二氧化碳时所用药品和操作均合理,并将A试管中液体换为氢氧化钠溶液。为探究用足量NaOH溶液吸收CO2后溶液中溶质成分,某同学进行了如下图所示的操作,并得出溶质成分为碳酸钠和氢氧化钠。请说明该方案中的错误及其理由,并加以改正_______ 。
(3)制取CO2后的酸性废液需处理,得到中性溶液后再排放,处理的方法可以加入熟石灰,请简述操作步骤_____ 。
(4)若探究实验中所用盐酸的质量分数为7.3%,用适量Na2CO3处理废液,通过蒸发得到氯化钠的质量为117g,则本次探究实验至少需要盐酸的质量是_____ ?

(1)实验室制取二氧化碳并进行检验。
①实验室制取二氧化碳的化学方程式为
②实验中试管A中溶液可能出现不同现象。若A中出现白色浑浊,则其反应的化学方程式为
(2)若制取二氧化碳时所用药品和操作均合理,并将A试管中液体换为氢氧化钠溶液。为探究用足量NaOH溶液吸收CO2后溶液中溶质成分,某同学进行了如下图所示的操作,并得出溶质成分为碳酸钠和氢氧化钠。请说明该方案中的错误及其理由,并加以改正

(3)制取CO2后的酸性废液需处理,得到中性溶液后再排放,处理的方法可以加入熟石灰,请简述操作步骤
(4)若探究实验中所用盐酸的质量分数为7.3%,用适量Na2CO3处理废液,通过蒸发得到氯化钠的质量为117g,则本次探究实验至少需要盐酸的质量是
您最近半年使用:0次
【推荐1】分类、类比是学习化学常用的方法,掌握这些方法有助于学生学习化学知识。
(1)初中化学有许多实验,若按照实验主要目的可将实验分为:探究物质发生化学反应前后质量关系,探究物质的性质,探究物质的含量等。据此应将下列实验中的D与_______________ (填“A”或“B”或“C”)归为一类,依据是_______________ 。
(2)通过分析物质的组成和结构,我们可以预测物质的某些性质。已知 NaHSO4在水中能解离出Na+、H+和 ,则关于它性质的下列推测,合理的是
,则关于它性质的下列推测,合理的是_______________ 。
A.其水溶液能使紫色石蕊试液变红
B.其水溶液能与钾发生置换反应,得到金属钠
C.向 NaHSO4溶液中逐滴加入氨水的过程中,溶液的pH会变大
类比金属单质间的置换反应,某些非金属单质间也能发生置换反应,如: ,可以判断非金属活动性:Cl2>Br2。通过
,可以判断非金属活动性:Cl2>Br2。通过 ,可以得出Cl2、Br2、I2的非金属活动性顺序为
,可以得出Cl2、Br2、I2的非金属活动性顺序为______________ 。
(1)初中化学有许多实验,若按照实验主要目的可将实验分为:探究物质发生化学反应前后质量关系,探究物质的性质,探究物质的含量等。据此应将下列实验中的D与
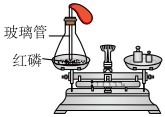 | 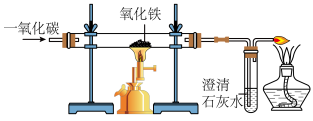 | 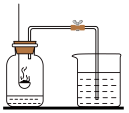 | 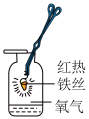 |
| A | B | C | D |
 ,则关于它性质的下列推测,合理的是
,则关于它性质的下列推测,合理的是A.其水溶液能使紫色石蕊试液变红
B.其水溶液能与钾发生置换反应,得到金属钠
C.向 NaHSO4溶液中逐滴加入氨水的过程中,溶液的pH会变大
类比金属单质间的置换反应,某些非金属单质间也能发生置换反应,如:
 ,可以判断非金属活动性:Cl2>Br2。通过
,可以判断非金属活动性:Cl2>Br2。通过 ,可以得出Cl2、Br2、I2的非金属活动性顺序为
,可以得出Cl2、Br2、I2的非金属活动性顺序为
您最近半年使用:0次
【推荐2】构建知识网络模型是化学学习中重要的学习方法。如图1是小明同学利用左手构建的酸的化学性质知识网络(其中A、B表示反应物,C表示生成物)。

请完成下列问题:
(1)如用湿润的pH试纸测定盐酸的pH,则结果会___________ (填“偏大”“偏小”或“无影响”)。
(2)世界卫生组织推广使用中国铁锅,使用铁锅炒菜时,放点食醋可以补充人体中构成血红素的___________ (填“Fe2+”或“Fe3+”),该反应的原理是利用了酸的___________ (填数字序号“②”“③”“④”或“⑤”)化学性质。
(3)小明用图2来说明稀硫酸与氢氧化钠溶液反应的过程,该过程不发生变化的微粒是_______ (用微粒符号表示),该反应的微观实质可表示为___________ 。
(4)如下图所示为氯化钠和硝酸钾的溶解度曲线。
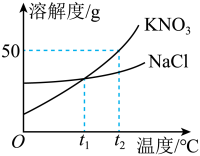
①将KNO3和NaC1的饱和溶液各100g由t2℃降温到t1℃,析出晶体质量较多的是___________ 。
②t2℃时,将30gKNO3物质加入50g水中,充分溶解后溶液的质量为___________ g。

请完成下列问题:
(1)如用湿润的pH试纸测定盐酸的pH,则结果会
(2)世界卫生组织推广使用中国铁锅,使用铁锅炒菜时,放点食醋可以补充人体中构成血红素的
(3)小明用图2来说明稀硫酸与氢氧化钠溶液反应的过程,该过程不发生变化的微粒是
(4)如下图所示为氯化钠和硝酸钾的溶解度曲线。

①将KNO3和NaC1的饱和溶液各100g由t2℃降温到t1℃,析出晶体质量较多的是
②t2℃时,将30gKNO3物质加入50g水中,充分溶解后溶液的质量为
您最近半年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】酸、碱、盐在生产、生活中有广泛的应用。
(1)稀盐酸、稀硫酸都能除铁锈,写出用稀硫酸除铁锈的化学方程式_______ 。
(2)氢氧化钠溶液与稀硫酸反应时,溶液pH变化如图所示。

①据图判断,该实验是将______ 滴入到另一种溶液中(填“氢氧化钠溶液”或“稀硫酸”)。
②滴入溶液体积为V2mL时,溶液中溶质为______ (填化学式)。
③测定某酸溶液pH时,如果放pH试纸的玻璃片上的水没有擦干就进行测定,会使测得的pH_______ (填“偏大”或“偏小”)。
(3)粗盐中常含有少量CaCl2、MgCl2、Na2SO4等杂质,将粗盐进行精制的流程如图所示:

①过量X(纯净物)溶液中溶质的化学式是______ 。
②加入过量稀盐酸的目的可以除去滤液中过量的碳酸钠,还有一个作用是______ (用化学方程式表示)。
③在操作Ⅲ中玻璃棒的作用是______ 。
(4)取10g已部分变质的氢氧化钠固体样品于烧杯中,加足量水溶解;向其中加入足量的CaC12溶液,恰好完全反应后,生成沉淀质量为5g。计算该样品中氢氧化钠的质量______ 。
(1)稀盐酸、稀硫酸都能除铁锈,写出用稀硫酸除铁锈的化学方程式
(2)氢氧化钠溶液与稀硫酸反应时,溶液pH变化如图所示。

①据图判断,该实验是将
②滴入溶液体积为V2mL时,溶液中溶质为
③测定某酸溶液pH时,如果放pH试纸的玻璃片上的水没有擦干就进行测定,会使测得的pH
(3)粗盐中常含有少量CaCl2、MgCl2、Na2SO4等杂质,将粗盐进行精制的流程如图所示:

①过量X(纯净物)溶液中溶质的化学式是
②加入过量稀盐酸的目的可以除去滤液中过量的碳酸钠,还有一个作用是
③在操作Ⅲ中玻璃棒的作用是
(4)取10g已部分变质的氢氧化钠固体样品于烧杯中,加足量水溶解;向其中加入足量的CaC12溶液,恰好完全反应后,生成沉淀质量为5g。计算该样品中氢氧化钠的质量
您最近半年使用:0次



