为测定某纯碱(Na2CO3)样品中(含有少量的氯化钠杂质)碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当稀盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(产生的气体全部逸出)。产生气体的质量与滴入稀盐酸的质量关系如图所示,
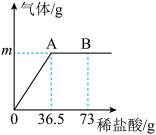
(1)A点产生气体的质量m为_______, 此时所得溶液的溶质质量为 ______。
(2)B点时,烧杯内溶液中粒子有__________________________。(写粒子符号)

(1)A点产生气体的质量m为_______, 此时所得溶液的溶质质量为 ______。
(2)B点时,烧杯内溶液中粒子有__________________________。(写粒子符号)
更新时间:2018-05-11 22:08:39
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】某同学为探究铜锌合金中锌的质量分数,先后进行了三次实验,(杂质不溶于水,也不参加反应)实验数据如下表:
根据该同学的实验,试回答以下问题:
(1)上表三次实验中,合金里的锌恰好完全反应时,消耗稀硫酸溶液的质量与合金的质量比是______ 。
(2)该铜锌合金中锌的质量分数是多少?
| 实验次数 项目 | 第一次 | 第二次 | 第三次 |
| 所取合金的质量/g | 10 | 10 | 20 |
| 所加稀硫酸的质量/g | 50 | 60 | 40 |
| 生成氢气的质量/g | 0.2 | 0.2 | 0.2 |
根据该同学的实验,试回答以下问题:
(1)上表三次实验中,合金里的锌恰好完全反应时,消耗稀硫酸溶液的质量与合金的质量比是
(2)该铜锌合金中锌的质量分数是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】化学兴趣小组为测定某石灰石样品中碳酸钙的质量分数,取30g石灰石样品放在烧杯中,然后向其中逐渐加入稀盐酸,使之与样品充分反应,恰好完全反应(杂质不参加反应)时,加入稀盐酸的质量为97g,反应后烧杯中物质的总质量为116g。
请计算:
(1)反应生成二氧化碳的质量为 克。
(2)样品中碳酸钙的质量;
(3)反应后的溶液中溶质的质量分数。
请计算:
(1)反应生成二氧化碳的质量为 克。
(2)样品中碳酸钙的质量;
(3)反应后的溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】某地石灰石资源丰富。石灰石经高温煅烧可得到生石灰产品。小奕同学为了测定某生石灰产品中是否含有碳酸钙杂质(其它杂质忽略不计),取6.6g样品进行测定。
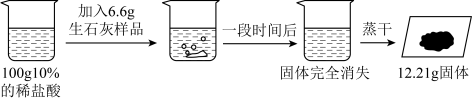
(1)计算6.6gCaO和足量的稀盐酸反应生成氯化钙的质量;(结果保留一位小数)
(2)下图是小奕同学的实验流程图,请根据相关数据计算该样品中CaCO3的质量。

(1)计算6.6gCaO和足量的稀盐酸反应生成氯化钙的质量;(结果保留一位小数)
(2)下图是小奕同学的实验流程图,请根据相关数据计算该样品中CaCO3的质量。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
所加盐酸的次数 第一次 第二次 第三次 第四次
烧杯及所盛物质总质量/g 181.2 204.4 228.6 253.6
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是 g.
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线.(不要求写出计算过程,只画出曲线即可)
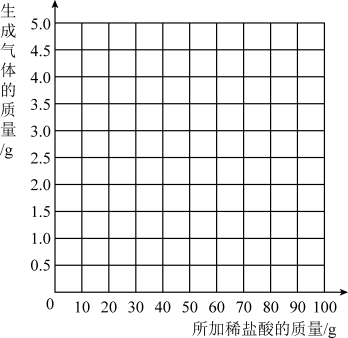
所加盐酸的次数 第一次 第二次 第三次 第四次
烧杯及所盛物质总质量/g 181.2 204.4 228.6 253.6
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是 g.
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线.(不要求写出计算过程,只画出曲线即可)

您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】28.7g的氯化钠和硝酸钠的混合物,溶于100g水中,向所得溶液中加入134g的硝酸银溶液,恰好完全反应,得到溶液的质量是234g.计算:原混合物中钠元素的质量分数.(已知:AgNO3+NaCl=AgCl↓+NaNO3;计算结果精确到1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】现有 H2SO4与 CuSO4的混合溶液,为了分析混合溶液中 H2SO4与 CuSO4的质量分数, 设计了如图所示的实验方案(注:硫酸铜溶液略显酸性)。
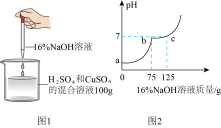
(1) c点表示混合溶液与 NaOH 恰好反应完全,此点溶液中的溶质为________(写化学式)。
(2)与硫酸铜溶液反应的氢氧化钠溶液的质量为____________g;请计算该混合溶液中 CuSO4的溶质质量分数(写出具体计算过程)。
(3)若在 100g 混合溶液中不断加入上述氢氧化钠的溶液,请你画出加入氢氧化钠溶液的质量与产生沉淀的质量的关系图(标出曲线中必要的数据)_________。

(4)在图2所示的曲线中,b-c段表示的溶液pH稍小于7,其原因是___________。

(1) c点表示混合溶液与 NaOH 恰好反应完全,此点溶液中的溶质为________(写化学式)。
(2)与硫酸铜溶液反应的氢氧化钠溶液的质量为____________g;请计算该混合溶液中 CuSO4的溶质质量分数(写出具体计算过程)。
(3)若在 100g 混合溶液中不断加入上述氢氧化钠的溶液,请你画出加入氢氧化钠溶液的质量与产生沉淀的质量的关系图(标出曲线中必要的数据)_________。

(4)在图2所示的曲线中,b-c段表示的溶液pH稍小于7,其原因是___________。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】小明同学为了测定市面销售的某品牌纯碱中碳酸钠的质量分数(杂质为氯化钠,氯化钠溶于水且不与氯化钙反应),进行了如下实验:①在三个烧杯中分别加入11.0g 样品及足量的水配成溶液;②向三个烧杯中分别加入一定质量的10.0%的氯化钙溶液;③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体。实验所得数据见下表,请你分析并进行有关计算:
(1)在图中绘制出白色沉淀与加入氯化钙溶液的质量关系图(图上要注明白色沉淀、氯化钙溶液的相关质量)。______

(2)样品中碳酸钠的质量分数是_____?(结果精确到0.1%)
(3)烧杯Ⅱ所得溶液中氯化钠的溶质质量分数是_______?(结果精确到0.1%)
| 烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
| 加入10.0%氯化钙溶液的质量/g | 55.5 | 120.0 | 150.0 |
| 白色固体的质量/g | 5.0 | 10.0 | 10.0 |

(2)样品中碳酸钠的质量分数是_____?(结果精确到0.1%)
(3)烧杯Ⅱ所得溶液中氯化钠的溶质质量分数是_______?(结果精确到0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
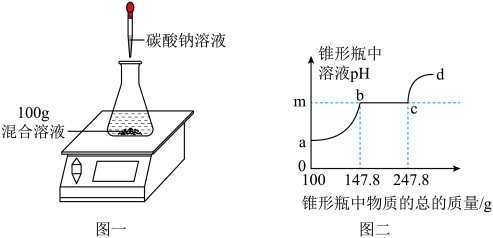
【推荐1】欲测定盐酸与氯化钙的混合溶液中氯化钙的质量分数,进行了如下实验:取混合溶液100g于锥形瓶中,向其中逐渐加入一定溶质质量分数的碳酸钠溶液(如图一),并不断测定锥形瓶中溶液的pH.反应过程中所得溶液的pH与锥形瓶中物质的总质量的关系如图二所示。
(1)m点的数值是___ 。
(2)a﹣b段表示碳酸钠与混合溶液中的___ 反应。
(3)b点的溶质为___ 。
(4)参加反应的碳酸钠溶液的溶质的质量分数是___ 。(写出计算过程)
(5)请计算原混合溶液中CaCl2的质量分数为___ 。(写出计算过程)
(1)m点的数值是
(2)a﹣b段表示碳酸钠与混合溶液中的
(3)b点的溶质为
(4)参加反应的碳酸钠溶液的溶质的质量分数是
(5)请计算原混合溶液中CaCl2的质量分数为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】现有13.4g固体氯化钙样品(含杂质氯化钠),为了测定样品中氯化钙的含量,将此固体全部溶于96.6g水中,向所得的混合溶液中滴加一定质量分数的碳酸钠溶液,记录了如图所示的曲线关系。提示:氯化钙与碳酸钠反应的化学方程式:CaCl2+Na2CO3 =CaCO3↓+2NaCl。
求:(第2问要求写出计算过程)
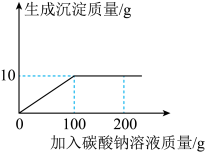
(1)当氯化钙与碳酸钠恰好完全反应时,消耗碳酸钠溶液 的质量是_________g。
(2)氯化钙与碳酸钠恰好完全反应后所得溶液中溶质的质量 是多少_______?
求:(第2问要求写出计算过程)

(1)当氯化钙与碳酸钠恰好完全反应时,消耗
(2)氯化钙与碳酸钠恰好完全反应后所得溶液中溶质的
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】工业纯碱中常含有少量的氯化钠。某学习小组对其组成展开探究。现取50g纯碱样品,加入200g水使其完全溶解,再加入190g过量的氯化钙溶液,完全反应后,过滤、洗涤、干燥得到沉淀40g。完成下列问题:
(1)通过已知数据,能求出的量有 (写字母序号)。
A 反应后溶液的总质量
B 参加反应的氯化钙的质量
C 样品中碳酸钠的质量分数
D 氯化钙溶液中溶质的质量分数
(2)参加反应的氯化钙的质量为 g。
(3)计算纯碱样品的纯度。(写出计算过程,结果保留到0.1%)。
(1)通过已知数据,能求出的量有 (写字母序号)。
A 反应后溶液的总质量
B 参加反应的氯化钙的质量
C 样品中碳酸钠的质量分数
D 氯化钙溶液中溶质的质量分数
(2)参加反应的氯化钙的质量为 g。
(3)计算纯碱样品的纯度。(写出计算过程,结果保留到0.1%)。
您最近一年使用:0次





