化学是以实验为基础的科学,实验是科学探究的重要手段。
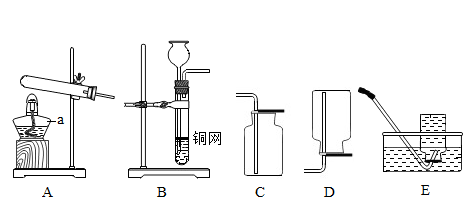
(1)如图是初中化学常见的仪器和装置,请回答下列问题。
①写出a的名称____________ ;②实验室选用装置A、E组合制取氧气,写出反应的化学方程式__________ ;③实验室用B、C装置制取二氧化碳时,若用铁丝网代替铜网,产生的后果是__________ 。
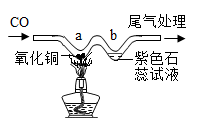
(2)如图所示,用“W”型玻璃管进行微型实验。
①b处发生的现象是_____________ ;②写出a处发生反应的化学方程式__________ ;③请简述该实验的尾气处理方法_____________ 。
(3)可燃冰(天然气水合物)是资源量丰富的高效清洁能源。科学家开采出一种可燃冰,取100g样品放置在一密闭容器内,该样品迅速转化为甲烷和水,将甲烷分离并完全燃烧,得到35.2g二氧化碳。求该可燃冰样品中甲烷的质量分数(精确到0.1%)_____ 。

(1)如图是初中化学常见的仪器和装置,请回答下列问题。
①写出a的名称

(2)如图所示,用“W”型玻璃管进行微型实验。
①b处发生的现象是
(3)可燃冰(天然气水合物)是资源量丰富的高效清洁能源。科学家开采出一种可燃冰,取100g样品放置在一密闭容器内,该样品迅速转化为甲烷和水,将甲烷分离并完全燃烧,得到35.2g二氧化碳。求该可燃冰样品中甲烷的质量分数(精确到0.1%)
更新时间:2018/05/25 21:37:12
|
相似题推荐
科学探究题
|
适中
(0.65)
【推荐1】某同学将光亮的镁条放入滴有酚酞的 NaHCO3 饱和溶液中,产生大量气泡和
白色固体,溶液红色加深。
(一)溶液红色加深,则反应后溶液的碱性_____ (填“增强”“不变”或“减 弱”)。
(二)为确定气体和固体的成分,该同学进行了如下的探究。
(1)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象。 则该气体为_____ (写化学式)。
(2)对白色固体做出如下猜测并进行实验:
查阅资料 1:Mg(HCO3)2 能 溶于水。
查阅资料 2:MgCO3 、Mg(OH)2 加热易分解,分别生成一种金属氧化物和非金属 氧化物。
【猜测】:
①白色固体可能是 MgCO3;
②白色固体可能是_____ ;
③白色固体可能是 MgCO3 和 Mg(OH)2。
【实验】:
①取洗净后的白色固体,加入足量的_____ 溶液,观察到 _____ , 则白色固体一定含有 MgCO3。
②为进一步确定白色固体的组成,该同学进行了定量探究实验,如下图所示:
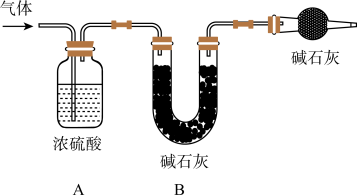
称取干燥的白色固体 22.6 g,充分加热至不再产生气体为止,并使分解产生的气体全部先通过浓硫酸,浓硫酸增重 1.8 g,然后再通过碱石灰(生石灰与氢氧化钠固体 的混合物),碱石灰增重 8.8 g,则固体中各成分的质量的最简比为_____ 。
【反思】:有同学提出将装置 A 与 B 对调也能测定固体混合物的组成,你______ “是 或否”)同意,你的理由是 _________ 。
白色固体,溶液红色加深。
(一)溶液红色加深,则反应后溶液的碱性
(二)为确定气体和固体的成分,该同学进行了如下的探究。
(1)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象。 则该气体为
(2)对白色固体做出如下猜测并进行实验:
查阅资料 1:Mg(HCO3)2 能 溶于水。
查阅资料 2:MgCO3 、Mg(OH)2 加热易分解,分别生成一种金属氧化物和非金属 氧化物。
【猜测】:
①白色固体可能是 MgCO3;
②白色固体可能是
③白色固体可能是 MgCO3 和 Mg(OH)2。
【实验】:
①取洗净后的白色固体,加入足量的
②为进一步确定白色固体的组成,该同学进行了定量探究实验,如下图所示:

称取干燥的白色固体 22.6 g,充分加热至不再产生气体为止,并使分解产生的气体全部先通过浓硫酸,浓硫酸增重 1.8 g,然后再通过碱石灰(生石灰与氢氧化钠固体 的混合物),碱石灰增重 8.8 g,则固体中各成分的质量的最简比为
【反思】:有同学提出将装置 A 与 B 对调也能测定固体混合物的组成,你
您最近一年使用:0次
科学探究题
|
适中
(0.65)
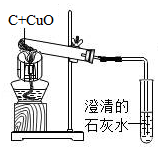
【推荐2】某校九年级“我们爱化学”活动小组的同学,在探究木炭与CuO反应时,完成了如下实验,请回答下列问题:
(1)请写出C与CuO反应的化学方程式___________ ;
(2)实验结束时,应___________ (填写下列操作代号)。
①先撤出导管,再熄灭酒精灯
②先熄灭酒精灯,再撤出导管
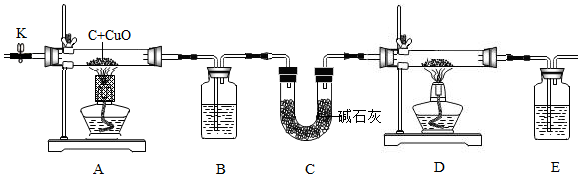
Ⅱ、小组中华雪同学通过仔细阅读教材,认为当木炭较多、温度较高时,该反应产生的气体中可能含有CO和CO2,小组的同学们在老师指导下设计实验进行了验证:
(3)仪器B中所盛试剂为___________ ,其作用为___________ 。
(4)D中玻璃管盛装的试剂为CuO,E中盛装的试剂为澄清的石灰水。若A装置产物中确有CO,则应观察到的现象有:___________ 。
(5)实验前,需检查___________ ;点燃酒精灯前,先打开K,通入N2一段时间,其作用为___________ 。
(6)请指出上述实验中的一项缺陷___________ 。
(7)将1.44g炭和16.0gCuO在较高温度下反应生成Cu,理论上可生成___________ gCO。
Ⅲ、小组中吴华同学通过查阅资料发现:Cu2O为红色固体,难溶于水,可与稀硫酸反应生成Cu和CuSO4。
(8)请设计简单实验验证CuO和足量炭反应后所得的红色固体中是否有Cu2O:___________ 。
(1)请写出C与CuO反应的化学方程式
(2)实验结束时,应
①先撤出导管,再熄灭酒精灯
②先熄灭酒精灯,再撤出导管
Ⅱ、小组中华雪同学通过仔细阅读教材,认为当木炭较多、温度较高时,该反应产生的气体中可能含有CO和CO2,小组的同学们在老师指导下设计实验进行了验证:
(3)仪器B中所盛试剂为
(4)D中玻璃管盛装的试剂为CuO,E中盛装的试剂为澄清的石灰水。若A装置产物中确有CO,则应观察到的现象有:
(5)实验前,需检查
(6)请指出上述实验中的一项缺陷
(7)将1.44g炭和16.0gCuO在较高温度下反应生成Cu,理论上可生成
Ⅲ、小组中吴华同学通过查阅资料发现:Cu2O为红色固体,难溶于水,可与稀硫酸反应生成Cu和CuSO4。
(8)请设计简单实验验证CuO和足量炭反应后所得的红色固体中是否有Cu2O:
您最近一年使用:0次
【推荐3】科学探究
爱吃饼干的同学在查看饼干配料表时,发现有些饼干的膨松剂含有碳酸氢钠,而有些饼干的膨松剂含有碳酸氢铵。同学们深感好奇,碳酸氢铵不是一种肥料吗?怎么也可以做膨松剂呢?为此,他们进行了如下的探究。
【查阅资料】
①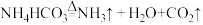 ;
;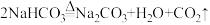
②通过控制碳酸氢铵的用量,不仅使残留在食品中的氨气含量符合食品安全标准,还能使食品具有独特的味道。
任务一 初识膨松剂
(1)膨松剂能使食品变松软、蓬松。碳酸氢铵、碳酸氢钠常用作膨松剂。碳酸氢铵别名碳铵,碳酸氢钠俗名是___________ 。
任务二 比较蓬松效果
(2)通过以上实验发现,加入碳酸氢铵的面团更大更松软,其原因是___________ 。
任务三 测定膨松剂中碳酸氢铵的含量
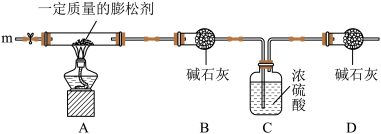
(3)膨松剂中的其他成分受热不分解,为测定膨松剂中碳酸氢铵的含量。同学们分别设计了实验方案。
①甲同学提出,加热一定质量的膨松剂,使其完全分解。通过测定反应前后物质的质量差来算出碳酸氢铵的含量。
②乙同学认为,膨松剂中可能含有水分,会影响实验结果。他提出可以通过测定反应后生成氨气的质量来达到实验目的,故设计了如图所示实验装置及主要步骤。
a.步骤4的具体操作是___________ ,若没有此操作,会使测量结果___________ (填“偏大”或“偏小”)。
b.装置D的作用是___________ 。
爱吃饼干的同学在查看饼干配料表时,发现有些饼干的膨松剂含有碳酸氢钠,而有些饼干的膨松剂含有碳酸氢铵。同学们深感好奇,碳酸氢铵不是一种肥料吗?怎么也可以做膨松剂呢?为此,他们进行了如下的探究。
【查阅资料】
①
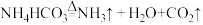 ;
;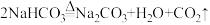
②通过控制碳酸氢铵的用量,不仅使残留在食品中的氨气含量符合食品安全标准,还能使食品具有独特的味道。
任务一 初识膨松剂
(1)膨松剂能使食品变松软、蓬松。碳酸氢铵、碳酸氢钠常用作膨松剂。碳酸氢铵别名碳铵,碳酸氢钠俗名是
任务二 比较蓬松效果
| 步骤 | 具体操作 | |
| 称量 | 10%面粉、0.5g碳酸氢钠置于蒸发皿中 | 10%面粉、0.5g碳酸氢铵置于蒸发皿中 |
| 和面 | 加入5mL水,用玻璃棒搅拌至水被吸干,揉搓成面团,盖上表面皿 | |
| 烘焙 | 模拟烘焙过程,用酒精灯加热约3min,熄灭酒精灯,停止实验 | |
(2)通过以上实验发现,加入碳酸氢铵的面团更大更松软,其原因是
任务三 测定膨松剂中碳酸氢铵的含量
(3)膨松剂中的其他成分受热不分解,为测定膨松剂中碳酸氢铵的含量。同学们分别设计了实验方案。
①甲同学提出,加热一定质量的膨松剂,使其完全分解。通过测定反应前后物质的质量差来算出碳酸氢铵的含量。
②乙同学认为,膨松剂中可能含有水分,会影响实验结果。他提出可以通过测定反应后生成氨气的质量来达到实验目的,故设计了如图所示实验装置及主要步骤。
| 实验装置及主要步骤(B、C、D中药品均足量,碱石灰是NaOH与CaO的固体混合物) |
步骤2:从m端通入氮气一段时间后,称量装置C的质量,记录; 步骤3:点燃酒精灯,充分反应后停止加热; 步骤4:… 步骤5:再次称量装置C的质量,记录,计算。 |
b.装置D的作用是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】兴趣小组同学在实验室用如图1所示的装置制取二氧化碳气体。
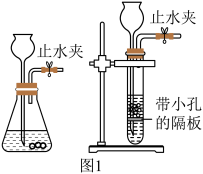
(1)请写出实验室检验二氧化碳的方法是______ 。B装置与A装置相比具有的优势是______ 。
实验结束后,兴趣小组的同学又对如何处理废液进行了如下探究。
(2)确定废液成分。
猜想一:______ (填化学式);
猜想二: 和
和 。
。
(3)已知氯化钙溶液呈中性,若要用一种试剂验证哪种推测成立,可选择的试剂是______(填序号)。
废液的处理。
实验表明废液中的溶质是 和
和 ,小组决定用
,小组决定用 除去它们。
除去它们。
【进行实验】取 废液样品于烧杯中,逐滴滴加5.3%的
废液样品于烧杯中,逐滴滴加5.3%的 溶液,用
溶液,用 传感器测定滴加过程中溶液的
传感器测定滴加过程中溶液的 。实验结果如图2所示。
。实验结果如图2所示。
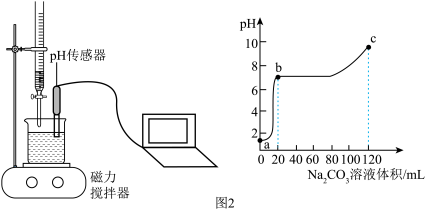
【结果讨论】
(4) 阶段,观察到烧杯中的现象是
阶段,观察到烧杯中的现象是______ 。
(5)b点后曲线平缓阶段,反应的化学方程式为______ 。
(6)c点时,取少量烧杯中的清液于试管中,滴加 溶液,有白色沉淀生成,说明处理
溶液,有白色沉淀生成,说明处理 废液,所需5.3%的
废液,所需5.3%的 溶液的体积
溶液的体积______ (选填“大于”“等于”或“小于”) 。
。

(1)请写出实验室检验二氧化碳的方法是
实验结束后,兴趣小组的同学又对如何处理废液进行了如下探究。
(2)确定废液成分。
猜想一:
猜想二:
 和
和 。
。(3)已知氯化钙溶液呈中性,若要用一种试剂验证哪种推测成立,可选择的试剂是______(填序号)。
| A.石蕊溶液 | B. 溶液 溶液 | C.氢氧化钙溶液 | D. 粉末 粉末 |
废液的处理。
实验表明废液中的溶质是
 和
和 ,小组决定用
,小组决定用 除去它们。
除去它们。【进行实验】取
 废液样品于烧杯中,逐滴滴加5.3%的
废液样品于烧杯中,逐滴滴加5.3%的 溶液,用
溶液,用 传感器测定滴加过程中溶液的
传感器测定滴加过程中溶液的 。实验结果如图2所示。
。实验结果如图2所示。
【结果讨论】
(4)
 阶段,观察到烧杯中的现象是
阶段,观察到烧杯中的现象是(5)b点后曲线平缓阶段,反应的化学方程式为
(6)c点时,取少量烧杯中的清液于试管中,滴加
 溶液,有白色沉淀生成,说明处理
溶液,有白色沉淀生成,说明处理 废液,所需5.3%的
废液,所需5.3%的 溶液的体积
溶液的体积 。
。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐2】实验一:实验室制备二氧化碳的实验如下.
(1)市售浓盐酸的标签局部如图1,为使制备过程中二氧化碳平稳地产生且较纯净,应将该浓盐酸_____ .
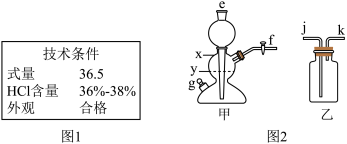
(2)用图2甲装置制备二氧化碳,选择的固体药品是_____ (填编号).
a 粉末状石灰石 b 块状大理石
c 粉末状熟石灰 d 块状生石灰
(3)控制所加盐酸的量,使反应时甲装置内液面位于_____ (填“x”或“y”)处为宜.
(4)收集二氧化碳时,应将甲的_____ 处与乙的_____ 处连接.(填有关编号)
(5)装置甲也可以用于实验室制取氢气,写出实验室制取氢气的化学方程式_____ .
实验二:某小组在学习“二氧化碳与氢氧化钠溶液反应”时,进行了如下探究:
【提出问题】二氧化碳与氢氧化钠反应,还是溶解在水中?
【查阅资料】
①15℃、101KPa时,二氧化碳的溶解度如表:
②15℃时,在酒精中氢氧化钠易溶、碳酸钠微溶.
③通常情况下,稀溶液的体积约等于溶剂的体积.
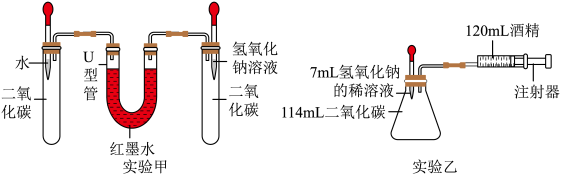
【实验设计】在15℃、101KPa时,制取二氧化碳并用于下图实验甲、实验乙.
【分析与表达】
(1)二氧化碳与氢氧化钠反应的化学方程式是_____ .
(2)实验前,两套装置都进行气密性检查,实验甲装置气密性检查的方法是_____ .
(3)实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是:右侧液面升高,左侧液面下降,一段时间后,右侧液面缓慢下降,左侧上升,最后右侧液面_____ (填“高于”或“低于”)左侧
(4)实验乙中,将氢氧化钠完全滴入锥形瓶中,注射器会自动向内移动并将酒精推入锥形瓶,活塞的移动速度是_____ .(填答案字母)实验乙中,还可能观察到的现象是__ .
A 先慢后快 B 先快后慢
(5)实验乙中,120mL酒精不能换成水,原因是_____ .
(1)市售浓盐酸的标签局部如图1,为使制备过程中二氧化碳平稳地产生且较纯净,应将该浓盐酸

(2)用图2甲装置制备二氧化碳,选择的固体药品是
a 粉末状石灰石 b 块状大理石
c 粉末状熟石灰 d 块状生石灰
(3)控制所加盐酸的量,使反应时甲装置内液面位于
(4)收集二氧化碳时,应将甲的
(5)装置甲也可以用于实验室制取氢气,写出实验室制取氢气的化学方程式
实验二:某小组在学习“二氧化碳与氢氧化钠溶液反应”时,进行了如下探究:
【提出问题】二氧化碳与氢氧化钠反应,还是溶解在水中?
【查阅资料】
①15℃、101KPa时,二氧化碳的溶解度如表:
②15℃时,在酒精中氢氧化钠易溶、碳酸钠微溶.
③通常情况下,稀溶液的体积约等于溶剂的体积.
| 溶剂 | 1.0L水 | 1.0L酒精 |
| 溶解度 | 1.0L | 0.5L |
【实验设计】在15℃、101KPa时,制取二氧化碳并用于下图实验甲、实验乙.

【分析与表达】
(1)二氧化碳与氢氧化钠反应的化学方程式是
(2)实验前,两套装置都进行气密性检查,实验甲装置气密性检查的方法是
(3)实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是:右侧液面升高,左侧液面下降,一段时间后,右侧液面缓慢下降,左侧上升,最后右侧液面
(4)实验乙中,将氢氧化钠完全滴入锥形瓶中,注射器会自动向内移动并将酒精推入锥形瓶,活塞的移动速度是
A 先慢后快 B 先快后慢
(5)实验乙中,120mL酒精不能换成水,原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】(1)化学是一门以实验为基础的科学,根据如图所示装置,回答相关问题。
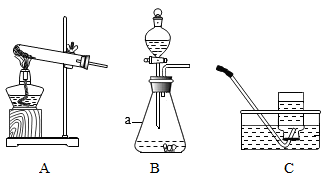
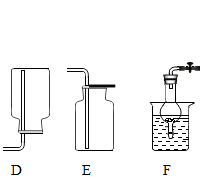
①图B中标有字母a的仪器名称是______ 。
②实验室用双氧水和二氧化锰制取氧气,该反应的化学方程式是______ ,若需收集一瓶氧气用于铁丝燃烧的实验,应选择的发生与收集装置的组合是______ (从A一E中选择,填字母)。
③装置F可以作为制取二氧化碳的发生装置,相比B装置其主要优点是______ 。
(2)纳米零价铁(单质铁)在环保领域应用广泛,以菱铁矿(主要成分为FeCO3不考虑杂质)为原料,制备纳米零价铁的反应为: 。反应一段时间后,某学习小组对剩余固体的成分进行探究。
。反应一段时间后,某学习小组对剩余固体的成分进行探究。
【提出问题】剩余固体的成分是什么?
【做出猜想】剩余固体的成分:
猜想一:Fe猜想二:FeCO3 猜想三:______ 。
【实验探究】该学习小组利用如图装置,对剩余固体成分进行探究,实验操作及现象如图。回答下列问题。
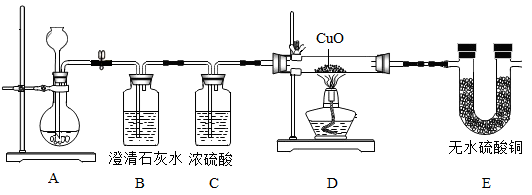
①向装置A中加入稀硫酸后,A中产生气泡且溶液变为浅绿色,小芳同学判断猜想一正确,小刚同学认为小芳的判断不合理,理由是:______ 。
②装置B中溶液变浑浊,说明______ 。
③装置C中浓硫酸的作用是______ 。
④观察到装置D中黑色粉末变红色,反应的化学方程式是______ 。
【实验结论】猜想______ 正确。
【反思交流】如果将装置E去掉,______ (填“能”或“不能”)验证剩余固体中含有Fe,理由是______ 。


①图B中标有字母a的仪器名称是
②实验室用双氧水和二氧化锰制取氧气,该反应的化学方程式是
③装置F可以作为制取二氧化碳的发生装置,相比B装置其主要优点是
(2)纳米零价铁(单质铁)在环保领域应用广泛,以菱铁矿(主要成分为FeCO3不考虑杂质)为原料,制备纳米零价铁的反应为:
 。反应一段时间后,某学习小组对剩余固体的成分进行探究。
。反应一段时间后,某学习小组对剩余固体的成分进行探究。【提出问题】剩余固体的成分是什么?
【做出猜想】剩余固体的成分:
猜想一:Fe猜想二:FeCO3 猜想三:
【实验探究】该学习小组利用如图装置,对剩余固体成分进行探究,实验操作及现象如图。回答下列问题。

①向装置A中加入稀硫酸后,A中产生气泡且溶液变为浅绿色,小芳同学判断猜想一正确,小刚同学认为小芳的判断不合理,理由是:
②装置B中溶液变浑浊,说明
③装置C中浓硫酸的作用是
④观察到装置D中黑色粉末变红色,反应的化学方程式是
【实验结论】猜想
【反思交流】如果将装置E去掉,
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】为探究二氧化碳的过度排放对人类的影响。小组同学聚焦人类活动中排放二氧化碳的主要途径,基于“炼铁技术”,我们该如何践行“低碳行动”展开了项目式探究。
任务一:认识人类活动中二氧化碳的排放途径
【查阅资料】人类活动中二氧化碳的排放量占比。
【交流讨论】
(1)同学们通过资料进行了认真比较、分析,形成了报告,并写下了自己的认识:_______ 。
任务二:认识炼铁过程中二氧化碳的排放
【参观学习】钢铁是使用最多的金属材料。钢是含有少量碳及其他金属或非金属的铁。钢和生铁是含碳量不同的两种铁合金。生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。炼制钢铁的原理是利用一氧化碳和赤铁矿反应。在工业生产中,炼铁是一个复杂的过程,高炉炼铁是常见的炼铁方法,在实验室里,可以利用如图装置进行制备铁的实验。
(2)工业炼铁途径的主要原理是_______ (用化学方程式表示)。炼铁过程中依据______ 的现象能判断反应过程中排放出了二氧化碳。
任务三:寻找清洁、可持续发展的炼铁途径
【咨询专家】从我国国情出发,现阶段以焦炉煤气等富氢气体为主,未来以纯氢气作为还原剂直接还原铁的新技术具有广阔的前景,对减少炼铁过程中二氧化碳的排放量,实现钢铁行业的可持续发展有重要意义。
(3)【演示实验】
【反思评价】
(4)小组同学进一步检验了实验中产生的黑色固体,具体的方法是_______ 。
(5)小组同学从绿色化学角度设想,寻找到清洁、可持续发展的炼铁途径是_______ ,该炼铁途径的优点是_______ 。
任务四:从生活视角提出“低碳行动”的建议
【成果分享】
(6)通过以上分析,同学们知道在炼铁的同时会带来一系列的生活与环保问题。基于炼铁技术从生活视角提出建议,你还能提出一条有价值的建议是_______ 。
任务一:认识人类活动中二氧化碳的排放途径
【查阅资料】人类活动中二氧化碳的排放量占比。
| 人类活动 | 二氧化碳排放占比/% |
| 电力生产与储存(电力) | 27 |
| 取暖与制冷(供暖系统、冷却系统、制冷系统) | 7 |
| 交通运输(飞机、卡车、货船) | 16 |
| 生产和制造(钢、水泥、塑料) | 31 |
| 种植和养殖(植物和动物) | 19 |
(1)同学们通过资料进行了认真比较、分析,形成了报告,并写下了自己的认识:
任务二:认识炼铁过程中二氧化碳的排放
【参观学习】钢铁是使用最多的金属材料。钢是含有少量碳及其他金属或非金属的铁。钢和生铁是含碳量不同的两种铁合金。生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。炼制钢铁的原理是利用一氧化碳和赤铁矿反应。在工业生产中,炼铁是一个复杂的过程,高炉炼铁是常见的炼铁方法,在实验室里,可以利用如图装置进行制备铁的实验。

(2)工业炼铁途径的主要原理是
任务三:寻找清洁、可持续发展的炼铁途径
【咨询专家】从我国国情出发,现阶段以焦炉煤气等富氢气体为主,未来以纯氢气作为还原剂直接还原铁的新技术具有广阔的前景,对减少炼铁过程中二氧化碳的排放量,实现钢铁行业的可持续发展有重要意义。
(3)【演示实验】
| 实验操作 | 实验现象分析 | 解释 |
| 在试管中加入3颗锌粒,再加入3mL稀硫酸,将缠绕有氧化铁的玻璃棒在酒精灯火焰上灼烧至红热,再迅速伸入试管中
| 产生大量气泡,红色固体变为黑色 |
【反思评价】
(4)小组同学进一步检验了实验中产生的黑色固体,具体的方法是
(5)小组同学从绿色化学角度设想,寻找到清洁、可持续发展的炼铁途径是
任务四:从生活视角提出“低碳行动”的建议
【成果分享】
(6)通过以上分析,同学们知道在炼铁的同时会带来一系列的生活与环保问题。基于炼铁技术从生活视角提出建议,你还能提出一条有价值的建议是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】已知草酸(H2C2O4)加热时在催化剂的作用下会发生分解反应,某化学兴趣小组对其分解产物进行了如下探究。
【提出猜想】
a.分解产物是一氧化碳和水蒸气的混合物。
b.分解产物是二氧化碳和水蒸气的混合物。
c.分解产物是一氧化碳、二氧化碳和水蒸气的混合物。
【查阅资料】
ⅰ.白色的无水硫酸铜遇水会变为蓝色。
ⅱ.碱石灰是固体氢氧化钠和氧化钙的混合物,能吸收水蒸气和二氧化碳。
【进行实验】为了检验草酸的分解产物,该小组同学将草酸的分解产物通过如图所示的装置(部分夹持仪器已略去)。
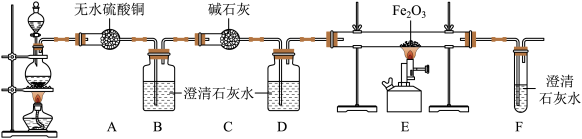
(1)装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊,证明草酸分解产生了______ 。
(2)装置D的作用是______ 。
(3)装置DEF中证明草酸分解产生了一氧化碳的现象分别为______ 。
(4)装置B中发生反应的化学方程式为______ 。
【得出结论】
(5)草酸分解的化学方程式为______ 。
【反思与评价】
(6)从环保角度考虑,上述实验的不足之处是______ 。
【数据与分析】兴趣小组同学将硬质玻璃管中Fe2O3换成铁红进行实验,铁红主要成分是Fe2O3,还含有少量的FeO、Fe3O4。
【铁的常见氧化物中铁的质量分数】:
小组同学称取铁红样品10.0 g,用上述装置进行实验,测定铁红中铁的质量分数。
(7)若E中充分反应后得到铁粉的质量为mg,则______ <m<______ 。
【提出猜想】
a.分解产物是一氧化碳和水蒸气的混合物。
b.分解产物是二氧化碳和水蒸气的混合物。
c.分解产物是一氧化碳、二氧化碳和水蒸气的混合物。
【查阅资料】
ⅰ.白色的无水硫酸铜遇水会变为蓝色。
ⅱ.碱石灰是固体氢氧化钠和氧化钙的混合物,能吸收水蒸气和二氧化碳。
【进行实验】为了检验草酸的分解产物,该小组同学将草酸的分解产物通过如图所示的装置(部分夹持仪器已略去)。

(1)装置A中无水硫酸铜变蓝,装置B中澄清石灰水变浑浊,证明草酸分解产生了
(2)装置D的作用是
(3)装置DEF中证明草酸分解产生了一氧化碳的现象分别为
(4)装置B中发生反应的化学方程式为
【得出结论】
(5)草酸分解的化学方程式为
【反思与评价】
(6)从环保角度考虑,上述实验的不足之处是
【数据与分析】兴趣小组同学将硬质玻璃管中Fe2O3换成铁红进行实验,铁红主要成分是Fe2O3,还含有少量的FeO、Fe3O4。
【铁的常见氧化物中铁的质量分数】:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
(7)若E中充分反应后得到铁粉的质量为mg,则
您最近一年使用:0次
科学探究题
|
适中
(0.65)
真题
解题方法
【推荐3】为了解甲酸的分解产物,实验小组进行了以下探究:
【查阅资料】甲酸(HCOOH)的熔点为8.6℃,能分解生成两种物质。
【提出猜想】实验小组对甲酸的分解产物提出了猜想:
猜想1.H2和CO2;猜想2.CO和H2O。
【设计实验】20℃时,甲酸的状态为______ ;从图一装置中选择合适的装置______ (填序号)对甲酸进行加热。为了加快分解速率,实验小组加入了催化剂,反应后将分解产物通入图二装置进行实验。

【实验预测】若猜想l成立,则D中的实验现象应为______ 。
【进行实验】实验中观察到C处瓶内出现大量水珠,F处玻璃管中出现的现象为______ ,甲酸分解的化学方程式为______ 。
【交流拓展】资料表明,不同条件下,甲酸的分解产物不同,猜想1和猜想2均能成立。据此小新对甲酸的分解产物又提出新猜想:猜想3.H2O和CO2;猜想4.CO和H2。经讨论认为无需进行实验就能确定猜想3和猜想4都错误,理由是______ 。
【查阅资料】甲酸(HCOOH)的熔点为8.6℃,能分解生成两种物质。
【提出猜想】实验小组对甲酸的分解产物提出了猜想:
猜想1.H2和CO2;猜想2.CO和H2O。
【设计实验】20℃时,甲酸的状态为

【实验预测】若猜想l成立,则D中的实验现象应为
【进行实验】实验中观察到C处瓶内出现大量水珠,F处玻璃管中出现的现象为
【交流拓展】资料表明,不同条件下,甲酸的分解产物不同,猜想1和猜想2均能成立。据此小新对甲酸的分解产物又提出新猜想:猜想3.H2O和CO2;猜想4.CO和H2。经讨论认为无需进行实验就能确定猜想3和猜想4都错误,理由是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】燃烧是人类最早利用的化学反应之一,燃烧与人类的生活以及社会的发展有着密切的联系。某校实践小组的同学们在老师的组织下,带着极大的兴趣以“探究燃烧的奥秘”为主题展开了如下项目化学习。
任务一:调查燃烧的价值
(1)同学们通过上网搜索、图书馆翻阅资料、社区调查、学习小组讨论等方式,调查发现社区 的家庭使用天然气(主要成分是
的家庭使用天然气(主要成分是 )做饭,
)做饭, 完全燃烧的化学方程式为
完全燃烧的化学方程式为______ 。
任务二:探究燃烧的条件
【设计实验】为探究燃烧的条件,小组同学在老师的指导下,在实验室设计并完成如下实验。
①白磷的着火点为 ,红磷的着火点为
,红磷的着火点为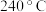 :
:
②磷燃烧产生的白烟会刺激人的呼吸道。
【实验分析】
(2)图甲中铜片上白磷燃烧的化学方程式______ ;烧杯中热水的作用一方面是提供热量,另一方面是______ 。
(3)通过对比图甲中______ (填序号)处的现象,可得出燃烧需要可燃物与氧气接触。
(4)通过图乙中a处的白磷燃烧,b处的红磷不燃烧,说明可燃物燃烧的条件之一是______ 。
【交流讨论】
(5)图乙中a处白磷燃烧后很快熄灭,原因可能是______(填字母)。
(6)实验小组又设计了如图所示的一组实验探究燃烧条件。下列说法中不正确的是______(填字母)。
任务三:调控运用燃烧
打铁花是一种传统的民间焰火表演艺术。其原理是将生铁烧至熔化成为铁水,再将铁水在空中用力击打而形成四处飞溅的耀眼“铁花”。
(7)烧铁水时,用鼓风机不断向燃着的焦炭中鼓入空气,其目的是______ 。
【拓展应用】
(8)对下列词语的有关化学原理解释不合理的是______(填字母)。
任务一:调查燃烧的价值
(1)同学们通过上网搜索、图书馆翻阅资料、社区调查、学习小组讨论等方式,调查发现社区
 的家庭使用天然气(主要成分是
的家庭使用天然气(主要成分是 )做饭,
)做饭, 完全燃烧的化学方程式为
完全燃烧的化学方程式为任务二:探究燃烧的条件
【设计实验】为探究燃烧的条件,小组同学在老师的指导下,在实验室设计并完成如下实验。

①白磷的着火点为
 ,红磷的着火点为
,红磷的着火点为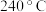 :
:②磷燃烧产生的白烟会刺激人的呼吸道。
【实验分析】
(2)图甲中铜片上白磷燃烧的化学方程式
(3)通过对比图甲中
(4)通过图乙中a处的白磷燃烧,b处的红磷不燃烧,说明可燃物燃烧的条件之一是
【交流讨论】
(5)图乙中a处白磷燃烧后很快熄灭,原因可能是______(填字母)。
| A.Y形管内的温度降低 | B.氧气耗尽 | C.白磷的着火点升高 |
(6)实验小组又设计了如图所示的一组实验探究燃烧条件。下列说法中不正确的是______(填字母)。
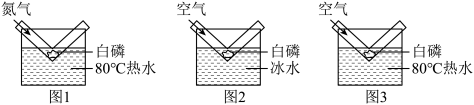
| A.图1白磷未燃烧是由于没有与氧气接触 |
| B.图2白磷未燃烧是由于温度没有达到着火点 |
| C.若将图3中白磷换成红磷,也能观察到燃烧现象 |
任务三:调控运用燃烧
打铁花是一种传统的民间焰火表演艺术。其原理是将生铁烧至熔化成为铁水,再将铁水在空中用力击打而形成四处飞溅的耀眼“铁花”。
(7)烧铁水时,用鼓风机不断向燃着的焦炭中鼓入空气,其目的是
【拓展应用】
(8)对下列词语的有关化学原理解释不合理的是______(填字母)。
| A.火上浇油—隔绝空气 | B.风助火威—为燃料燃烧提供充足的氧气 |
| C.釜底抽薪—燃烧需要可燃物 | D.钻木取火—使温度达到可燃物的着火点 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】化学在能源、环境、生命科学等方面发挥着其他学科所不能替代的作用,化学使世界变得更加绚丽多彩。
(1)氢气被称为最理想的燃料,理由是______ (写一条)。
(2)煤、石油、天然气被称为“三大”化石燃料。水煤气的主要成分是一氧化碳和氢气,可在高温条件下由碳与水蒸气反应制得,写出制取水煤气的化学方程式:______ 。
(3)可燃冰外观很像冰,主要含有甲烷水合物(由甲烷分子和水分子组成),可燃冰属于______ (填“可再生资源”或“不可再生资源”),甲烷完全燃烧的化学方程式为______ 。
(4)乙醇俗称酒精,可通过高粱、玉米等发酵、蒸馏而得,酒精是实验室常用的燃料之一,为进一步验证酒精的元素组成,同学们按下列步骤开展探究。
①点燃酒精,在酒精燃烧的火焰上罩一个干冷的烧杯,烧杯内壁出现水雾;迅速将烧杯倒转过来,并倒入澄清石灰水,观察到_______ 。
得出结论:酒精中含有碳元素和氢元素。
②进一步探究酒精中是否含有氧元素。
a.查阅资料:CO2能被NaOH溶液吸收;浓硫酸具有吸水性。
b.设计了下列实验,按照实验步骤进行探究。
步骤:
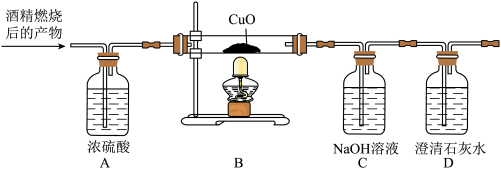
Ⅰ.按下列装置连接好仪器,从A装置先通入一会儿氮气,再点燃酒精灯;
Ⅱ.将n克酒精燃烧后的产物(不考虑酒精的挥发性)通入装置内;
Ⅲ.待充分反应后,再向装置内通入一会儿氮气。
反应前后分别称量装置A、C、D的质量,如下表所示(已知 ):
):
c.分析得出结论:探究过程中,装置D的作用是_____ 。酒精中碳、氢元素的质量比是_____ (用含m1、m2、m3、m4的代数式表示)。
d.评价:你认为该装置的设计是否合理,并说明理由:_______ 。
(1)氢气被称为最理想的燃料,理由是
(2)煤、石油、天然气被称为“三大”化石燃料。水煤气的主要成分是一氧化碳和氢气,可在高温条件下由碳与水蒸气反应制得,写出制取水煤气的化学方程式:
(3)可燃冰外观很像冰,主要含有甲烷水合物(由甲烷分子和水分子组成),可燃冰属于
(4)乙醇俗称酒精,可通过高粱、玉米等发酵、蒸馏而得,酒精是实验室常用的燃料之一,为进一步验证酒精的元素组成,同学们按下列步骤开展探究。
①点燃酒精,在酒精燃烧的火焰上罩一个干冷的烧杯,烧杯内壁出现水雾;迅速将烧杯倒转过来,并倒入澄清石灰水,观察到
得出结论:酒精中含有碳元素和氢元素。
②进一步探究酒精中是否含有氧元素。
a.查阅资料:CO2能被NaOH溶液吸收;浓硫酸具有吸水性。
b.设计了下列实验,按照实验步骤进行探究。
步骤:
Ⅰ.按下列装置连接好仪器,从A装置先通入一会儿氮气,再点燃酒精灯;
Ⅱ.将n克酒精燃烧后的产物(不考虑酒精的挥发性)通入装置内;
Ⅲ.待充分反应后,再向装置内通入一会儿氮气。
反应前后分别称量装置A、C、D的质量,如下表所示(已知
 ):
):| 装置名称 | 装置A | 装置C | 装置D |
| 步骤Ⅰ通氮气后质量(g) | m1 | m3 | m5 |
| 步骤Ⅲ通氮气后质量(g) | m2 | m4 | m6 |

c.分析得出结论:探究过程中,装置D的作用是
d.评价:你认为该装置的设计是否合理,并说明理由:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】李红同学通过调查得知,自己家庭厨房所用燃料是天然气。她对天然气主要成分甲烷燃烧后生成的气体成分产生了兴趣,进行了如下探究。
【提出问题】甲烷燃烧生成的气体成分都有哪些?
【查阅资料】
I.无水硫酸铜是白色固体,它遇到水变成蓝色。
Ⅱ.NaOH溶液能吸收CO2气体。
【猜想与假设】
(1)猜想1:CO2和H2O
猜想2:CO和H2O
猜想3:______ 。
【实验探究】李红同学设计下图所示装置进行探究(夹持装置未画出):
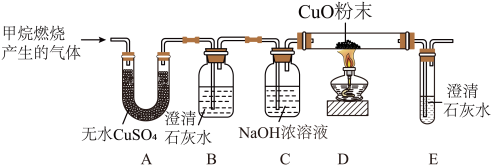
【现象与结论】
(2)观察到A装置中_______ 的现象,说明甲烷燃烧产生的气体中含有水蒸气。
(3)观察到B装置中的澄清石灰水变浑浊,证明甲烷燃烧有CO2气体生成,请写出B装置中反应的化学方程式:____________ 。
(4)观察到E中澄清石灰水变浑浊和D中____________ 现象,说明甲烷燃烧生成的气体中含有CO。
【交流与评价】
(5)A装置与B装置位置对换____________ (选填“会”或“不会”)对实验造成影响,C装置的作用是____________ 。
(6)李红认为实验装置的设计还有一处明显不足(实验前已排尽装置内的空气),请提出改进措施:____________ (任写一条)。
(7)通过上述实验得知甲烷燃烧不充分的后果是______________ 。
【提出问题】甲烷燃烧生成的气体成分都有哪些?
【查阅资料】
I.无水硫酸铜是白色固体,它遇到水变成蓝色。
Ⅱ.NaOH溶液能吸收CO2气体。
【猜想与假设】
(1)猜想1:CO2和H2O
猜想2:CO和H2O
猜想3:
【实验探究】李红同学设计下图所示装置进行探究(夹持装置未画出):

【现象与结论】
(2)观察到A装置中
(3)观察到B装置中的澄清石灰水变浑浊,证明甲烷燃烧有CO2气体生成,请写出B装置中反应的化学方程式:
(4)观察到E中澄清石灰水变浑浊和D中
【交流与评价】
(5)A装置与B装置位置对换
(6)李红认为实验装置的设计还有一处明显不足(实验前已排尽装置内的空气),请提出改进措施:
(7)通过上述实验得知甲烷燃烧不充分的后果是
您最近一年使用:0次