海水综合利用流程如下,有关说法错误的是
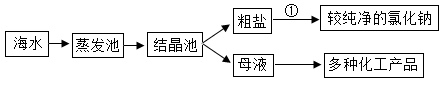

| A.从母液中可进一步制得金属镁 |
| B.①处操作是溶解、过滤、蒸发结晶 |
| C.海水“晒盐”得到的粗盐还含有杂质 |
| D.析出粗盐后的母液是氯化钠的不饱和溶液 |
2018·广西梧州·中考真题 查看更多[13]
广西梧州市2018年中考化学试题【校级联考】江苏省扬州市江都区四校联谊2019届九年级下学期中考二模化学试题鲁教版九年级下册第八单元第二节 海水“晒盐”2019年江苏省扬州市广陵区树人学校中考二模化学试题(已下线)课题11.1 生活中常见的盐 第1课时(练)-2019-2020学年九年级化学下册同步精品课堂(人教版)(已下线)8.2.2 粗盐的提纯-2020-2021学年九年级化学下册课时同步练(鲁科版)(已下线)第3节 几种重要的盐(第2课时)(练)-九年级化学下册同步精品课堂(沪教全国版)山东省泰安市岱岳区2020-2021学年九年级上学期期末化学试题(已下线)第十一单元 盐 化肥单元测试卷(A卷基础篇)-2020-2021学年九年级化学下册同步单元AB卷(人教版)山东省淄博沂源县2020-2021学年九年级上学期期末化学试题(已下线)第八单元到实验室去:粗盐中难溶性杂质的去除-2021-2022学年九年级化学鲁教版下册山东省泰安市岱岳区道朗镇第一中学2022-2023学年九年级上学期期末化学试题山东省泰安市东平县实验中学2022-2023学年九年级上学期期末化学试题
更新时间:2018-08-04 07:32:37
|
相似题推荐
【推荐1】为除去粗盐中的泥沙、CaCl2、MgCl2、Na2SO4得到 NaCl,可将粗盐溶解于水,然后依次进行下列操作:①加过量 NaOH 溶液、②加过量 BaCl2溶液、③加过量Na2CO3溶液、④过滤、⑤加适量稀盐酸、⑥蒸发,即可得纯净的氯化钠晶体。下列有关说法不正确的是
| A.若将步骤①和②交换顺序,不影响最终所得晶体的纯度 |
| B.若将步骤②和③交换顺序,不影响最终所得晶体的纯度 |
| C.若将第①②步删去,改为加过量 Ba(OH)2溶液,不影响最终所得晶体纯度 |
| D.第⑤步中若稀盐酸过量,不影响最终所得晶体的纯度 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
名校
【推荐2】氯化钠溶液中含有杂质CaCl2和Na2SO4依次通过以下操作将其除去:①加入过量的氯化钡溶液:②加入过量的碳酸钠溶液;③过滤;④加入适量的盐酸至溶液呈中性。则关于该过程的说法正确的是
| A.操作①和②的顺序可以颠倒 |
| B.操作②只除去了Ca2+ |
| C.操作③和④的顺序可以颠倒 |
| D.操作④只除去了CO32- |
您最近一年使用:0次
选择题-选择题组
|
较难
(0.4)
解题方法
【推荐1】阅读下列资料,完成下面小题。
海洋是地球上最大的储水库,其储水量约占全球总储水量的 96.5%。海水中蕴藏着丰富的化学资源,人类正运用各种方法,对海水进行科学的开发和综合利用。工业流程如下图所示:
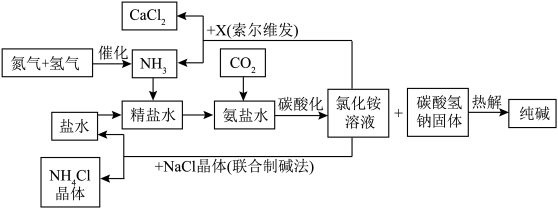
1.下列有关海水资源开发和利用的描述中,正确的是
2.侯德榜发明了制碱与制氨结合的联合制碱法,为纯碱和氮肥工业技术发展作出了杰出的贡献。 下列叙述不正确的是
3.“侯氏制碱法”生产纯碱的主要反应是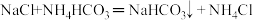 。如图是三种物质的溶解度曲线。下列选项的叙述正确的是
。如图是三种物质的溶解度曲线。下列选项的叙述正确的是

海洋是地球上最大的储水库,其储水量约占全球总储水量的 96.5%。海水中蕴藏着丰富的化学资源,人类正运用各种方法,对海水进行科学的开发和综合利用。工业流程如下图所示:

1.下列有关海水资源开发和利用的描述中,正确的是
| A.海水淡化:蒸馏法淡化海水是利用海水中各组分的颗粒大小不同 |
| B.海水晒盐:蒸发结晶池得到粗盐,剩余的母液为氯化钠的饱和溶液 |
| C.粗盐提纯:除去粗盐中泥沙等难溶性杂质,先将固体溶解再蒸发结晶 |
| D.粗盐精制:除去粗盐中可溶性杂质 Na2SO4,可选用足量 Ba(NO3)2溶液 |
| A.合成氨原料中 N2、H2中常含有 CO2和水蒸气,反应前要净化。在实验室可采用先通足量氢氧化钠溶液,再通过足量浓硫酸 |
| B.氨碱工业中,为增大二氧化碳在氨碱水中的溶解度,可减小压强 |
| C.“索尔维法”中将氯化铵溶液与 X 混合产生大量废弃物 CaCl2,X 为 Ca(OH)2 |
| D.联合制碱法中实现了 NaCl 的回收再利用,大大提高了产率 |
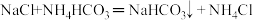 。如图是三种物质的溶解度曲线。下列选项的叙述正确的是
。如图是三种物质的溶解度曲线。下列选项的叙述正确的是 
| A.NaCl 中混有少量 NH4Cl,可用降温结晶提纯 NaCl |
| B.60℃,NH4Cl 的溶液的溶质质量分数一定大于 NaHCO3溶液的溶质质量分数 |
| C.析出 NaHCO3晶体的原因可能是同温下 NaHCO3的溶解度远小于 NH4Cl |
| D.20℃时,100g 水中加入 5.85g NaCl 和 7.9g NH4HCO3固体,肯定有 NaHCO3晶体析出 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
名校
【推荐2】氨碱法生成纯碱的主要反应原理如下:①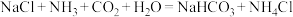 ②
②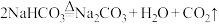 ,对上述信息的有关理解不正确的是
,对上述信息的有关理解不正确的是
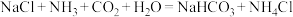 ②
②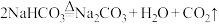 ,对上述信息的有关理解不正确的是
,对上述信息的有关理解不正确的是| A.二氧化碳的作用是提供碳、氧元素 |
| B.①中析出碳酸氢钠晶体后剩余溶液只有一种溶质 |
| C.氨盐水比食盐水更易吸收二氧化碳,是因为氨盐水呈碱性 |
| D.反应①中生成碳酸氢钠而不是碳酸钠,是因为室温下,碳酸氢钠更易达到饱和而结晶析出 |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
名校
解题方法
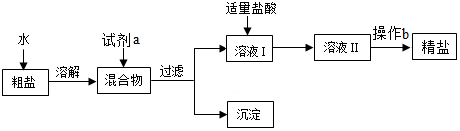
【推荐1】从天然盐井中获取粗盐(含泥沙、CaCl2、MgCl2、Na2SO4等杂质)为了除去以上杂质得到精盐,小明设计如下实验:
【提示】杂质含量较少,不考虑微溶物形成沉淀

下列有关实验的说法正确的是
①蒸发操作中用到的玻璃仪器有酒精灯、玻璃棒和蒸发皿
②沉淀b是BaSO4
③物质X是Na2SO4
④取滤液b少许滴入适量Na2SO4溶液,即可证明Ba(OH)2溶液过量
⑤滤液C中加入稀盐酸后有中和反应发生
⑥理论上得到精盐的质量与粗盐中氯化钠的质量不相等
【提示】杂质含量较少,不考虑微溶物形成沉淀

下列有关实验的说法正确的是
①蒸发操作中用到的玻璃仪器有酒精灯、玻璃棒和蒸发皿
②沉淀b是BaSO4
③物质X是Na2SO4
④取滤液b少许滴入适量Na2SO4溶液,即可证明Ba(OH)2溶液过量
⑤滤液C中加入稀盐酸后有中和反应发生
⑥理论上得到精盐的质量与粗盐中氯化钠的质量不相等
| A.①②③ | B.④⑤⑥ | C.①④ | D.⑤⑥ |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
【推荐2】下列依据实验目的所设计的实验过程,不合理的是

| 选项 | 实验目的 | 实验设计 |
| A | 鉴别硝酸钾溶液和碳酸钾溶液 | 取样滴加稀盐酸,观察是否产生气泡 |
| B | 鉴别合成纤维和羊毛纤维 | 取样品灼烧 |
| C | 除去一氧化碳中少量二氧化碳气体 | 将气体通过灼热的氧化铜粉末 |
| D | 除去氯化钠固体中混有的泥沙 | 溶解、过滤、蒸发 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
解题方法
【推荐1】下列实验方案正确的是
| 选项 | 实验内容 | 操作方法 |
| A | 分离木炭粉和氧化铜 | 在空气中灼烧至固体质量不再变化 |
| B | 除去食盐水中混有的Ca2+、Mg2+、 | 依次加入过量的BaC12溶液、NaOH溶液、Na2CO3溶液,过滤,向滤液中滴加盐酸至中性 |
| C | 鉴别氯化钡、碳酸钾、硫酸钠、氢氧化钙四种溶液 | 将四种溶液两两混合就能鉴别 |
| D | 除去氧化钙中混有的碳酸钙 | 先加入足量的水溶解,然后过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
选择题-单选题
|
较难
(0.4)
解题方法
【推荐2】我省叶县是中国岩盐之都,岩盐中除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,要除去杂质得到精盐,设计了如下实验方案。有关该方案说法错误的是


| A.操作①⑤⑦均用到了玻璃棒,但玻璃棒的作用不一样 |
| B.过滤所得的固体中含有泥沙和反应生成的四种沉淀物 |
| C.第②③④步依次加入的试剂为NaOH、Na2CO3、BaCl2 |
| D.调节pH=7时必须使用稀盐酸,不能使用其它酸类物质 |
您最近一年使用:0次