海水是巨大的资源宝库,如图所示利用海水为原料可获得许多化工产品:
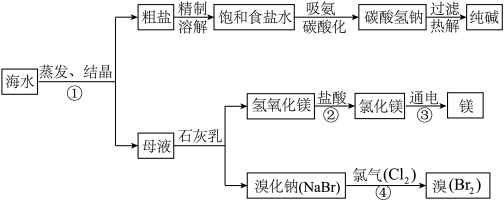
(1)获得的化工产品中属于非金属单质的是________ (填化学式)
(2)要区分海水和蒸馏水,可选用的化学试剂是________ (填化学式)
(3)步骤①中选用蒸发结晶法而不用降温结晶法的理由是________
(4)步骤②发生反应的化学方程式是________ ,其基本反应类型为________ ,用镁制造的一种镁铝合金常用作生产飞机外壳的材料,该材料具有的优良性能有________ (任答一点)

(1)获得的化工产品中属于非金属单质的是
(2)要区分海水和蒸馏水,可选用的化学试剂是
(3)步骤①中选用蒸发结晶法而不用降温结晶法的理由是
(4)步骤②发生反应的化学方程式是
更新时间:2018-08-25 20:53:19
|
相似题推荐
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】构建知识网络是一种重要的学习方法。如图A、B、C、D是初中化学常见的氧化物、酸、碱、盐四种不同类别的物质与CO2的知识网络图,其中D、E是氧化物,D为红棕色固体;B为钠盐;E与D的反应用于工业炼铁;A与B反应可制取烧碱。图中“一”表示反应关系,“→”表示转化关系,请回答下列问题:
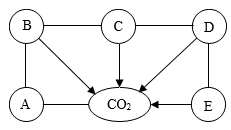
(1)A属于上述五种类别中的______ 。
(2)D和E反应的化学方程式为______ ;C制取CO2的化学方程式为______ 。
(3)A与B反应所属基本反应类型是______ 。

(1)A属于上述五种类别中的
(2)D和E反应的化学方程式为
(3)A与B反应所属基本反应类型是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下图表示硫元素的常见化合价与含硫物质类别的关系。
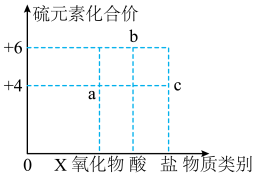
(1)X 的物质类别是______ , b的化学式为______ 。
(2)a与氢氧化钠溶液反应能生成c,对应的化学方程式为______ ,该反应______ (填“属于”或“不属于”)复分解反应。

(1)X 的物质类别是
(2)a与氢氧化钠溶液反应能生成c,对应的化学方程式为
您最近一年使用:0次
【推荐3】海水“制碱”体现了人类利用和改造自然的智慧。工业上以粗盐(含少量Ca2+、Mg2+、 等杂质离子)制取纯碱的流程如下:
等杂质离子)制取纯碱的流程如下:

(1)海水“晒盐”是通过______ (“蒸发结晶”或“降温结晶”)的方法获取粗盐。
(2)工业上用下列药品除去粗盐水杂质离子,请写出一组合理的添加顺序:______ (填序号)。
①Na2CO3 ②BaCl2 ③NaOH
(3)“除杂”最后应加入适量盐酸,其目的是除去溶液中的______ (填离子符号)。
(4)步骤Ⅲ先向饱和食盐水中通入氨气得到饱和氨盐水,饱和氨盐水的pH值______ (填“>”"=”或“<”)。写出步骤Ⅲ反应的化学方程式______ 。
(5)若在实验室提纯粗盐,溶解3g粗盐《室温下NaCl的溶解度约为36g),最好用量筒量取______ (填“5”、“10”或“50”)mL水。蒸发滤液时要用到的仪器有铁架台(带铁圈)、酒精灯、玻璃棒和______ 。
 等杂质离子)制取纯碱的流程如下:
等杂质离子)制取纯碱的流程如下:
(1)海水“晒盐”是通过
(2)工业上用下列药品除去粗盐水杂质离子,请写出一组合理的添加顺序:
①Na2CO3 ②BaCl2 ③NaOH
(3)“除杂”最后应加入适量盐酸,其目的是除去溶液中的
(4)步骤Ⅲ先向饱和食盐水中通入氨气得到饱和氨盐水,饱和氨盐水的pH值
(5)若在实验室提纯粗盐,溶解3g粗盐《室温下NaCl的溶解度约为36g),最好用量筒量取
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】现有以下几种物质:A.空气 B.氧气 C.蒸馏水 D.二氧化碳 E.高锰酸钾 F.铁粉 G.氮气 H.四氧化三铁。其中属于混合物的有(填字母代号,下同)_______ ,化合物的有______ , 氧化物的有_____ ,单质的有______ 。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】我们生活在一个丰富多彩的物质世界中,人类的生活和化学密不可分。
(1)用适当的化学符号填空。
①最轻的气体_______ ; ②3个亚铁离子______ ;
③空气中最多的元素_______ ; ④氧化铝中铝元素的化合价_____ 。
(2)正确的分类是学习化学的一种重要方法,请你按要求填空:

①如澄清石灰水,其有效成分为氢氧化钙,写出其阴离子的符号______ ,它与CO2反应方程式是 ______________________ 。
②处的物质类别是_____ 。如氧气,保持氧气化学性质的最小粒子是_____ 。(填名称)
③如水(H2O),请写出电解水的化学方程式:____________ ;该反应的基本类型是 ____________ 。
(1)用适当的化学符号填空。
①最轻的气体
③空气中最多的元素
(2)正确的分类是学习化学的一种重要方法,请你按要求填空:

①如澄清石灰水,其有效成分为氢氧化钙,写出其阴离子的符号
②处的物质类别是
③如水(H2O),请写出电解水的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】氢能源是理想能源,氢能源开发一直是前沿科学研究的课题之一。科学家研发出一种以铝镓合金(镓:Ga)和水为原料制取氢气的新工艺,流程如图1所示。回答下列问题:
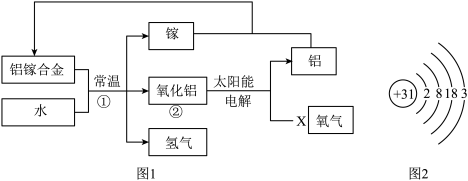
(1)从物质分类的角度看,铝镓合金属于________ (选填“混合物”或“纯净物”),用该合金与铝片相互刻划发现铝片上有划痕,说明________
(2)如图1所示,物质X是一种单质,X的化学式是_____________ 。反应①中镓的作用是________ ,该反应的化学方程式是___________ ,它属于四种基本反应类型中的__________ 。
(3)与电解水制取氢气相比,用铝镓合金和水为原料制取氢气的优点是(答出一点即可)________ 。
(4)镓的原子结构示意图如图2所示,写出镓与氧气在加热时反应的化学方程式_______ 。

(1)从物质分类的角度看,铝镓合金属于
(2)如图1所示,物质X是一种单质,X的化学式是
(3)与电解水制取氢气相比,用铝镓合金和水为原料制取氢气的优点是(答出一点即可)
(4)镓的原子结构示意图如图2所示,写出镓与氧气在加热时反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】西汉海昏侯墓出土的青铜雁鱼灯造型优美,设计精妙,整体作鸿雁回首衔鱼伫立状,其示意图如图所示。_______ (写一个)。
(2)雁鱼灯出土时表面某些部分存在绿色锈迹,其主要成分为铜绿[Cu2(OH)2CO3],生成铜绿是铜与空气中的氧气、水蒸气和_______ 共同作用的结果。Cu2(OH)2CO3中铜、氧元素的原子个数比为_______ 。
(3)雁鱼灯上用漆彩绘出雁的翎毛、鳞片,施以黑、白、红、绿四色。彩绘经久不变色,说明彩绘颜料的化学性质_______ (填“活泼”或“不活泼”)。
(4)将雁鱼灯的灯罩左右转动开合是为了挡风并调节_______ 。
(5)雁鱼灯“腹部”盛放清水的目的是_______ 。

(2)雁鱼灯出土时表面某些部分存在绿色锈迹,其主要成分为铜绿[Cu2(OH)2CO3],生成铜绿是铜与空气中的氧气、水蒸气和
(3)雁鱼灯上用漆彩绘出雁的翎毛、鳞片,施以黑、白、红、绿四色。彩绘经久不变色,说明彩绘颜料的化学性质
(4)将雁鱼灯的灯罩左右转动开合是为了挡风并调节
(5)雁鱼灯“腹部”盛放清水的目的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】铁、镁、铝、铜是生活中最常见的金属。
(1)铜质电缆是利用了铜的______ 性;镁铝合金与铝相比其优点是______ 。
(2)为验证铁、镁、铝、铜的金属活动性顺序,将相同表面积的铁、镁、铝、铜片打磨后放入相同的稀盐酸中。写出反应前后溶液颜色有变化的化学反应方程式______ 。
(3)有同学设计了如下新的实验方案验证这四种金属的活动性顺序,其中不能达到实验目的的是______(填序号)。
(1)铜质电缆是利用了铜的
(2)为验证铁、镁、铝、铜的金属活动性顺序,将相同表面积的铁、镁、铝、铜片打磨后放入相同的稀盐酸中。写出反应前后溶液颜色有变化的化学反应方程式
(3)有同学设计了如下新的实验方案验证这四种金属的活动性顺序,其中不能达到实验目的的是______(填序号)。
| A.镁、铝、硫酸铜溶液、硫酸亚铁溶液 | B.铁、镁、硫酸铝溶液、硫酸铜溶液 |
| C.铝、铜、硫酸镁溶液、硫酸亚铁溶液 | D.铁、铝、硫酸镁溶液、硫酸铜溶液 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】下表是KNO3和Ca(OH)2在不同温度时的溶解度:
(1)硝酸钾中含有少量氨氧化钙时,可采用______ (填"降温结晶”或"恒温蒸发溶剂")的方法提纯硝酸钾。
(2)60 ℃时,进行下图操作:
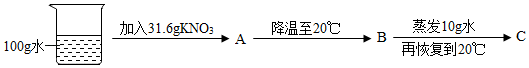
B中的溶液是______ (填"饱和"成“不饱和")溶液。C中析出固体的质量为______ g。
(3)如图是同学们配制100 g溶质质量分数为12%的KNO3溶液的实验操作示意图,正确的操作顺序是______ (填序号)。

| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度 | KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |
| Ca(OH)2 | 0.19 | 0.17 | 0.16 | 0.14 | 0.13 | 0.11 | |
(2)60 ℃时,进行下图操作:

B中的溶液是
(3)如图是同学们配制100 g溶质质量分数为12%的KNO3溶液的实验操作示意图,正确的操作顺序是

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】下图是A、B、C三种固体物质的溶解度曲线。
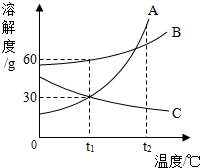
(1)t1℃时,三种物质溶解度由大到小的关系是_______ ;
(2)t2℃时,将30gB固体投入100g水中,充分溶解后可得到的是________ 溶液(填“不饱和”、“饱和”或“不能确定”)。
(3)将饱和C溶液变为不饱和溶液,可行的方法之一是加溶剂水,还可以用的方法是____ 。
(4)从B的溶液中得到B晶体,可采用______ 的方法。

(1)t1℃时,三种物质溶解度由大到小的关系是
(2)t2℃时,将30gB固体投入100g水中,充分溶解后可得到的是
(3)将饱和C溶液变为不饱和溶液,可行的方法之一是加溶剂水,还可以用的方法是
(4)从B的溶液中得到B晶体,可采用
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】过氧化钙(CaO2),在常温下稳定,在潮湿空气及水中缓慢反应放出氧气,因而在水产养殖中常用作供氧剂。CaO2·8H2O是一种白色固体,难溶于水、乙醇,在0℃时稳定,加热至130℃时逐渐变为无水CaO2,实验室可用氯化钙制取CaO2·8H2O,再经脱水制得CaO2,其制备流程如图所示:

【查阅资料】1、乙醇与水任意比互溶;
2、乙醇与CaO2不发生化学反应;
3.反应2化学方程式为:CaCl2+H2O2+2NH3·H2O+6H2O=CaO2·8H2O↓+2NH4Cl。
请回答下列问题:
(1)反应2和操作a都要在低温下进行,其主要原因是______ 。
(2)进行操作a时玻璃棒的作用是______ ;操作b的名称是______ 。
(3)用“水洗”的目是______ ,“乙醇洗涤”的目的是______ 。
(4)该流程得到的副产品是______ 。
(5)过氧化钙在水产养殖中供氧时还会生成氢氧化钙,该反应的化学方程式为______ 。
(6)过氧化钙中常含有杂质CaO,在过氧化钙样品中,钙元素的质量分数会随CaO含量的增加而______ (填“增大”、“减小”或“不变”),为测定某过氧化钙样品的纯度,称取2.0g样品,充分加热使之完全分解(杂质不参与反应),生成CaO和O2,得到O2的质量0.32g,则该样品中过氧化钙的质量分数为______ 。

【查阅资料】1、乙醇与水任意比互溶;
2、乙醇与CaO2不发生化学反应;
3.反应2化学方程式为:CaCl2+H2O2+2NH3·H2O+6H2O=CaO2·8H2O↓+2NH4Cl。
请回答下列问题:
(1)反应2和操作a都要在低温下进行,其主要原因是
(2)进行操作a时玻璃棒的作用是
(3)用“水洗”的目是
(4)该流程得到的副产品是
(5)过氧化钙在水产养殖中供氧时还会生成氢氧化钙,该反应的化学方程式为
(6)过氧化钙中常含有杂质CaO,在过氧化钙样品中,钙元素的质量分数会随CaO含量的增加而
您最近一年使用:0次



