某化学兴趣小组在实验室做“金属与酸反应”的实验,将两根铝丝分别插入稀盐酸和稀硫酸中发现产生气泡的速率不同,于是进行了下列研究:
〖提出问题〗影响铝和酸反应的速率的因素有哪些?
〖猜想与假设〗猜想一:酸的浓度 猜想二:_______ 猜想三: _______ 猜想四:金属的颗粒大小
〖验证实验〗
(1)为了验证猜想一是否正确,小明同学惊醒了如下实验:
①写出铝与盐酸反应的化学反应方程式_________
②反应前打磨铝丝的原因________________
(2)为了验证猜想四是否正确,小阳同学进行了如下实验:
〖反思与评价〗小铭将铝丝与一定量稀盐酸混合在一密闭容器内反应,利用压强和温度传感器测出了反应过程中压强和温度随时间变化的关系(如下图所示)
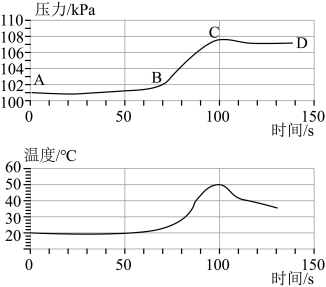
(1)由图可知:_________ 点(填字母)时铝与盐酸反应结束
(2)分别解释压强曲线AB段、BC段、CD段变化的原因
①_______________________
②__________________________
③__________________________
〖提出问题〗影响铝和酸反应的速率的因素有哪些?
〖猜想与假设〗猜想一:酸的浓度 猜想二:
〖验证实验〗
(1)为了验证猜想一是否正确,小明同学惊醒了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 将打磨后质量相同、粗细一致 的两根铝丝、分别加入两支试管中,再分别倾倒体积相同、浓度不同的稀盐酸 | 酸的浓度越大,反应速率越快 |
①写出铝与盐酸反应的化学反应方程式
②反应前打磨铝丝的原因
(2)为了验证猜想四是否正确,小阳同学进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 将打磨后质量相同、粗细不同的两根铝丝、分别放入两支试管中,再分别倾倒体积和浓度均相同的稀盐酸 | 放入细铝丝的试管产生的气泡更快 |

(1)由图可知:
(2)分别解释压强曲线AB段、BC段、CD段变化的原因
①
②
③
更新时间:2018-12-30 16:38:51
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】为测定空气中氧气的含量,小华同学进行操作如实验1:选用实际容积为50mL的硬质玻璃管作反应容器,将过量的铜粉放入试管,用橡皮塞塞紧硬质玻璃管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置。请回答下列问题:______ 。
(2)选择铜作为反应物的原因是______ 。
(3)实验过程中,硬质玻璃管内的实验现象为______ ,该反应的化学方程式是______ 。
(4)①根据表中提供的数据,完成下列内容。
②上述测定结果偏______ (填“高”或“低”)。
③出现误差的原因可能是______ (填序号)。
A.加热时不断推拉注射器活塞 B.读数时冷却至室温
C.加入铜粉量太少 D.加入铜粉量太多
(5)小明同学设计出如实验2所示的实验装置,实验时在粗铜丝末端的燃烧匙中放足量白磷。如图为用气体压力传感器测得的广口瓶中气压变化情况。______ 。
②图像中CD段气压变化的原因是______ 。
③DE段压强突然增大的实验操作是______ 。
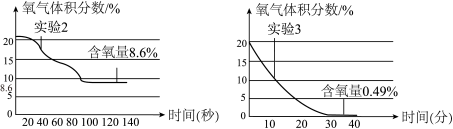
(6)实验3:在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀会消耗空气中的氧气原理测定空气中氧气的体积分数。用数字传感器测实验2、实验3中氧气的体积分数随时间变化的关系如图所示。______ 的测定方法更准确,判断依据是______ 。

(2)选择铜作为反应物的原因是
(3)实验过程中,硬质玻璃管内的实验现象为
(4)①根据表中提供的数据,完成下列内容。
| 硬质玻璃管的容积/mL | 反应前注射器中气体体积/mL | 反应后注射器中气体体积/mL | 实验测得空气中氧气的体积分数/% |
| 50 | 30 | 18 |
③出现误差的原因可能是
A.加热时不断推拉注射器活塞 B.读数时冷却至室温
C.加入铜粉量太少 D.加入铜粉量太多
(5)小明同学设计出如实验2所示的实验装置,实验时在粗铜丝末端的燃烧匙中放足量白磷。如图为用气体压力传感器测得的广口瓶中气压变化情况。

②图像中CD段气压变化的原因是
③DE段压强突然增大的实验操作是
(6)实验3:在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用铁锈蚀会消耗空气中的氧气原理测定空气中氧气的体积分数。用数字传感器测实验2、实验3中氧气的体积分数随时间变化的关系如图所示。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】化学兴趣小组同学做了关于物质燃烧的两组实验。
实验一:甲组同学探究燃烧条件
提供物品:①酒精灯、②铜片、③火柴头、④火柴梗、⑤沙土、⑥三脚架
【实验探究】
【解释与结论】
(1)探究1得出物质燃烧的条件之一为______ 。
(2)探究2说明火柴头的着火点比火柴梗的着火点______ (填“高”或“低”)。
【拓展与应用】
户外野炊时,为使木柴燃烧得更旺,往往将木柴架空,这是为了______ 。
实验二:乙组同学采用如图所示的装置测定空气中氧气含量。
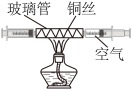
实验操作步骤:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化。
(1)铜丝在加热过程中的颜色变化是______ 。
(2)实验过程中,玻璃管内发生反应的化学方程式为______ ,该反应属于______ (填基本反应类型)。
(3)乙组同学测得实验结果如下:
由此数据可以推算出乙组同学测定的空气中氧气的体积分数______ (填“大于”、“小于”或“等于”)21%,造成该实验出现误差的原因可能是______ (填序号)。
①交替缓缓推动两个注射器活塞次数较少
②未冷却至室温就读数
③加入铜丝量太多
实验一:甲组同学探究燃烧条件
提供物品:①酒精灯、②铜片、③火柴头、④火柴梗、⑤沙土、⑥三脚架
【实验探究】
| 探究内容 | 实验设计与操作 | 实验现象 |
| 探究1:燃烧与物质的关系 |  | 火柴头燃烧,沙土不燃烧 |
| 探究2:燃烧与温度的关系 |  | 火柴头先燃烧,火柴梗后燃烧 |
(1)探究1得出物质燃烧的条件之一为
(2)探究2说明火柴头的着火点比火柴梗的着火点
【拓展与应用】
户外野炊时,为使木柴燃烧得更旺,往往将木柴架空,这是为了
实验二:乙组同学采用如图所示的装置测定空气中氧气含量。

实验操作步骤:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化。
(1)铜丝在加热过程中的颜色变化是
(2)实验过程中,玻璃管内发生反应的化学方程式为
(3)乙组同学测得实验结果如下:
| 反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
| 25 mL | 21 mL |
①交替缓缓推动两个注射器活塞次数较少
②未冷却至室温就读数
③加入铜丝量太多
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组设计如下实验探究FeCl3溶液的相关性质。
相关信息:Fe和Fe3O4,易被磁铁吸引,FeO是一种黑色固体,不能被磁铁吸引;Fe3O4能与盐酸反应,生成盐和水。FeCl3具有氧化性,与单质铁等物质化合时铁元素化合价会降低。
(1)实验一:将饱和FeCl3溶液在蒸发皿中加热至沸腾后,发现逐渐产生红褐色沉淀,加热时,FeCl3,易与水反应生成红褐色固体物质和盐酸,红色固体的化学式是_______________ 。
(2)实验二:将实验一蒸发获得的红色固体灼烧,颜色由红色变为红棕色。该反应的化学方程式是__________ 。
①氢氧化镁,氢氧化铜等物质加热也能分解得到对应的金属氧化物,而氢氧化钠、氢氧化钙等物质则无此性质。结合实验,从物质类别及其溶解性推断,通过加热分解___________ 可生成对应的金属氧化物。
②将氢氧化镁和铜粉混合物充分加热,得到的固体物质与原混合物质量相同,请问,氢氧化镁和铜粉的质量比为________ 。
(3)实验三:小组同学用多根玻璃棒蘸取饱和FeCl3溶液于酒精灯火焰上灼烧,在1分钟内观察到玻璃棒表面颜色的变化依次为:黄色、红褐色、红棕色,黑色。
①同学们对黑色物质的成分产生了疑问。联系酒精的可燃性、还原性等相关性质,对黑色物质的成分提出了猜想,经讨论,可能是_______ 和Fe3O4四种物质中的一种或几种。
②为了确定黑色物质的成分,收集黑色物质,进行了如下实验:
相关信息:Fe和Fe3O4,易被磁铁吸引,FeO是一种黑色固体,不能被磁铁吸引;Fe3O4能与盐酸反应,生成盐和水。FeCl3具有氧化性,与单质铁等物质化合时铁元素化合价会降低。
(1)实验一:将饱和FeCl3溶液在蒸发皿中加热至沸腾后,发现逐渐产生红褐色沉淀,加热时,FeCl3,易与水反应生成红褐色固体物质和盐酸,红色固体的化学式是
(2)实验二:将实验一蒸发获得的红色固体灼烧,颜色由红色变为红棕色。该反应的化学方程式是
①氢氧化镁,氢氧化铜等物质加热也能分解得到对应的金属氧化物,而氢氧化钠、氢氧化钙等物质则无此性质。结合实验,从物质类别及其溶解性推断,通过加热分解
②将氢氧化镁和铜粉混合物充分加热,得到的固体物质与原混合物质量相同,请问,氢氧化镁和铜粉的质量比为
(3)实验三:小组同学用多根玻璃棒蘸取饱和FeCl3溶液于酒精灯火焰上灼烧,在1分钟内观察到玻璃棒表面颜色的变化依次为:黄色、红褐色、红棕色,黑色。
①同学们对黑色物质的成分产生了疑问。联系酒精的可燃性、还原性等相关性质,对黑色物质的成分提出了猜想,经讨论,可能是
②为了确定黑色物质的成分,收集黑色物质,进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取黑色粉末用磁铁吸引,观察现象 | 黑色粉末全部被磁铁吸引 | 综合实验现象判断,此黑色物质成分是 |
| 向装有黑色粉末的试管中加入足量的盐酸,充分反应,观察现象 | 固体逐渐溶解,但无气泡产生 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】张景同学拿来一片黄色的金属向同学们炫耀,说他捡到一块黄金。刘静说这块黄色的金属不一定是黄金,于是他们一起进行探究;
提出问题:这块黄色的金属是黄金还是铜锌合金。
资料查阅:金在高温下不与氧气反应,锌在高温下与氧气反应生成白色固体。
进行猜想:①张景认为是黄金 ②刘静认为是铜锌合金
设计实验:①张景设计的实验是:取一小片黄色的金属放在石棉网上用酒精灯加热
②刘静设计的实验是:取一小片黄色的金属放入硝酸银溶液中。
现象与结论:
(1)张景在实验中观察到黄色金属变黑,则他的猜想______ (填“正确”或“不正确”),你认为该黑色的物质是______ (填化学式)。
(2)刘静在实验中能观察到的现象是______ 。
反思与应用:
(3)假如你的观点与刘静相同,你还可以设计的一个实验是______ ,
(4)你设计实验中能观察到的现象是______
提出问题:这块黄色的金属是黄金还是铜锌合金。
资料查阅:金在高温下不与氧气反应,锌在高温下与氧气反应生成白色固体。
进行猜想:①张景认为是黄金 ②刘静认为是铜锌合金
设计实验:①张景设计的实验是:取一小片黄色的金属放在石棉网上用酒精灯加热
②刘静设计的实验是:取一小片黄色的金属放入硝酸银溶液中。
现象与结论:
(1)张景在实验中观察到黄色金属变黑,则他的猜想
(2)刘静在实验中能观察到的现象是
反思与应用:
(3)假如你的观点与刘静相同,你还可以设计的一个实验是
(4)你设计实验中能观察到的现象是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】【问题情景】化学老师说不能用金属与浓硫酸反应来制取氢气,可是某实验小组的同学在一次实验中将锌粒加入到浓硫酸中发现有大量的气泡放出,他们对气体的成分进行了探究。
【提出猜想】从物质组成元素的角度来看,放出的气体可能是 、
、 、
、 。
。
【查阅资料】 有刺激性气味,易溶于水,能使品红(一种有机色素,呈红色)溶液褪色,能与
有刺激性气味,易溶于水,能使品红(一种有机色素,呈红色)溶液褪色,能与 反应生成
反应生成 。
。
【方案设计】实验小组的同学设计了如下一些方案。
(1)甲同学认为是 ,其检验方法是
,其检验方法是______ 。
(2)乙同学认为是 ,则检验方法是
,则检验方法是______ 。
(3)丙同学认为是 ,则可将气体通过盛有灼热
,则可将气体通过盛有灼热 的硬质玻璃管,若出现
的硬质玻璃管,若出现______ ,证明是 。
。
【问题研究】经充分论证,确认所得气体含有 和
和 。
。
(4)写出 与浓
与浓 反应生成
反应生成 的化学方程式
的化学方程式______ 。
(5)产生 的原因是
的原因是______ 。
(6)要用过量锌与浓 反应后的混合物制取
反应后的混合物制取 固体,首先需要进行的操作是
固体,首先需要进行的操作是______ 。
(7)有两种方案可制得 ,甲:
,甲: 与浓
与浓 反应;乙:
反应;乙: 和稀
和稀 反应。要制得等量的
反应。要制得等量的 ,哪个方案更好,理由是
,哪个方案更好,理由是______ 。
【提出猜想】从物质组成元素的角度来看,放出的气体可能是
 、
、 、
、 。
。【查阅资料】
 有刺激性气味,易溶于水,能使品红(一种有机色素,呈红色)溶液褪色,能与
有刺激性气味,易溶于水,能使品红(一种有机色素,呈红色)溶液褪色,能与 反应生成
反应生成 。
。【方案设计】实验小组的同学设计了如下一些方案。
(1)甲同学认为是
 ,其检验方法是
,其检验方法是(2)乙同学认为是
 ,则检验方法是
,则检验方法是(3)丙同学认为是
 ,则可将气体通过盛有灼热
,则可将气体通过盛有灼热 的硬质玻璃管,若出现
的硬质玻璃管,若出现 。
。【问题研究】经充分论证,确认所得气体含有
 和
和 。
。(4)写出
 与浓
与浓 反应生成
反应生成 的化学方程式
的化学方程式(5)产生
 的原因是
的原因是(6)要用过量锌与浓
 反应后的混合物制取
反应后的混合物制取 固体,首先需要进行的操作是
固体,首先需要进行的操作是(7)有两种方案可制得
 ,甲:
,甲: 与浓
与浓 反应;乙:
反应;乙: 和稀
和稀 反应。要制得等量的
反应。要制得等量的 ,哪个方案更好,理由是
,哪个方案更好,理由是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】化学兴趣小组的同学将足量的锌加入到浓硫酸中,发现有大量的气泡放出,他们对气体的成分进行了探究。
(提出问题)锌粒加入浓硫酸后生成的气体是什么?
(查阅资料)①浓硫酸具有吸水性,能与锌反应,但不产生氢气,也不会产生氧气。
②SO2有刺激性气味,易溶于水,能使品红溶液(一种红色色素)褪色。
(提出猜想)甲:气体是H2;乙:气体是SO2;丙:气体是H2和SO2。
(实验探究)针对上述猜想,同学们在老师的指导下设计了如图的实验装置进行探究实验。

(1)实验开始后,观察到A中品红溶液褪色,证明气体中含有________ 。
(2)B装置的作用是__________ 。
(3)C装置在点燃酒精灯加热之前应先通一段时间的气体,目的是______ ;加热一段时间后,观察到____ 现象,证明气体中含有H2。
(4)该实验装置存在一个缺点,请你指出:__________ 。
(讨论)
(5)锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么在反应过程中又产生了氢气呢?请从下列选项中选择一个你认为合适的答案______ 。
A. 因为浓硫酸在反应的过程中浓度降低变为稀硫酸,稀硫酸与锌反应放出了氢气
B. 因为锌和浓硫酸反应直接放出了氢气
C. 因为浓硫酸直接分解放出了氢气
(提出问题)锌粒加入浓硫酸后生成的气体是什么?
(查阅资料)①浓硫酸具有吸水性,能与锌反应,但不产生氢气,也不会产生氧气。
②SO2有刺激性气味,易溶于水,能使品红溶液(一种红色色素)褪色。
(提出猜想)甲:气体是H2;乙:气体是SO2;丙:气体是H2和SO2。
(实验探究)针对上述猜想,同学们在老师的指导下设计了如图的实验装置进行探究实验。

(1)实验开始后,观察到A中品红溶液褪色,证明气体中含有
(2)B装置的作用是
(3)C装置在点燃酒精灯加热之前应先通一段时间的气体,目的是
(4)该实验装置存在一个缺点,请你指出:
(讨论)
(5)锌和浓硫酸反应生成硫酸锌、水和二氧化硫,为什么在反应过程中又产生了氢气呢?请从下列选项中选择一个你认为合适的答案
A. 因为浓硫酸在反应的过程中浓度降低变为稀硫酸,稀硫酸与锌反应放出了氢气
B. 因为锌和浓硫酸反应直接放出了氢气
C. 因为浓硫酸直接分解放出了氢气
您最近一年使用:0次



