从海水中可制备纯碱和金属镁,其流程如图所示。

(1)粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下列物质:a适量的盐酸;b.稍过量的Na2CO3溶液;c稍过量的Ba(OH)2溶液。利用过滤等操作进行除杂,则加入这三种物质的先后顺序为______ (填字母序号)。
(2)向饱和的氯化钠溶液中通入氨气和二氧化碳经过一系列变化,最终可制得纯碱。请写出第Ⅲ步反应的化学方程式______ 。
(3)写出第Ⅵ步制取金属镁的化学反应方程式______ 。

(1)粗盐水中主要含有CaCl2、MgSO4等可溶性杂质,可加入下列物质:a适量的盐酸;b.稍过量的Na2CO3溶液;c稍过量的Ba(OH)2溶液。利用过滤等操作进行除杂,则加入这三种物质的先后顺序为
(2)向饱和的氯化钠溶液中通入氨气和二氧化碳经过一系列变化,最终可制得纯碱。请写出第Ⅲ步反应的化学方程式
(3)写出第Ⅵ步制取金属镁的化学反应方程式
更新时间:2019-03-05 15:19:25
|
相似题推荐
填空与简答-推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F、G是初中常见的物质,其转化关系如下图所示。其中A、B、C、D、E是五种不同类别的物质,C是厕所清洁剂的重要成分。E是侯氏制碱法的产品之一,俗名纯碱。G为红棕色固体,B常温下是液体。(图中反应条件及部分反应物、生成物已省略,“—”表示反应关系“→”表示转化关系)

⑴写出下列物质的化学式:G_________ ;
⑵写出D→F的化学反应方程式_____________________________ 。

⑴写出下列物质的化学式:G
⑵写出D→F的化学反应方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
真题
【推荐2】A、B、C、D是初中化学中常见的物质。A是一种常见的盐,其水溶液显碱性,A和B反应生成的一种物质C在大气中含量的增加会导致温室效应。D是一种常见的碱,B和D反应生成的一种物质是我们厨房常用的调味品。
(1)写出B的化学式_________ ;
(2)A和B的反应属于________ 反应(填基本反应类型);
(3)B和D反应的实质是_________ 。
(1)写出B的化学式
(2)A和B的反应属于
(3)B和D反应的实质是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】化学与人类生活息息相关。请用化学知识回答下列问题。
(1)下表列举了生活中三种常见的清洁剂,且NaClO+2HCl═NaCl+Cl2↑+H2O(Cl2黄绿色、有毒),下列说法错误的是______ (填序号)。
a.“洁厕灵”可用于金属表面除锈
b.洁厕灵和漂白水二者混用效果更好
c.NaClO中Cl元素的化合价是﹣1价
d.可以在家庭中用彩漂液制取氧气
(2)农作物增产依赖化学,NH4Cl、KCl、KNO3、Ca(H2PO4)2都是常用的化肥,其中属于______ 复合肥。
(3)正常雨水pH约为5.6的原因是______ (用化学方程式表示)。
(4)有的胃病患者胃酸过多,医生建议服用一些含氢氧化铝的药物,请用化学方程式表示其原理______ 。
(5)“釜底抽薪”原意是把柴火从锅底抽掉,该方法能阻断燃烧的原因是______ 。
(1)下表列举了生活中三种常见的清洁剂,且NaClO+2HCl═NaCl+Cl2↑+H2O(Cl2黄绿色、有毒),下列说法错误的是
| 清洁剂 |  |  |  |
| 名称 | 洁厕灵 | 彩漂液 | 漂白水 |
| 功能 | 清除污垢,除异味 | 漂洗衣物,使色彩鲜艳 | 漂除衣物污渍 |
| 有效成分 | 盐酸(HCl) | 过氧化氢(H2O2) | 次氯酸钠(NaClO) |
b.洁厕灵和漂白水二者混用效果更好
c.NaClO中Cl元素的化合价是﹣1价
d.可以在家庭中用彩漂液制取氧气
(2)农作物增产依赖化学,NH4Cl、KCl、KNO3、Ca(H2PO4)2都是常用的化肥,其中属于
(3)正常雨水pH约为5.6的原因是
(4)有的胃病患者胃酸过多,医生建议服用一些含氢氧化铝的药物,请用化学方程式表示其原理
(5)“釜底抽薪”原意是把柴火从锅底抽掉,该方法能阻断燃烧的原因是
您最近一年使用:0次
【推荐1】某兴趣小组的同学在实验室用含有少量MgCl2的NaCl固体配制一定质量分数的NaCl溶液.实验步骤如下图所示:
下图所示:

请回答:
(1)在“溶液A”中加入过量NaOH溶液所发生反应的化学方程式为_______ 。
(2)操作2的名称是_______ ,在“操作2”中,要用到的玻璃仪器除玻璃棒、烧杯外,还有______ 。
(3)加入“适量HCl”的目的是__________ 。
(4)操作3是蒸发,为了得到固体NaCl,应蒸发至______ 时停止加热,该操作中玻璃棒的作用是______ 。
(5)配制一定溶质质量分数的氯化钠溶液常有以下操作。

请回答下列问题:
①用上图所示的序号 表示配制该溶液的正确操作顺序为____________ 。
②用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应________ 。
A.调节游码
B.添加砝码
C.减少适量氯化钠固体
D.增加适量氯化钠固体
③下列过程中对所配制溶液的溶质质量分数没有影响的是_______ 。
A.配制时所用烧杯中有少量水
B.称量时有少量氯化钠残留在纸上
C.将量筒中的水转移到烧杯时,有少量水溅出
D.搅拌均匀后,转移到试剂瓶时有少量溶液溅出
下图所示:

请回答:
(1)在“溶液A”中加入过量NaOH溶液所发生反应的化学方程式为
(2)操作2的名称是
(3)加入“适量HCl”的目的是
(4)操作3是蒸发,为了得到固体NaCl,应蒸发至
(5)配制一定溶质质量分数的氯化钠溶液常有以下操作。

请回答下列问题:
①用
②用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应
A.调节游码
B.添加砝码
C.减少适量氯化钠固体
D.增加适量氯化钠固体
③下列过程中对所配制溶液的溶质质量分数没有影响的是
A.配制时所用烧杯中有少量水
B.称量时有少量氯化钠残留在纸上
C.将量筒中的水转移到烧杯时,有少量水溅出
D.搅拌均匀后,转移到试剂瓶时有少量溶液溅出
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】实验室有一包固体混合物,可能由Fe(OH)3、KOH、Ba(NO3)2、K2CO3、C、Cu、CuO中的三种物质组成。某校化学兴趣小组的同学为了探究其成分,设计了如下实验流程:
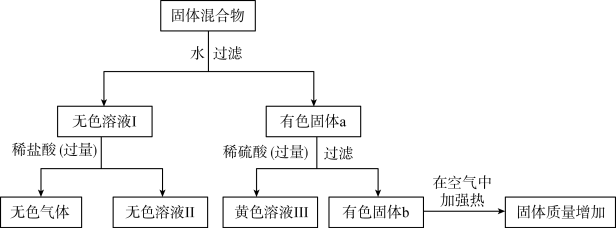
请回答下列有关问题:
(1)无色溶液Ⅱ中所含阳离子的符号是___________ 。
(2)有色固体a与稀硫酸反应的化学方程式为___________ 。
(3)有色固体b在空气中加强热时发生反应的化学方程式为___________ 。
(4)这包固体混合物的成分是___________ 。

请回答下列有关问题:
(1)无色溶液Ⅱ中所含阳离子的符号是
(2)有色固体a与稀硫酸反应的化学方程式为
(3)有色固体b在空气中加强热时发生反应的化学方程式为
(4)这包固体混合物的成分是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】我国力争在2060年前实现“碳中和”。
Ⅰ.碳捕集工业上一种利用NaOH溶液实现“碳捕集”技术的流程如图所示。

(1)①反应分离室中发生复分解反应的化学方程式为______________ 。
②流程中可循环利用的物质有CaO、______________ 。
Ⅱ. 碳封存“碳封存”可从大气中分离出二氧化碳将其压缩液化泵入地下长期储存。
(2)“碳封存”可将CO2压缩至地下储存,其原因是___________ (从微观角度解释)。
Ⅲ. 碳利用
我国科学家在实验室实现以CO2和H2为原料人工合成淀粉(C6H10O5)n,人工合成淀粉技术可分为以下两个阶段,如图所示:

阶段1:从太阳能→电能→氢能→甲醇;
阶段2:以甲醇为原料通过“C1→C3→C6→淀粉”的策略,多步酶催化合成淀粉。
(3)①在阶段1中,利用氢能合成甲醇的化学反应方程式为_____________ 。
②若用44gCO2人工合成淀粉(假设反应过程中无含碳物质的加入和损失),计算理论上制得淀粉的质量________ (写出计算过程)。
(4)人工合成淀粉技术虽处于实验室阶段,但对解决粮食危机和减少碳排放有着重大意义。传统农业中绿色植物(以玉米为例)光合作用和人工合成淀粉技术合成等量淀粉的对比如下表所示。
据表分析,人工合成淀粉技术相较于传统农业,其优势是____________ 。(写出1点)
Ⅰ.碳捕集工业上一种利用NaOH溶液实现“碳捕集”技术的流程如图所示。

(1)①反应分离室中发生复分解反应的化学方程式为
②流程中可循环利用的物质有CaO、
Ⅱ. 碳封存“碳封存”可从大气中分离出二氧化碳将其压缩液化泵入地下长期储存。
(2)“碳封存”可将CO2压缩至地下储存,其原因是
Ⅲ. 碳利用
我国科学家在实验室实现以CO2和H2为原料人工合成淀粉(C6H10O5)n,人工合成淀粉技术可分为以下两个阶段,如图所示:

阶段1:从太阳能→电能→氢能→甲醇;
阶段2:以甲醇为原料通过“C1→C3→C6→淀粉”的策略,多步酶催化合成淀粉。
(3)①在阶段1中,利用氢能合成甲醇的化学反应方程式为
②若用44gCO2人工合成淀粉(假设反应过程中无含碳物质的加入和损失),计算理论上制得淀粉的质量
(4)人工合成淀粉技术虽处于实验室阶段,但对解决粮食危机和减少碳排放有着重大意义。传统农业中绿色植物(以玉米为例)光合作用和人工合成淀粉技术合成等量淀粉的对比如下表所示。
| 玉米淀粉 | 人工合成淀粉 | |
| 能量转化效率 | 2% | 7% |
| 生产条件与方式 | 阳光、灌溉、施肥施药、收割 | 全天候车间生产 |
| 生产周期 | 4-6个月 | 1-2天 |
您最近一年使用:0次
【推荐1】乳山是一座美丽的滨海小城,拥有漫长的海岸线,蕴藏着丰富的海洋资源,粗盐中含有泥沙等不溶性杂质,还含有氯化钙、氯化镁、硫酸钠等可溶性杂质。提纯粗盐并制取纯碱的工艺流程如下:

【查阅资料】20℃时,几种物质在水中的溶解度/g如下表所示。请根据有关信息,回答下列问题:
(1)步骤Ⅲ中加入试剂A的化学式是______ 。步骤Ⅳ中加入过量Na2CO3溶液的目的是除去(填离子符号)______ ,步骤V加入适量稀盐酸的目的是______ 。
(2)在步骤Ⅵ反应中,X、Y分别是(填化学式)______ 、______ ;有NaHCO3晶体析出,而没有NH4C1和NaCl析出的原因是______ 。该反应的化学方程式是______ 。
(3)步骤Ⅶ中 NaHCO3转化为纯碱的化学反应方程式______ 。

【查阅资料】20℃时,几种物质在水中的溶解度/g如下表所示。请根据有关信息,回答下列问题:
| NaCl | NH4C1 | NaHCO3 |
| 36.0 | 37.2 | 9.6 |
(2)在步骤Ⅵ反应中,X、Y分别是(填化学式)
(3)步骤Ⅶ中 NaHCO3转化为纯碱的化学反应方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
【推荐2】Ⅰ下面是某工厂苛化法生产烧碱的示意图。请回答下列问题:

(1)X的化学式________ 。
(2)生石灰可以由__________ (填名称)高温煅烧而得,其反应的化学方程式为:________________ 。
(3)操作②的名称是_________ ;结晶得到的固体烧碱中可能含有少量的__________ (写化学式);烧碱有强烈的腐蚀性,如果不慎将碱液沾到皮肤上,可先用较多的水冲洗,再涂上稀_________ 溶液。
(4)滤液C可加入反应池循环再利用,目的是降低生产成本和防止__________ 。
(5)操作①需要的玻璃仪器有漏斗、玻璃棒________ ,其中玻璃棒的作用为_________________
Ⅱ.我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如下:

⑴粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制。则加入试剂合理的顺序为_______ 、盐酸(写序号,只写一种)。加盐酸的作用是(用化学方程式表示)_______________ 、_______________ 。
(2)X的化学式为_______ 。
(3)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为_______ ,写出Y的一种用途_______ 。

(1)X的化学式
(2)生石灰可以由
(3)操作②的名称是
(4)滤液C可加入反应池循环再利用,目的是降低生产成本和防止
(5)操作①需要的玻璃仪器有漏斗、玻璃棒
Ⅱ.我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如下:

⑴粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制。则加入试剂合理的顺序为
(2)X的化学式为
(3)Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】碳酸钠用途非常广泛,是工业生产中重要的化工原料。1921年,我国制碱工业的先驱侯德榜创造了一种将制碱与制氨结合起来的“联合制碱法”。其生产工艺流程示意图如图:
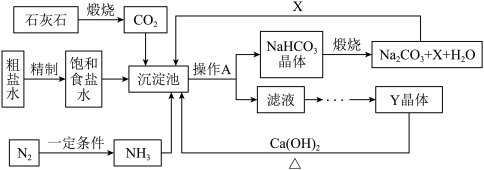
(1)工业上用分离液态空气的方法制取氮气,属于______ 变化(填“物理”或“化学”)。
(2)高温煅烧石灰石可以得到二氧化碳,反应原理为______ 。(用化学方程式表示)
(3)粗盐水中主要含有Ca2+、Mg2+、 等杂质离子,工业上常用加入稍过量的①NaOH溶液、②Na2CO3溶液、③BaCl2溶液及适量的盐酸除杂、精制。则加入试剂合理的顺序为
等杂质离子,工业上常用加入稍过量的①NaOH溶液、②Na2CO3溶液、③BaCl2溶液及适量的盐酸除杂、精制。则加入试剂合理的顺序为______ (填序号)。
(4)30℃时,“沉淀池”中的主要反应为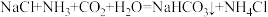 ,下列说法正确的是______;
,下列说法正确的是______;
(5)Y是滤液中最主要成分,Y在农业生产中的一种用途是______ 。

(1)工业上用分离液态空气的方法制取氮气,属于
(2)高温煅烧石灰石可以得到二氧化碳,反应原理为
(3)粗盐水中主要含有Ca2+、Mg2+、
 等杂质离子,工业上常用加入稍过量的①NaOH溶液、②Na2CO3溶液、③BaCl2溶液及适量的盐酸除杂、精制。则加入试剂合理的顺序为
等杂质离子,工业上常用加入稍过量的①NaOH溶液、②Na2CO3溶液、③BaCl2溶液及适量的盐酸除杂、精制。则加入试剂合理的顺序为(4)30℃时,“沉淀池”中的主要反应为
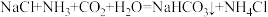 ,下列说法正确的是______;
,下列说法正确的是______;| A.该反应消耗CO2体现碳中和 |
B.反应后溶液中不含 |
| C.两种产物均属于盐 |
| D.常温下NaCl溶液的pH=7 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某氯化钾固体样品中含有少量氯化钙和硫酸镁等杂质,实验室提纯氯化钾流程如下:

(1)过滤时发现过滤速度较慢,可能是固体颗粒阻碍了液体通过滤纸孔隙,还可能是___________ 。在蒸发操作中玻璃棒的作用是___________ 。
(2)加入过量氢氧化钡溶液除去的杂质离子是___________ (填离子符号);Y溶液中溶质是___________ (填写化学式)。若先加入过量Y溶液,再加过量氢氧化钡溶液,则蒸发后所得固体中含有的杂质是___________ (填写化学式)。

(1)过滤时发现过滤速度较慢,可能是固体颗粒阻碍了液体通过滤纸孔隙,还可能是
(2)加入过量氢氧化钡溶液除去的杂质离子是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如图:
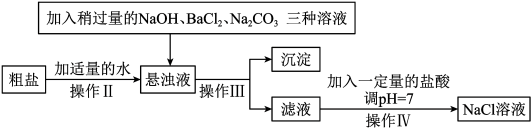
(1)加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是_______ (用化学方程式表示)。
(2)实验操作Ⅲ是_______ ,要用到的实验玻璃仪器是玻璃棒、漏斗和______ 。
(3)如果稍过量的试剂加入的顺序依次为:Na2CO3、NaOH、BaCl2,则最后得到的氯化钠溶液中一定含有杂质________ 。
(4)操作Ⅳ的方法可以是:先在滤液中滴入酚酞溶液,再逐滴滴入盐酸直到滤液的pH=7,依据的现象是溶液由________ ,如果加入的盐酸有点过量了,对后面NaCl溶液的结晶是否有影响________ (是或否)。

(1)加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是
(2)实验操作Ⅲ是
(3)如果稍过量的试剂加入的顺序依次为:Na2CO3、NaOH、BaCl2,则最后得到的氯化钠溶液中一定含有杂质
(4)操作Ⅳ的方法可以是:先在滤液中滴入酚酞溶液,再逐滴滴入盐酸直到滤液的pH=7,依据的现象是溶液由
您最近一年使用:0次
【推荐3】本草古籍是中医药文化中极为重要的一部分,蕴藏着深厚的人文底蕴,同时也涉及大量化学知识。
(1)《神农本草经》记载:“药性有宜丸者.......宜酒渍者”。“酒渍”类似于酒精在“自制指示剂实验”中的作用,“酒渍”的作用是______ 。
(2)《神农本草经》记载:“孔公孽主伤食不化”。孔公孽(主要成分为CaCO3)可用于治疗胃酸过多。写出该反应的化学方程式:______ 。
(3)《开宝本草》记载了KNO3的提纯方法:“......所在山泽。冬月地上有霜,扫取以水淋汁后,乃煎炼而成”。与“乃煎炼而成”相似的实验操作是______ 。
(4)《本草图经》记载:“以铁拍作片段,置醋棚中积久衣生刮取者,为铁华粉”。铁华粉可用作补血剂,其有效成分为醋酸亚铁[Fe(CH3COO)2]。1.74g醋酸亚铁中铁元素质量为______ 。
(1)《神农本草经》记载:“药性有宜丸者.......宜酒渍者”。“酒渍”类似于酒精在“自制指示剂实验”中的作用,“酒渍”的作用是
(2)《神农本草经》记载:“孔公孽主伤食不化”。孔公孽(主要成分为CaCO3)可用于治疗胃酸过多。写出该反应的化学方程式:
(3)《开宝本草》记载了KNO3的提纯方法:“......所在山泽。冬月地上有霜,扫取以水淋汁后,乃煎炼而成”。与“乃煎炼而成”相似的实验操作是
(4)《本草图经》记载:“以铁拍作片段,置醋棚中积久衣生刮取者,为铁华粉”。铁华粉可用作补血剂,其有效成分为醋酸亚铁[Fe(CH3COO)2]。1.74g醋酸亚铁中铁元素质量为
您最近一年使用:0次



