某化学实验室产生的废液中含有FeCl3、CuCl2、CaCl2,为了处理废液,回收金属并制备氯化铁晶体,现设计如下实验过程(部分):
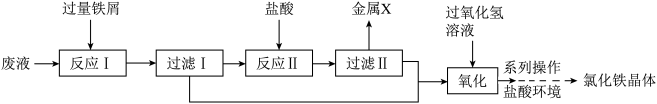
已知:氯化铁溶液在加热过程中,容易产生氢氧化铁沉淀。
(1)金属X的化学式为______ 。
(2)已知“反应Ⅰ”中的其中一个反应为2FeCl3+Fe===3FeCl2,另一个反应的化学方程式为___ ;“反应Ⅱ”的化学方程式为 __________ 。
(3)氧化过程的反应化学方程式为2FeCl2+H2O2+2HCl===2FeCl3+2H2O,选用过氧化氢溶液氧化的优点是__________ 。
(4)“系列操作”中包含:蒸发浓缩、__________ 、过滤,玻璃棒在蒸发浓缩过程中的作用是_________ 。

已知:氯化铁溶液在加热过程中,容易产生氢氧化铁沉淀。
(1)金属X的化学式为
(2)已知“反应Ⅰ”中的其中一个反应为2FeCl3+Fe===3FeCl2,另一个反应的化学方程式为
(3)氧化过程的反应化学方程式为2FeCl2+H2O2+2HCl===2FeCl3+2H2O,选用过氧化氢溶液氧化的优点是
(4)“系列操作”中包含:蒸发浓缩、
更新时间:2019-05-06 10:46:13
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】为了回收硝酸亚铁和硝酸银的混合溶液中的银,设计了如图的实验方案:
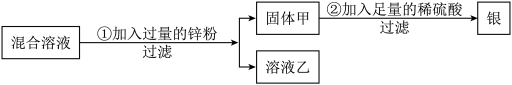
(1)若溶液乙为无色溶液,则固体甲一定有的物质是__________ (填写物质名称,下同),可能有的物质是_____ ,步骤②中肯定发生的反应的化学方程式为__________ ;
(2)若溶液乙为浅绿色溶液,则溶液乙的溶质中一定有_____ (填写物质的化学式,下同),可能有_______________ 。

(1)若溶液乙为无色溶液,则固体甲一定有的物质是
(2)若溶液乙为浅绿色溶液,则溶液乙的溶质中一定有
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】如图中的五个圆A、B、C、D、E分别表示硝酸铜溶液、铁粉、稀硫酸、氧气、一氧化碳五种物质,其中E是一种蓝色溶液,用“→”表示一种物质能转化为另一种物质,用“—”表示两物质能发生反应,五种物质的反应关系及转化关系如图所示。请回答下列问题:
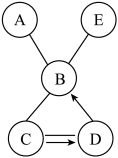
(1)请写出图中五种物质(或主要物质)的化学式:
A______ ;B______ ;C______ ;D______ ;E______ 。
(2)请写出A与B反应的实验现象:______ 。
(3)请写出B与E反应的化学方程式:______ 。

(1)请写出图中五种物质(或主要物质)的化学式:
A
(2)请写出A与B反应的实验现象:
(3)请写出B与E反应的化学方程式:
您最近一年使用:0次
【推荐1】A、B、C三种物质的溶解度曲线如图所示。请回答下列问题:
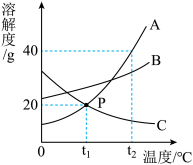
(1)P点表示的意义是___________ 。
(2)从B物质的饱和溶液中获得B最好的办法是___________ 。
(3)t2℃时,取ABC三种物质各10g,分别加入到50g水中,能形成饱和溶液的是___________ 。
(4)将t2℃,ABC三种物质的饱和溶液分别降温到t1℃,所得溶液中溶质的质量分数由大到小的顺序为___________ 。
(5)t1℃,将240gA物质的饱和溶液加水稀释成溶质的质量分数为10%的溶液,需加入水的质量为___________ g。

(1)P点表示的意义是
(2)从B物质的饱和溶液中获得B最好的办法是
(3)t2℃时,取ABC三种物质各10g,分别加入到50g水中,能形成饱和溶液的是
(4)将t2℃,ABC三种物质的饱和溶液分别降温到t1℃,所得溶液中溶质的质量分数由大到小的顺序为
(5)t1℃,将240gA物质的饱和溶液加水稀释成溶质的质量分数为10%的溶液,需加入水的质量为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】以高纯度的二氧化锰为原料制备高锰酸钾的主要流程如下:

(1)熔融氧化时,也可以用氯酸钾代替空气,原因是______ 。
(2)“酸化”时反应的化学方程式为: ,该反应中锰元素的转化率(所得高锰酸钾中锰元素与反应物中锰元素的质量百分比)为
,该反应中锰元素的转化率(所得高锰酸钾中锰元素与反应物中锰元素的质量百分比)为______ (精确到小数点后一位)。
(3)操作Ⅱ是根据KMnO4和K2CO3两种物质在溶解性上的差异将两者分离。具体操作步骤为:蒸发浓缩、降温结晶,过滤,洗涤干燥,得KMnO4晶体。则两者中______ (填化学式)的溶解度受温度影响变化更大,母液是高锰酸钾的______ 溶液(填“饱和”或“不饱和”)。蒸发过程中温度不宜过高,原因是______ (用方程式表示)。
(4)本流程中可以循环利用的物质是______ 。
(5)电解法也可以实现由K2MnO4向KMnO4的转化,与“通CO2”相比,其优点是______ (填字母,该反应的化学方程式为: )。
)。
a.节约能源 b.锰元素转化率高 c.得到的KOH可以循环利用 d.可以同时获得氢气

(1)熔融氧化时,也可以用氯酸钾代替空气,原因是
(2)“酸化”时反应的化学方程式为:
 ,该反应中锰元素的转化率(所得高锰酸钾中锰元素与反应物中锰元素的质量百分比)为
,该反应中锰元素的转化率(所得高锰酸钾中锰元素与反应物中锰元素的质量百分比)为(3)操作Ⅱ是根据KMnO4和K2CO3两种物质在溶解性上的差异将两者分离。具体操作步骤为:蒸发浓缩、降温结晶,过滤,洗涤干燥,得KMnO4晶体。则两者中
(4)本流程中可以循环利用的物质是
(5)电解法也可以实现由K2MnO4向KMnO4的转化,与“通CO2”相比,其优点是
 )。
)。a.节约能源 b.锰元素转化率高 c.得到的KOH可以循环利用 d.可以同时获得氢气
您最近一年使用:0次
【推荐3】硝酸钾和氯化钾两种物质的溶解度表及曲线如图 1。
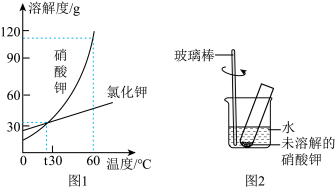
请回答下列问题:
(1)观察溶解度曲线和溶解度表,判断物质乙是指______ (填写化学式)。
(2)60℃时,饱和 KNO3溶液中混有少量 KC1,应采用______ 的方法提纯 KNO3(填写“蒸发溶剂”或“冷却结晶”)。
(3)60℃时,分别将等质量的 KNO3和 KC1 两种物质的饱和溶液温度降至 t℃,析出晶体的质量关系为:KNO3______ KCI(填写“>”“=”或“<”下同)。20℃时,甲、乙两种物质的饱和溶液各 100g,所含溶剂的质量关系是甲______ 乙。
(4)如图 2 所示,20℃时,将一定质量的 KNO3固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解、则加入的物质可以是______ 。
①冰块 ②生石灰固体 ③硝酸铵固体 ④干冰 ⑤浓硫酸 ⑥氢氧化钠固体
(5)60℃时,将 45gKCI 固体溶解于 100g 水中,降温至 20℃,析出体的质量是______ g。
(6)如图所示,弹簧秤下挂着 A 为木块,B 为饱和氯化钠溶液,在恒温条件下向烧杯内溶液中加入 KNO3晶体,弹簧秤读数______ (填“变大”、“变小”、“不变”)

温度 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度 | 甲 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
乙 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | |

请回答下列问题:
(1)观察溶解度曲线和溶解度表,判断物质乙是指
(2)60℃时,饱和 KNO3溶液中混有少量 KC1,应采用
(3)60℃时,分别将等质量的 KNO3和 KC1 两种物质的饱和溶液温度降至 t℃,析出晶体的质量关系为:KNO3
(4)如图 2 所示,20℃时,将一定质量的 KNO3固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解、则加入的物质可以是
①冰块 ②生石灰固体 ③硝酸铵固体 ④干冰 ⑤浓硫酸 ⑥氢氧化钠固体
(5)60℃时,将 45gKCI 固体溶解于 100g 水中,降温至 20℃,析出体的质量是
(6)如图所示,弹簧秤下挂着 A 为木块,B 为饱和氯化钠溶液,在恒温条件下向烧杯内溶液中加入 KNO3晶体,弹簧秤读数

您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】某化学兴趣小组用锌、硫酸、氢氧化钙、硫酸铜和碳酸钠五种物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生化学反应。其中B与C反应产生的气体是光合作用的原料之一,E物质的溶液呈蓝色。
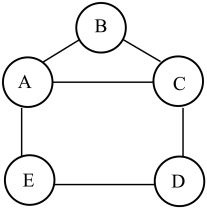
(1)写出D和E的化学式:D_________ ,E_______ 。
(2)B物质的俗称是_________ ,请写出C物质的一种用途_________ 。
(3)D与E的反应所属基本反应类型为__________ 。
(4)按游戏规则,下列能替代A物质的是_____ (填序号)。
①银 ②氢氧化钡 ③氯化钡 ④氧化铜

(1)写出D和E的化学式:D
(2)B物质的俗称是
(3)D与E的反应所属基本反应类型为
(4)按游戏规则,下列能替代A物质的是
①银 ②氢氧化钡 ③氯化钡 ④氧化铜
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐2】将铁粉和铜粉的混合物加入硝酸银溶液中,充分反应后过滤。
(1)若向过滤后的固体中加入稀硫酸,有气体生成,则该固体中含有哪些物质?_________________ 。
(2)若向滤液中加入稀盐酸,有白色沉淀生成,则滤液中含有哪些金属离子_________ (写离子符号)并写出产生白色沉淀的反应方程式:_______________________________ 。
(1)若向过滤后的固体中加入稀硫酸,有气体生成,则该固体中含有哪些物质?
(2)若向滤液中加入稀盐酸,有白色沉淀生成,则滤液中含有哪些金属离子
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】某工厂利用硼砂(主要成分为Na2B4O7,含少量硫酸铁杂质)制备硼(B)单质的部分流程如图所示:
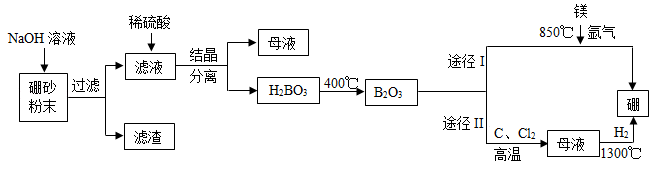
已知:BCl3在常温下是一种气体;MgO、B的熔点均高于2000℃。
(1)“结晶分离”过程包含:蒸发浓缩、___________ 和过滤。
(2)加入NaOH溶液反应的化学方程式为___________ ,该反应属于___________ 反应(填基本反应类型);母液中一定含有的溶质为H3BO3、___________ (填化学式)。
(3)镁和B2O3发生反应的化学方程式为___________ ,是___________ 反应。
(4)获得高纯度的硼,适宜选择途径___________ (填“Ⅰ”或“Ⅱ”),理由是___________ 。

已知:BCl3在常温下是一种气体;MgO、B的熔点均高于2000℃。
(1)“结晶分离”过程包含:蒸发浓缩、
(2)加入NaOH溶液反应的化学方程式为
(3)镁和B2O3发生反应的化学方程式为
(4)获得高纯度的硼,适宜选择途径
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】硫酸铝在造纸、水净化、土壤改良中有广泛的应用,某化工厂利用炼铝厂废料(主要成分含Al、Al2O3、SiO2、FeO、Fe2O3)制备硫酸铝晶体的工艺流程如图所示,回答以下问题。
查阅资料:部分金属离子生成氢氧化物开始沉淀和沉淀完全的pH范围:
资料:加入过氧化氢溶液使得溶液中的亚铁离子转化为铁离子。
(1)“预处理”时需要将铝废料粉碎,其目的是_______ 。
(2)料液1中含有的阳离子是______ ,料渣1的成分是______ 。
(3)试剂a用来调pH使得部分离子沉淀,为了不引入新的杂质,试剂A最好选用______ 。
A.氧化铝 B.氢氧化钾 C.氢氧化钠 D.稀硫酸
pH的范围应该控制在______ 。
(4)操作X是蒸发浓缩、______ 、过滤、洗涤、干燥。
查阅资料:部分金属离子生成氢氧化物开始沉淀和沉淀完全的pH范围:
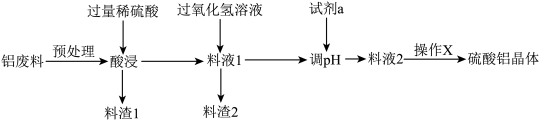
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀的pH | 3.6 | 6.3 | 2.3 |
| 沉淀完全的pH | 4.9 | 8.3 | 3.2 |
(1)“预处理”时需要将铝废料粉碎,其目的是
(2)料液1中含有的阳离子是
(3)试剂a用来调pH使得部分离子沉淀,为了不引入新的杂质,试剂A最好选用
A.氧化铝 B.氢氧化钾 C.氢氧化钠 D.稀硫酸
pH的范围应该控制在
(4)操作X是蒸发浓缩、
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】醋酸钙[Ca(Ac)2]是国家允许使用的补钙制剂之一。以蛋壳为原料回收膜并制备醋酸钙的一种工艺流程如图。
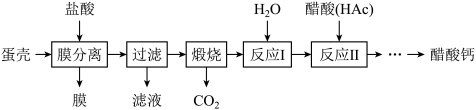
(1)写出煅烧时的化学方程式__________________ 。CO2的任意排放会引发的环境问题,可以将CO2与CH4一定条件下化合生成化工产品甲醛(HCHO),则此反应中CO2与CH4的最佳质量比是____________ 。
(2)在反应I中制备石灰乳,而不是制备澄清石灰水的目的是____________________ ,写出熟石灰的一种用途________________ 。
(3)在反应II中醋酸过量的目的是_______________ ,写出反应II的化学方程式________ 。
(4)膜分离时,盐酸不能过量的主要原因是________________ 。

(1)写出煅烧时的化学方程式
(2)在反应I中制备石灰乳,而不是制备澄清石灰水的目的是
(3)在反应II中醋酸过量的目的是
(4)膜分离时,盐酸不能过量的主要原因是
您最近一年使用:0次




