今年3月22日是第二十二届“世界水日”,3月22﹣28日是第二十七届“中国水周”.联合国确定“世界水日”的宣传主题是“水与能源”(Water and Energy).水与人类的生活和生产密切相关.如图为我国《生活饮用水国家标准》的部分内容,请回答下列问题.
(1)测得某地区合格饮用水的pH=6.6,可知略呈_____性(填“酸”或“碱”),通常是因为水中有一种常见弱酸是_____(填化学式).
(2)生活饮用水中的铝元素以铝离子形式存在,则3个铝离子表示为_____,铁元素以硫酸铁形式存在,硫酸铁的化学式为_____.
(3)天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是_____.
(4)(选做)天然水的硬度较大时,煮沸后饮用是降低硬度的方法之一,其化学原理是Ca(HCO3)2、Mg(HCO3)2加热后发生反应生成了水垢.Ca(HCO3)2加热分解为碳酸钙、二氧化碳和水,请写出化学方程式_____,Mg(HCO3)2加热后分解为氢氧化镁和二氧化碳,请写出化学方程式_____,因而水垢的主要成分有2种,请写出醋酸(用HAc代表醋酸)与水垢中碳酸钙反应的化学方程式_____.
(5)1升合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量应不超过_____mg.
| 项目 限值 |
| 色 度 不超过15度 并不得呈现其他异色 浑浊度 不超过1度 特殊情况下不超过5度 pH 6.5-8.5 总硬度(以CaCO3计) 450mg/L 铝 0.2mg/L 铁 0.3mg/L 硫酸盐 250mg/L |
(2)生活饮用水中的铝元素以铝离子形式存在,则3个铝离子表示为_____,铁元素以硫酸铁形式存在,硫酸铁的化学式为_____.
(3)天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是_____.
(4)(选做)天然水的硬度较大时,煮沸后饮用是降低硬度的方法之一,其化学原理是Ca(HCO3)2、Mg(HCO3)2加热后发生反应生成了水垢.Ca(HCO3)2加热分解为碳酸钙、二氧化碳和水,请写出化学方程式_____,Mg(HCO3)2加热后分解为氢氧化镁和二氧化碳,请写出化学方程式_____,因而水垢的主要成分有2种,请写出醋酸(用HAc代表醋酸)与水垢中碳酸钙反应的化学方程式_____.
(5)1升合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量应不超过_____mg.
更新时间:2019-05-11 15:14:57
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】氢化钙(CaH2)固体是登山队员常用的能源提供剂,用它和水反应生成氢氧化钙和氢气,
(1)写出该反应化学方程式为______ ;
(2)现有84g氢化钙与足量水反应,可生成氢气的质量是多少?
(1)写出该反应化学方程式为
(2)现有84g氢化钙与足量水反应,可生成氢气的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】铜长时间放置会与空气中的O2、H2O、CO2发生化合反应生成Cu2(OH)2CO3,该反应的化学方程式为___________ ;向9g氧化铁和铜的混合物中通入足量一氧化碳还原后,反应前后固体中铜元素的质量分数之比为3:4,则原混合物中氧化铁的质量为___________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)某化合物由碳、氧两种元素组成,碳、氧元素的质量比为3:8,该化合物的化学式量为44,它的化学式为_______ 。
(2)已知镁的相对原子质量为24,铜的相对原子质量为64。若镁、铜各为2g,则其中所含有的镁、铜原子个数比为_______ 。
(1)某化合物由碳、氧两种元素组成,碳、氧元素的质量比为3:8,该化合物的化学式量为44,它的化学式为
(2)已知镁的相对原子质量为24,铜的相对原子质量为64。若镁、铜各为2g,则其中所含有的镁、铜原子个数比为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】乳酸亚铁片可用于治疗缺铁性贫血,如图为乳酸亚铁说明书上部分文字.请仔细阅读后回答:
(1)乳酸亚铁中共有_________ 种元素.
(2)每个乳酸亚铁分子中含有___________ 个原子,
(3)每片乳酸亚铁中含有的铁元素的质量是__________________ (只列出计算式即可,不要求计算结果).
【主要成分】乳酸亚铁,化学式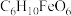 【用量】成人治疗量 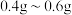 /日 /日【注意事项】1.宜饭后口服 2.服时忌茶,以免被鞣质沉淀 【规格】  /片 /片 |
(2)每个乳酸亚铁分子中含有
(3)每片乳酸亚铁中含有的铁元素的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】医用酒精、84消毒液[主要成分为次氯酸钠(NaClO)]等常用于对环境进行杀菌、消毒。
(1)医用消毒酒精中酒精的体积分数为75%,其中溶质的化学式为_______ 。
(2)学校现有“84消毒液”(原液)中有效氯浓度为50g/L,兴趣小组用该原液配制了1L有效氯浓度为0.5g/L的消毒液。
①所需原液的体积为_______ mL。
②配制过程中,需要的仪器有烧杯、玻璃棒、胶头滴管、_______ 。
(3)SO2是造成酸雨的主要空气污染物之一。SO2可用次氯酸钠(NaClO)溶液来吸收,发生反应的化学方程式为NaClO+SO2+H2O═NaCl+H2SO4.某实验室用一定量含14.9g次氯酸钠(NaClO)的“84消毒液”,理论上可以吸收的二氧化硫的质量为_____ g?(请将计算过程写到答题卡上)
(1)医用消毒酒精中酒精的体积分数为75%,其中溶质的化学式为
(2)学校现有“84消毒液”(原液)中有效氯浓度为50g/L,兴趣小组用该原液配制了1L有效氯浓度为0.5g/L的消毒液。
①所需原液的体积为
②配制过程中,需要的仪器有烧杯、玻璃棒、胶头滴管、
(3)SO2是造成酸雨的主要空气污染物之一。SO2可用次氯酸钠(NaClO)溶液来吸收,发生反应的化学方程式为NaClO+SO2+H2O═NaCl+H2SO4.某实验室用一定量含14.9g次氯酸钠(NaClO)的“84消毒液”,理论上可以吸收的二氧化硫的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】长江水经净化处理,可成为居民的生产生活用水。
(1)水净化时先沉降过滤,后通过活性炭再经消毒处理。其中活性炭的作用是______ 。
(2)生活中常通过______ 方法可降低水的硬度
(3)世界卫生组织规定饮用水中 ClO2剩余量应小于 0.2mg/L。取 1.5L 经 ClO2消毒后的饮用水,与足量 KI 充分反应(原理: ),测得生成 I2的质量为 0.508mg。请通过计算判断该饮用水中 ClO2的含量是否符合世界卫生组织标准(写出计算过程)。
),测得生成 I2的质量为 0.508mg。请通过计算判断该饮用水中 ClO2的含量是否符合世界卫生组织标准(写出计算过程)。
(1)水净化时先沉降过滤,后通过活性炭再经消毒处理。其中活性炭的作用是
(2)生活中常通过
(3)世界卫生组织规定饮用水中 ClO2剩余量应小于 0.2mg/L。取 1.5L 经 ClO2消毒后的饮用水,与足量 KI 充分反应(原理:
 ),测得生成 I2的质量为 0.508mg。请通过计算判断该饮用水中 ClO2的含量是否符合世界卫生组织标准(写出计算过程)。
),测得生成 I2的质量为 0.508mg。请通过计算判断该饮用水中 ClO2的含量是否符合世界卫生组织标准(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】长江水经净化处理,可成为居民的生产生活用水。
(1)水净化时利用活性炭的___________ 性;
(2)生活中常用肥皂水鉴别软水和硬水,证明自来水是软水的现象是___________ 。
(3)世界卫生组织规定饮用水中ClO2剩余量应小于0.2mg/L。取1.5L经ClO2消毒后的饮用水,与足量KI充分反应(原理: ),测得生成I2的质量为0.508mg。请通过计算判断该饮用水中ClO2的含量是否符合世界卫生组织标准(利用化学方程式进行计算)。
),测得生成I2的质量为0.508mg。请通过计算判断该饮用水中ClO2的含量是否符合世界卫生组织标准(利用化学方程式进行计算)。
(1)水净化时利用活性炭的
(2)生活中常用肥皂水鉴别软水和硬水,证明自来水是软水的现象是
(3)世界卫生组织规定饮用水中ClO2剩余量应小于0.2mg/L。取1.5L经ClO2消毒后的饮用水,与足量KI充分反应(原理:
 ),测得生成I2的质量为0.508mg。请通过计算判断该饮用水中ClO2的含量是否符合世界卫生组织标准(利用化学方程式进行计算)。
),测得生成I2的质量为0.508mg。请通过计算判断该饮用水中ClO2的含量是否符合世界卫生组织标准(利用化学方程式进行计算)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】长江水经净化处理,可成为居民的生产生活用水。
(1)水净化时先沉降过滤,后通过活性炭再经消毒处理。其中活性炭的作用是_______ 。
(2)生活中常通过_______ 方法可降低水的硬度,证明自来水是软水的方法是_______ 。
(3)世界卫生组织规定饮用水中ClO2剩余量应小于0.2mg/L。取1.5L经ClO2消毒后的饮用水,与足量KI充分反应(原理:2ClO2+2KI═2KClO2+I2),测得生成I2的质量为0.508mg。请通过计算判断该饮用水中ClO2的含量是否符合世界卫生组织标准(写出计算过程)。
(1)水净化时先沉降过滤,后通过活性炭再经消毒处理。其中活性炭的作用是
(2)生活中常通过
(3)世界卫生组织规定饮用水中ClO2剩余量应小于0.2mg/L。取1.5L经ClO2消毒后的饮用水,与足量KI充分反应(原理:2ClO2+2KI═2KClO2+I2),测得生成I2的质量为0.508mg。请通过计算判断该饮用水中ClO2的含量是否符合世界卫生组织标准(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】往100克含有盐酸和氯化钙的混合溶液中,加入21.2%的碳酸钠溶液,所得溶液的pH变化与加入碳酸钠溶液的质量关系如图,试分析计算:
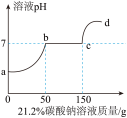
(1)a→b段表示碳酸钠与混合溶液中的 反应;
(2)反应到c点时,所得溶液的溶质质量分数是多少?(写出计算过程,精确到0.1%)

(1)a→b段表示碳酸钠与混合溶液中的 反应;
(2)反应到c点时,所得溶液的溶质质量分数是多少?(写出计算过程,精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】某校实验小组的同学做中和反应实验时,向50g未知浓度的NaOH溶液中逐滴加入7.3%的稀盐酸,当恰好完全反应时,共用去稀盐酸40g。
请完成下列分析及计算:
(1)恰好完全反应时,溶液的pH=___________ 。
(2)实验所用NaOH溶液的溶质质量分数是多少?
请完成下列分析及计算:
(1)恰好完全反应时,溶液的pH=
(2)实验所用NaOH溶液的溶质质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】兴趣小组的同学借助pH传感器测定某氢氧化钠溶液中溶质的质量分数,取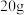 氢氧化钠溶液于烧杯中,逐滴滴加
氢氧化钠溶液于烧杯中,逐滴滴加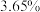 的稀盐酸,并用玻璃棒不断搅拌,实验过程及溶液pH的变化曲线如图所示:
的稀盐酸,并用玻璃棒不断搅拌,实验过程及溶液pH的变化曲线如图所示:______ (用离子符号表示)。
(2)请计算该氢氧化钠溶液的溶质质量分数。
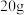 氢氧化钠溶液于烧杯中,逐滴滴加
氢氧化钠溶液于烧杯中,逐滴滴加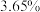 的稀盐酸,并用玻璃棒不断搅拌,实验过程及溶液pH的变化曲线如图所示:
的稀盐酸,并用玻璃棒不断搅拌,实验过程及溶液pH的变化曲线如图所示: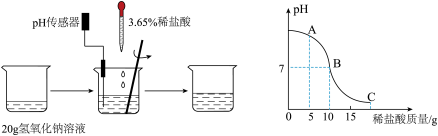
(2)请计算该氢氧化钠溶液的溶质质量分数。
您最近一年使用:0次

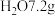 、
、 和CO10g且其中碳元素的质量分数为36%;
和CO10g且其中碳元素的质量分数为36%;

