我国制碱工业的先驱——侯德榜成功地探索和改进了西方的制碱方法。下表为侯氏制碱法中部分物质的溶解度。
(1)由上表可知,在10℃-40℃之间溶解度随温度变化最小的物质是_____ (填名称)。
(2)40℃时,将等质量的三种表中物质的饱和溶液降温至20℃,所得溶液中溶质的质量分数由大到小的顺序是_____ (用化学式表示)。
(3)侯氏制碱法制得的碱为纯碱,纯碱的化学式为_____ 。
(4)制碱原理为向饱和的NaCl溶液中通入足量NH3和CO2生成NaHCO3晶体和NH4Cl,NaHCO3加热分解即制得纯碱。
①生成NaHCO3的化学方程式为_____ 。
②结合上表分析,析出NaHCO3晶体的原因可能有_____ (填序号)。
A 溶剂质量减少
B 同温下NaHCO3溶解度小于NaCl
C 生成的NaHCO3质量大于消耗的NaCl质量
| 温度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度/g | Na2CO3 | 12.2 | 21.8 | 39.7 | 48.8 |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | |
| NaHCO3 | 8.2 | 9.6 | 11.1 | 12.7 | |
(2)40℃时,将等质量的三种表中物质的饱和溶液降温至20℃,所得溶液中溶质的质量分数由大到小的顺序是
(3)侯氏制碱法制得的碱为纯碱,纯碱的化学式为
(4)制碱原理为向饱和的NaCl溶液中通入足量NH3和CO2生成NaHCO3晶体和NH4Cl,NaHCO3加热分解即制得纯碱。
①生成NaHCO3的化学方程式为
②结合上表分析,析出NaHCO3晶体的原因可能有
A 溶剂质量减少
B 同温下NaHCO3溶解度小于NaCl
C 生成的NaHCO3质量大于消耗的NaCl质量
2019·重庆·中考真题 查看更多[6]
重庆市2019年中考(B卷)化学试题(已下线)【万唯原创】2020年河北省中考化学面对面卷练习册九年级第九单元(已下线)主题 溶液·基础必练2(已下线)微专题 溶解度及其应用·满分特训12021年四川省广安市邻水县中考二模化学试题2023年山东省东营市初中学业水平模拟考试化学试题(五)
更新时间:2019-06-17 13:02:00
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】甲、乙两种物质的溶解度曲线如图所示。根据图中信息,回答下列问题:
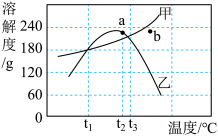
(1)b点状态下的甲溶液属于___________ 溶液。(填“饱和”或“不饱和”)
(2)在t1℃时,将120g乙物质加入到50g水中,充分溶解后恢复到原温度,所得溶液的质量为___________ 。
(3)将t1℃的甲、乙两种物质的饱和溶液分别升温至t2℃时,两溶液溶质的质量分数___________ (填“相等”或“不相等”)。
(4)现有t2℃时甲和乙的饱和溶液(只含两种溶质,且均饱和),若要得到纯净的乙晶体,下列措施可行的是___________。(填写字母标号)
(5)t1℃时,将甲的饱和溶液140g稀释成溶质质量分数为20%的甲溶液,需加入水的质量为___________ g。

(1)b点状态下的甲溶液属于
(2)在t1℃时,将120g乙物质加入到50g水中,充分溶解后恢复到原温度,所得溶液的质量为
(3)将t1℃的甲、乙两种物质的饱和溶液分别升温至t2℃时,两溶液溶质的质量分数
(4)现有t2℃时甲和乙的饱和溶液(只含两种溶质,且均饱和),若要得到纯净的乙晶体,下列措施可行的是___________。(填写字母标号)
| A.降温到t1℃,过滤 |
| B.升温到t3℃,趁热过滤 |
| C.蒸发适量水后,恢复到t2℃,过滤 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】根据右图AB两种物质的溶解度曲线回答下列问题:

(1)t2时,若将120gA 的饱和溶液的质量分数稀释成原溶液质量分数的一半,需加水______________ g
(2)t2℃时AB两种物质的饱和溶液降温至t1℃,所得溶液的溶质的质量分数A________ B(填大于、小于、等于)

(1)t2时,若将120gA 的饱和溶液的质量分数稀释成原溶液质量分数的一半,需加水
(2)t2℃时AB两种物质的饱和溶液降温至t1℃,所得溶液的溶质的质量分数A
您最近一年使用:0次
【推荐1】甲、乙两种固体物质的溶解度曲线如下图所示。
(1)图中P点的含义是____________________________ 。
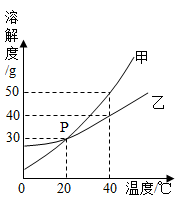
(2)40℃时,饱和溶液中溶质的质量分数:甲____ 乙(填“>”、“=”或“<”)。若将40℃的甲、乙的饱和溶液降温至15℃,则饱和溶液中溶质的质量分数:甲____ 乙(填“>”、“=”或“<”)。20℃时,将60 g乙物质放入100 g水中,升温至40℃,溶液中溶解的溶质与溶剂的质量比为__________ (用最简整数比表示)。
(3)20℃时,进行了如下图所示的实验:
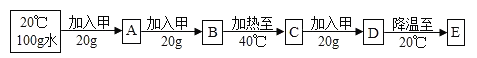
上述实验过程中所得的溶液,属于不饱和溶液的是________ (填序号,下同),________ 溶液与B溶液中溶质的质量分数相同。
(1)图中P点的含义是

(2)40℃时,饱和溶液中溶质的质量分数:甲
(3)20℃时,进行了如下图所示的实验:

上述实验过程中所得的溶液,属于不饱和溶液的是
您最近一年使用:0次
【推荐2】如图是甲、乙、丙三种固体的溶解度曲线,回答下列问题:
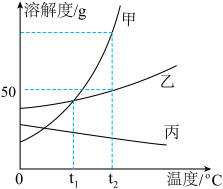
(1)t2℃时,甲的溶解度_______ 乙的溶解度(填“>”、“<”或“=”)。
(2)t2℃时,向50克水中加入50g乙物质,充分溶解后所得溶液的质量是______ 。
(3)t1℃甲、乙、丙的饱和溶液升温到t2℃,所得溶液中溶质质量分数的大小关系为________ (填“>”、“<”或“=”)。
(4)若固体乙中含有少量的甲,可用________ 方法提纯乙。
(5)现有接近饱和的丙物质溶液,使其变成饱和溶液的方法有:
①加入丙物质;②恒温蒸发溶剂;③______ 。

(1)t2℃时,甲的溶解度
(2)t2℃时,向50克水中加入50g乙物质,充分溶解后所得溶液的质量是
(3)t1℃甲、乙、丙的饱和溶液升温到t2℃,所得溶液中溶质质量分数的大小关系为
(4)若固体乙中含有少量的甲,可用
(5)现有接近饱和的丙物质溶液,使其变成饱和溶液的方法有:
①加入丙物质;②恒温蒸发溶剂;③
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】溶液与人们的生产生活密切相关,结合所给图表回答下列问题。
(1)下表所示为氢氧化钠、碳酸钠分别在水、酒精中的溶解度:

①上述图象表示__________________ (填“氢氧化钠”或“碳酸钠”)的溶解度曲线。
②20℃时,氢氧化钠在水中的溶解度____________ (填“大于”或“小于”)碳酸钠在水中的溶解度。
③40℃时,若将 50g NaOH 分别投入 100g 水和 100g 酒精中,能形成饱和溶液的是___________ ,再将 CO2通入所得 NaOH 的酒精溶液中,观察到的现象为________________________ 。
(2)探究 20℃时配制硝酸钾溶液过程中,溶质质量分数与加入水的质量关系。向硝酸钾中分批加水,充分搅拌,现象如下图所示:(已知:20℃时,硝酸钾的溶解度为 31.6g)

该过程中溶质质量分数的变化趋势是______________ 。
(1)下表所示为氢氧化钠、碳酸钠分别在水、酒精中的溶解度:
| 氢氧化钠 | 碳酸钠 | |||
| 20℃ | 40℃ | 20℃ | 40℃ | |
| 水 | 109g | 129g | 21.8g | 49g |
| 酒精 | 17.3g | 40g | 不溶 | 不溶 |

①上述图象表示
②20℃时,氢氧化钠在水中的溶解度
③40℃时,若将 50g NaOH 分别投入 100g 水和 100g 酒精中,能形成饱和溶液的是
(2)探究 20℃时配制硝酸钾溶液过程中,溶质质量分数与加入水的质量关系。向硝酸钾中分批加水,充分搅拌,现象如下图所示:(已知:20℃时,硝酸钾的溶解度为 31.6g)

该过程中溶质质量分数的变化趋势是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】海水是巨大的资源宝库。如图所示利用海水为原料可获得许多化工产品。

(1)要鉴别海水是硬水还是软水,可选用_________________ ;
(2)步骤①中选用蒸发结晶法而不用降温结晶法的理由是________________________ ;
(3)制纯碱过程中,其中过滤操作所需要的玻璃仪器有烧杯、漏斗和_____________ ;
(4)步骤②发生反应的化学方程式是________________ ,其基本反应类型为________ ;
(5)步骤④发生的反应为置换反应(类似于金属与盐溶液之间的反应),试写出该反应的化学方程式________________ 。

(1)要鉴别海水是硬水还是软水,可选用
(2)步骤①中选用蒸发结晶法而不用降温结晶法的理由是
(3)制纯碱过程中,其中过滤操作所需要的玻璃仪器有烧杯、漏斗和
(4)步骤②发生反应的化学方程式是
(5)步骤④发生的反应为置换反应(类似于金属与盐溶液之间的反应),试写出该反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】海洋是人类宝贵的自然资源,海水“制碱”体现了化学科学在改造物质中的智慧。下图是某厂生产纯碱的工艺流程图:

(1)流程I中加入药品的顺序还可以是______ 。
(2)流程I中为了除去杂质,加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液。请分析加入过量的碳酸钠溶液的作用是______ ;过滤后得到的沉淀含______ 种物质。
(3)若在上述制取纯碱的过程中CO2和NH3都是可以循环使用的物质,试写出一种再获得NH3的一个最佳的反应方程式:______ 。
(4)我国化学家侯德榜创立的联合制碱法的优点有______。

(1)流程I中加入药品的顺序还可以是
(2)流程I中为了除去杂质,加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液。请分析加入过量的碳酸钠溶液的作用是
(3)若在上述制取纯碱的过程中CO2和NH3都是可以循环使用的物质,试写出一种再获得NH3的一个最佳的反应方程式:
(4)我国化学家侯德榜创立的联合制碱法的优点有______。
| A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境 |
| B.大大提高了食盐的利用率,节约了成本 |
| C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作复合肥 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐3】材料一:侯德榜是我国著名的化学家,发明了侯氏制碱法,为纯碱和氮肥工业技术的发展作出了杰出的贡献。下面是实验室模拟侯氏制碱法原理的生产过程:

①20℃时,将CO2通入含NH3的饱和NaCl溶液中,生成 NaHCO3晶体和NH4Cl溶液。
②将①中的产物 NaHCO3晶体充分加热分解,得到Na2CO3、H2O和CO2。
材料二:20℃时几种物质在水中的溶解度/g
请回答下列问题:
(1)在第①步反应中,有 NaHCO3晶体析出,而没有NH4Cl和NaCl晶体析出的原因是_____ 。
(2)该生产过程中部分生成物可作为原料循环使用的是_____ ,同时得到的副产品NH4Cl是一种氮肥。

①20℃时,将CO2通入含NH3的饱和NaCl溶液中,生成 NaHCO3晶体和NH4Cl溶液。
②将①中的产物 NaHCO3晶体充分加热分解,得到Na2CO3、H2O和CO2。
材料二:20℃时几种物质在水中的溶解度/g
| NaCl | NH4Cl | NaHCO3 |
| 36.0 | 37.2 | 9.6 |
(1)在第①步反应中,有 NaHCO3晶体析出,而没有NH4Cl和NaCl晶体析出的原因是
(2)该生产过程中部分生成物可作为原料循环使用的是
您最近一年使用:0次




