(1)图1是A、B、C三种固体物质的溶解度曲线,请用“大于”“小于”或“等于”填空。


①t1℃时A物质的溶解度_____ t2℃时A物质的溶解度。
②t2℃时B物质的饱和溶液中溶质的质量分数_____ C物质的饱和溶液中溶质的质量分数。
(2)化学中有许多概念是对立的,又是统一的。图2反映了饱和溶液、不饱和溶液、浓溶液以及稀溶液的关系。
①从图2可以看出,饱和溶液与浓溶液、稀溶液的关系是_____ 。
②0.9%的医用生理盐水可归于图2中_____ 区域(填“Ⅰ”“Ⅱ”“Ⅲ”或“Ⅳ”)


①t1℃时A物质的溶解度
②t2℃时B物质的饱和溶液中溶质的质量分数
(2)化学中有许多概念是对立的,又是统一的。图2反映了饱和溶液、不饱和溶液、浓溶液以及稀溶液的关系。
①从图2可以看出,饱和溶液与浓溶液、稀溶液的关系是
②0.9%的医用生理盐水可归于图2中
更新时间:2019-06-20 00:49:47
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如图1是硝酸钾、氯化钠和图2氢氧化钙固体物质在水中的溶解度曲线,请回答下列问题。
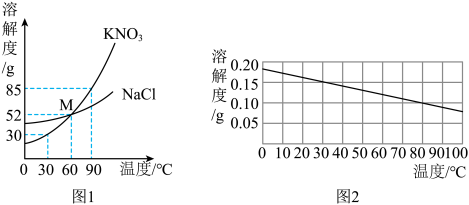
(1)交点M的含义是_______ 。
(2)硝酸钾中含有少量的氯化钠,为了得到纯净的硝酸钾常用的方法是_______ 。
(3)图2中,将接近饱和的氢氧化钙溶液变为饱和溶液,且质量分数不变的方法是_______ 。
(4)图1中,80℃时将45g的硝酸钾加入50g水中,充分溶解,所得溶液的溶质质量分数为_______ 。
(5)图1中,将80℃等质量的硝酸钾和氯化钠的饱和溶液降温至60℃,所得溶液的溶质质量分数关系为_______ 。

(1)交点M的含义是
(2)硝酸钾中含有少量的氯化钠,为了得到纯净的硝酸钾常用的方法是
(3)图2中,将接近饱和的氢氧化钙溶液变为饱和溶液,且质量分数不变的方法是
(4)图1中,80℃时将45g的硝酸钾加入50g水中,充分溶解,所得溶液的溶质质量分数为
(5)图1中,将80℃等质量的硝酸钾和氯化钠的饱和溶液降温至60℃,所得溶液的溶质质量分数关系为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】甲、乙、丙三种固体物质的溶解度曲线如下图所示。
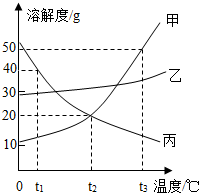
(1)甲的溶解度为20 g时对应的温度为_____________ ;
(2)t3℃时甲、乙饱和溶液中溶质质量分数的大小关系是甲_____ 乙(填“大于”、“小于”或“等于”)。
(3)乙的饱和溶液中含有少量的甲,由该液体得到固体乙采用的方法是_______________ 。
(4)下列说法正确的是____________ 。

(1)甲的溶解度为20 g时对应的温度为
(2)t3℃时甲、乙饱和溶液中溶质质量分数的大小关系是甲
(3)乙的饱和溶液中含有少量的甲,由该液体得到固体乙采用的方法是
(4)下列说法正确的是
| A.从t1℃升温到t3℃,甲、丙的饱和溶液都会析出晶体 |
| B.常温下加水稀释丙的饱和溶液,需要用到的仪器有: 烧杯、玻璃棒、量筒、胶头滴管 |
| C.t2℃乙的饱和溶液中加入固体乙,溶质的质量分数不变 |
| D.t3℃等质量甲、乙、丙的饱和溶液中,含溶质最多的是丙 |
您最近一年使用:0次
【推荐1】请回答下列问题。
(1)根据图中KNO3、NaCI的溶解度曲线,试回答:

①40℃时,KNO3、NaCl两种物质的溶解度大小关系:KNO3_______ NaCl(填“<” “>”或“=”)。
②t℃时,将45gKNO3固体放入50g水中充分溶解,所得溶液的质量为_______ 。
③在不改变溶液质量的情况下,要使一定量接近饱和的KNO3溶液变为饱和溶液的方法是_______ 。
④NaCl溶液中含有少量KNO3,提纯NaCl的方法是_______ 。
(2)回答下列问题:
①沙子是加油站常备灭火用品,其灭火原理是_______ 。
②用汽油能除去衣服上的油污,其除油污的原理为_______ 。
(1)根据图中KNO3、NaCI的溶解度曲线,试回答:

①40℃时,KNO3、NaCl两种物质的溶解度大小关系:KNO3
②t℃时,将45gKNO3固体放入50g水中充分溶解,所得溶液的质量为
③在不改变溶液质量的情况下,要使一定量接近饱和的KNO3溶液变为饱和溶液的方法是
④NaCl溶液中含有少量KNO3,提纯NaCl的方法是
(2)回答下列问题:
①沙子是加油站常备灭火用品,其灭火原理是
②用汽油能除去衣服上的油污,其除油污的原理为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】如图为A、B、C三种固体物质在水中的溶解度曲线,请回答下列问题。
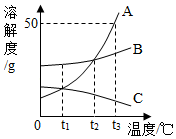
(1)保持溶液质量不变的情况下,将C的不饱和溶液转化为饱和溶液的方法是_____ ;
(2)若B中混有少量A可用_____ 的方法提纯B。
(3)将t3℃时A、B、C三种物质的饱和溶液降温到t1℃,析出晶体最多的是_____ (填数字序号)。
①A ②B ③C ④无法确定
(4)欲将t3℃时A的饱和溶液30g,稀释为10%的溶液需加水_____ g。
(5)分别将t1℃时等质量的A、B、C三种物质的饱和溶液升温至t2℃(忽略水分的蒸发),对所得溶液的叙述不正确的是_____ (填序号)。
①溶剂质量:A=C>B
②溶质质量:A<B
③溶质质量分数:A=B>C
④都是饱和溶液

(1)保持溶液质量不变的情况下,将C的不饱和溶液转化为饱和溶液的方法是
(2)若B中混有少量A可用
(3)将t3℃时A、B、C三种物质的饱和溶液降温到t1℃,析出晶体最多的是
①A ②B ③C ④无法确定
(4)欲将t3℃时A的饱和溶液30g,稀释为10%的溶液需加水
(5)分别将t1℃时等质量的A、B、C三种物质的饱和溶液升温至t2℃(忽略水分的蒸发),对所得溶液的叙述不正确的是
①溶剂质量:A=C>B
②溶质质量:A<B
③溶质质量分数:A=B>C
④都是饱和溶液
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】请根据如图a、b、c三种固体物质的溶解度曲线,回答下列问题:

(1)点P的表示的意义是_____ 。
(2)a、b两种物质,溶解度随温度升高而变大,其中受温度影响溶解度变化趋势比较大的是_____ (填“a”或“b”)。
(3)将c物质的饱和溶液变为不饱和溶液,可以用到的方法是_____ 。(填序号)①升温 ②降温 ③增加溶质 ④减少溶剂 ⑤增加溶剂
(4)在t2℃时,向盛有50g a物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为_____ g。
(5)取t2℃时三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是_____ 。

(1)点P的表示的意义是
(2)a、b两种物质,溶解度随温度升高而变大,其中受温度影响溶解度变化趋势比较大的是
(3)将c物质的饱和溶液变为不饱和溶液,可以用到的方法是
(4)在t2℃时,向盛有50g a物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为
(5)取t2℃时三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是
您最近一年使用:0次
【推荐1】某实验室欲配制一定溶质质量分数的KNO3溶液,现实验室只有含少量NaCl的KNO3固体药品。如图所示,回答下列问题。
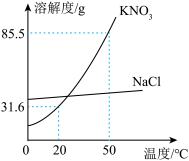
(1)如图所示50℃时,将85.5g固体药品溶于100g水中,得到的是KNO3的______ 溶液(填“饱和”或“不饱和”)。
(2)提纯KNO3的方法是______ 。
(3)小明用提纯后的KNO3固体配制100g溶质质量分数为5%的KNO3溶液,经检测,所配溶液中KNO3溶质质量分数偏大,其原因可能是______ 。
①KNO3固体仍然不纯;
②溶解前,烧杯中有水;
③量取水时,俯视读数;
④装瓶时,有少量溶液洒出。

(1)如图所示50℃时,将85.5g固体药品溶于100g水中,得到的是KNO3的
(2)提纯KNO3的方法是
(3)小明用提纯后的KNO3固体配制100g溶质质量分数为5%的KNO3溶液,经检测,所配溶液中KNO3溶质质量分数偏大,其原因可能是
①KNO3固体仍然不纯;
②溶解前,烧杯中有水;
③量取水时,俯视读数;
④装瓶时,有少量溶液洒出。
您最近一年使用:0次
【推荐2】水和溶液与人们的生活息息相关。
(1)自来水厂净水过程为:天然水→加絮凝剂→沉降→过滤→吸附→加消毒剂→自来水,其中通常用作絮凝剂的物质是___________ 。
(2)电解水的过程如图1,通电一段时间后,a玻璃管内产生的气体为___________ 。

(3)如图2是NaCl、KNO3的溶解度曲线。

①在60℃时,分别取 Xg NaCl和KNO3固体进行如图的实验。加入甲烧杯中的固体是___________ (填“NaCl”或“KNO3”),X的取值范围是___________ 。
②下列说法错误的是___________ 。
A.状态1时,甲烧杯为饱和溶液,乙烧杯为不饱和溶液
B.若采用某操作使甲中固体全部溶解,则溶液中溶质质量分数一定增大
C.乙烧杯在状态2时的溶质质量分数是状态1时的2倍
D.若将状态1时的甲、乙烧杯溶液降温至10℃,所得溶液溶质质量分数甲>乙
(1)自来水厂净水过程为:天然水→加絮凝剂→沉降→过滤→吸附→加消毒剂→自来水,其中通常用作絮凝剂的物质是
(2)电解水的过程如图1,通电一段时间后,a玻璃管内产生的气体为

(3)如图2是NaCl、KNO3的溶解度曲线。

①在60℃时,分别取 Xg NaCl和KNO3固体进行如图的实验。加入甲烧杯中的固体是
②下列说法错误的是
A.状态1时,甲烧杯为饱和溶液,乙烧杯为不饱和溶液
B.若采用某操作使甲中固体全部溶解,则溶液中溶质质量分数一定增大
C.乙烧杯在状态2时的溶质质量分数是状态1时的2倍
D.若将状态1时的甲、乙烧杯溶液降温至10℃,所得溶液溶质质量分数甲>乙
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】A、B、C三种固体物质的溶解度曲线如图所示,据图回答问题:

(1)温度为_____ ℃时,A与C物质的溶解度相等。
(2)将t1℃时A、B、C三种物质的饱和溶液升温到t2℃,有晶体析出的是_____ (填字母代号)。
(3)t2℃时,把A、B物质各50g分别加到100g水中,不能形成饱和溶液的是_____ (填字母代号),若要使之达到饱和状态,还需要向溶液中加入_____ g该溶质。
(4)现将t1℃时A、B的饱和溶液同时升温至t3℃(不考虑水的蒸发),则此时A、B两溶液溶质质量分数的大小关系为A_____ B(填“>”、“=”或“<”)。
(5)现有t2℃时B的溶液100g,将其蒸发掉10g水,再将温度恢复到t2℃时析出3gB,若继续蒸发掉10g水,仍将温度恢复到t2℃,此时析出B的质量_____ 3g(填“>”、“=”或“≥”)。
(6)当A中混有少量B时,提纯A采用的方法是_____ (填“蒸发结晶”或“降温结晶”)。
(7)现用提纯后的A配制一定溶质质量分数的溶液,实验中用到的玻璃仪器除了烧杯、玻璃棒、胶头滴管和试剂瓶外,还需要_____ 。

(1)温度为
(2)将t1℃时A、B、C三种物质的饱和溶液升温到t2℃,有晶体析出的是
(3)t2℃时,把A、B物质各50g分别加到100g水中,不能形成饱和溶液的是
(4)现将t1℃时A、B的饱和溶液同时升温至t3℃(不考虑水的蒸发),则此时A、B两溶液溶质质量分数的大小关系为A
(5)现有t2℃时B的溶液100g,将其蒸发掉10g水,再将温度恢复到t2℃时析出3gB,若继续蒸发掉10g水,仍将温度恢复到t2℃,此时析出B的质量
(6)当A中混有少量B时,提纯A采用的方法是
(7)现用提纯后的A配制一定溶质质量分数的溶液,实验中用到的玻璃仪器除了烧杯、玻璃棒、胶头滴管和试剂瓶外,还需要
您最近一年使用:0次




