如图为A、B、C三种固体物质在水中的溶解度曲线,请回答下列问题。
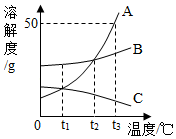
(1)保持溶液质量不变的情况下,将C的不饱和溶液转化为饱和溶液的方法是_____ ;
(2)若B中混有少量A可用_____ 的方法提纯B。
(3)将t3℃时A、B、C三种物质的饱和溶液降温到t1℃,析出晶体最多的是_____ (填数字序号)。
①A ②B ③C ④无法确定
(4)欲将t3℃时A的饱和溶液30g,稀释为10%的溶液需加水_____ g。
(5)分别将t1℃时等质量的A、B、C三种物质的饱和溶液升温至t2℃(忽略水分的蒸发),对所得溶液的叙述不正确的是_____ (填序号)。
①溶剂质量:A=C>B
②溶质质量:A<B
③溶质质量分数:A=B>C
④都是饱和溶液

(1)保持溶液质量不变的情况下,将C的不饱和溶液转化为饱和溶液的方法是
(2)若B中混有少量A可用
(3)将t3℃时A、B、C三种物质的饱和溶液降温到t1℃,析出晶体最多的是
①A ②B ③C ④无法确定
(4)欲将t3℃时A的饱和溶液30g,稀释为10%的溶液需加水
(5)分别将t1℃时等质量的A、B、C三种物质的饱和溶液升温至t2℃(忽略水分的蒸发),对所得溶液的叙述不正确的是
①溶剂质量:A=C>B
②溶质质量:A<B
③溶质质量分数:A=B>C
④都是饱和溶液
更新时间:2023-12-06 13:17:43
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示。请回答:

(1)t1℃时,将30g丙溶于水配制成饱和溶液,需水的质量为______ g。配制该溶液时所需玻璃仪器有烧杯、玻璃棒、量筒和______ 。
(2)甲固体中含有少量乙,可采用的______ 方法提纯甲。
(3)已知R是甲、乙、丙三种物质中的一种。现用R做如图实验,①②中没有固体析出,③中有固体析出。根据图示信息,以下说法一定正确的是______ 。

AR是甲物质
B①②③中,只有③的上层清液是饱和溶液
C①和②的溶液中,溶质质量相等
D①的溶液中溶质的质量分数比③的上层清液中溶质的质量分数小

(1)t1℃时,将30g丙溶于水配制成饱和溶液,需水的质量为
(2)甲固体中含有少量乙,可采用的
(3)已知R是甲、乙、丙三种物质中的一种。现用R做如图实验,①②中没有固体析出,③中有固体析出。根据图示信息,以下说法一定正确的是

AR是甲物质
B①②③中,只有③的上层清液是饱和溶液
C①和②的溶液中,溶质质量相等
D①的溶液中溶质的质量分数比③的上层清液中溶质的质量分数小
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】海水中含有氯化钠、氯化钙等物质,下面是从海水中提取氯化钠的大致过程(如图1)和氯化钠、氯化钙的溶解度表与溶解度曲线。
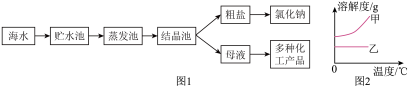
请回答下列问题:
(1)将粗盐从海水中结晶出来的方法是_____ 。
(2)经长时间日晒,氯化钙也不易大量结晶析出的原因是_____ ,40℃时,50g水中最多溶解氯化钙_____ g。
(3)根据海水晒盐的原理,下列说法中正确的是_____ (填序号)。
A 海水进入贮水池,海水的成分基本不变
B 在蒸发池里,海水中水的质量逐渐增加
C 析出晶体后的母液是氯化钠的不饱和溶液
(4)如图2溶解度曲线图中,能表示氯化钙溶解度曲线的是_____ (填“甲”或“乙”)。

| 温度/C | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 128 | |
(1)将粗盐从海水中结晶出来的方法是
(2)经长时间日晒,氯化钙也不易大量结晶析出的原因是
(3)根据海水晒盐的原理,下列说法中正确的是
A 海水进入贮水池,海水的成分基本不变
B 在蒸发池里,海水中水的质量逐渐增加
C 析出晶体后的母液是氯化钠的不饱和溶液
(4)如图2溶解度曲线图中,能表示氯化钙溶解度曲线的是
您最近一年使用:0次
【推荐3】图为A、B、C三种固体物质的溶解度曲线,根据曲线图回答下列题。

(1)t1℃时,溶解度最大的物质是___________ 。
(2)B、C两种物质的溶解度相等时,温度为___________ ℃;
(3)t3℃时,将A、B两种物质相同质量的饱和溶液,分别降温至t1℃,析出晶体较多的是___________ 物质。
(4)若将M点处C的不饱和溶液变为饱和溶液,可以选择的方法是___________ (填序号)。
①降低温度②增加溶质③蒸发溶剂
(5)将t2℃时的A、B、C三种物质的饱和溶液升温至t3℃,所得溶液中溶质的质量分数的大小关系是___________ (填“<”、“=”或“>”)。

(1)t1℃时,溶解度最大的物质是
(2)B、C两种物质的溶解度相等时,温度为
(3)t3℃时,将A、B两种物质相同质量的饱和溶液,分别降温至t1℃,析出晶体较多的是
(4)若将M点处C的不饱和溶液变为饱和溶液,可以选择的方法是
①降低温度②增加溶质③蒸发溶剂
(5)将t2℃时的A、B、C三种物质的饱和溶液升温至t3℃,所得溶液中溶质的质量分数的大小关系是
您最近一年使用:0次
【推荐1】水是生命之源,孕育万物,没有水就没有生命。
(1)家用净水器的滤芯主要成分是活性炭,是利用其___________ 。
(2)20℃,将固体物质X溶于水并进行如下实验,如图所示。回答下列问题。根据图1判断,物质X的溶解度随温度的变化关系是___________

(3)20℃,物质X溶于不同质量的水中,溶液达到饱和状态时,溶质质量与水的质量关系如图2所示。
①20℃时,属于饱和溶液的是___________ ;
②A、B、C、D点对应的溶液中溶质质量分数由大到小的关系是___________ ;
③20℃时,将X溶液从A状态转化为C状态的一种方法___________ 。
(1)家用净水器的滤芯主要成分是活性炭,是利用其
(2)20℃,将固体物质X溶于水并进行如下实验,如图所示。回答下列问题。根据图1判断,物质X的溶解度随温度的变化关系是

(3)20℃,物质X溶于不同质量的水中,溶液达到饱和状态时,溶质质量与水的质量关系如图2所示。
①20℃时,属于饱和溶液的是
②A、B、C、D点对应的溶液中溶质质量分数由大到小的关系是
③20℃时,将X溶液从A状态转化为C状态的一种方法
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】水是生命之源,是地球上最普遍、最常见的物质之一。

(1)图 1 中的陆地淡水属于_______ (填“纯净物”或“混合物”)。除去海水中难溶性杂质的操作是_______ 。
(2)图 2 中水发生的是_______ (填“物理”或“化学”)变化。
(3)用燃着的木条检验图 3 试管 b 内气体,观察到的现象是_______ 。电解水的化学方程式为_______ ;在此反应过程中没有发生变化的微粒是_______ (填符号)。
(4)甲、乙两种固体的溶解度曲线如图一所示:

①t1℃时,乙的溶解度是 40g。这句话的含义是_______ 。
②t2℃时,配制 90g 甲物质的饱和溶液,需称量甲的质量_______ g。
③由图二推测硝酸钾是图一中的_______ (填“甲”或“乙”)物质。
④图二操作Ⅱ前后的溶液状态变化过程,可以在图一中表示为_______ (填字母)。
A c 点→a 点 B c 点→b 点 C c 点→d 点 D b 点→a 点

(1)图 1 中的陆地淡水属于
(2)图 2 中水发生的是
(3)用燃着的木条检验图 3 试管 b 内气体,观察到的现象是
(4)甲、乙两种固体的溶解度曲线如图一所示:

①t1℃时,乙的溶解度是 40g。这句话的含义是
②t2℃时,配制 90g 甲物质的饱和溶液,需称量甲的质量
③由图二推测硝酸钾是图一中的
④图二操作Ⅱ前后的溶液状态变化过程,可以在图一中表示为
A c 点→a 点 B c 点→b 点 C c 点→d 点 D b 点→a 点
您最近一年使用:0次
【推荐3】如图是A、B、C三种固体物质的溶解度曲线。

(1)点P表示___________________________________ 。
(2)当温度为t2℃时,A、B、C三种物质的溶解度由小到大的顺序_________________________ 。
(3)要使接近饱和的C物质溶液变为饱和溶液,可采取的一种措施是________________________ 。
(4)t2℃时,A物质的饱和溶液150g降温到t1℃析出A物质_________________ g(不含结晶水)。
(5)将t2℃时A、B、C三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数由大到小的顺序为_________________________ 。
(6)当A中含有少量B时,为了得到纯净的A,可采用____________________ 的方法。

(1)点P表示
(2)当温度为t2℃时,A、B、C三种物质的溶解度由小到大的顺序
(3)要使接近饱和的C物质溶液变为饱和溶液,可采取的一种措施是
(4)t2℃时,A物质的饱和溶液150g降温到t1℃析出A物质
(5)将t2℃时A、B、C三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质量分数由大到小的顺序为
(6)当A中含有少量B时,为了得到纯净的A,可采用
您最近一年使用:0次
【推荐1】a、b、c三种物质的溶解度曲线如图1所示,请结合图示回答下列问题:

(1)P点的含义是______________
(2)若图2试管中为b物质的饱和溶液,则固体X放入水中会_________ (填“吸热”或“放热”)
(3)t3℃时,将50克的a物质放入50克水中形成_______ 溶液(填“饱和”或“不饱和”),此时溶液的溶质质量分数为_______ 。(保留至0.1%)
(4)当a中混入少量b,可采用_________ 提纯a物质。若将c的饱和溶液转化为不饱和溶液可采用_________ 、___________ 。

(1)P点的含义是
(2)若图2试管中为b物质的饱和溶液,则固体X放入水中会
(3)t3℃时,将50克的a物质放入50克水中形成
(4)当a中混入少量b,可采用
您最近一年使用:0次
【推荐2】下图是甲、乙、丙三种物质的溶解度曲线,回答下列问题:
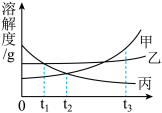
(1)乙物质的溶解度受温度影响变化___________ ;
(2)t3℃时,甲、乙、丙三种物质的溶解度从大到小的排列顺序是_____________ ;
(3)将丙物质的饱和溶液变成不饱和溶液除增加溶剂外还能用_________ 方法;
(4)t2℃时,甲和丙物质的饱和溶液各100g,其溶质的质量,甲______ 丙(填“>”、“<”或“=”)。

(1)乙物质的溶解度受温度影响变化
(2)t3℃时,甲、乙、丙三种物质的溶解度从大到小的排列顺序是
(3)将丙物质的饱和溶液变成不饱和溶液除增加溶剂外还能用
(4)t2℃时,甲和丙物质的饱和溶液各100g,其溶质的质量,甲
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】如图是A、B、C三种固体物质的溶解度曲线,请回答。

(1)50℃时,A物质的饱和溶液中,溶质与溶液的质量比为______ (填最简整数比)。
(2)若B中混有少量的A,提纯B可采取的方法是______ 。
(3)使C物质的饱和溶液溶质质量分数增大方法的是______ 。
(4)50℃时,将A、B、C的饱和溶液分别降温至20℃,对所得溶液叙述正确的是______ (填序号)。
AA、B、C均为饱和溶液 B溶液质量:C>B>A
C溶质质量分数:B>A>C D溶剂质量:A>B>C

(1)50℃时,A物质的饱和溶液中,溶质与溶液的质量比为
(2)若B中混有少量的A,提纯B可采取的方法是
(3)使C物质的饱和溶液溶质质量分数增大方法的是
(4)50℃时,将A、B、C的饱和溶液分别降温至20℃,对所得溶液叙述正确的是
AA、B、C均为饱和溶液 B溶液质量:C>B>A
C溶质质量分数:B>A>C D溶剂质量:A>B>C
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】赣州经开区引进的单体投资规模最大的工业项目吉利(赣州)动力电池一期项目预计将在今年四月份全线投产,届时新能源汽车将更快地走进我们的生活。制造新能源汽车的常用材料有塑料、玻璃钢、工业陶瓷、橡胶、皮革、铝合金、合成纤维等。与传统汽车使用化石燃料不同,新能源汽车的能量来源更加多元化。目前新能源汽车主要有纯电动汽车、乙醇汽车、氢动力汽车等几类。
(1)上述涉及的材料中,属于金属材料的有______ 。
(2)生活中初步鉴别合成纤维和羊毛的简单方法是______ 。
(3)新能源汽车的车架表面喷漆不仅美观,而且可有效防止其与空气中的______ 接触而生锈。
(4)氢动力汽车使用的氢气可以通过电解水制取,请写出电解水的化学方程式为:______ 。
(5)市场上部分电动车会装配铅酸电池,它是一种电极主要由铅及其氧化物制成,电解液是硫酸溶液的蓄电池。现某工厂生产一批铅酸电池,需要质量分数为30%的硫酸溶液980kg,通过稀释质量分数为98%浓硫酸得到,则需要浓硫酸的质量为______ kg。
(1)上述涉及的材料中,属于金属材料的有
(2)生活中初步鉴别合成纤维和羊毛的简单方法是
(3)新能源汽车的车架表面喷漆不仅美观,而且可有效防止其与空气中的
(4)氢动力汽车使用的氢气可以通过电解水制取,请写出电解水的化学方程式为:
(5)市场上部分电动车会装配铅酸电池,它是一种电极主要由铅及其氧化物制成,电解液是硫酸溶液的蓄电池。现某工厂生产一批铅酸电池,需要质量分数为30%的硫酸溶液980kg,通过稀释质量分数为98%浓硫酸得到,则需要浓硫酸的质量为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请按要求回答下列问题:
(1)自然界中的水都是混合物,通过多种途径可以使水得到不同程度的净化。活性炭具有良好的____ 性,可以滤去水中一些不溶性和可溶性杂质。在图1和图2示意的净水原理中,能明显降低水的硬度的净水方法是____ 。(填“图1”或“图2”)
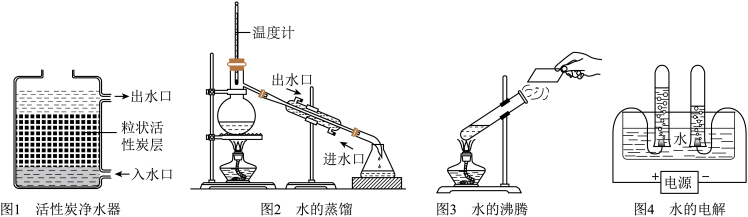
(2)水是一种化学资源,保持水的化学性质的最小微粒是_______ 。
(3)水在自然界的物质循环中起着至关重要的作用。
①水参加植物光合作用的化学方程式为:6CO2+6H2O 6O2+X,则X的化学式:
6O2+X,则X的化学式:____ 。
②电解水可以产生氢气。氢气作为未来最理想的能源,主要优点是_____ 。上图4是水的电解装置,氢气在与电源_____ 极相连的玻璃管内放出。
③在图3和图4所示的水的两种变化中,其微观本质区别在于_____ 。
(4)小明用已配制好的质量分数为6%的氯化钠溶液(密度约为1.04g/cm3),配制50g质量分数为3%的氯化钠溶液。①配制步骤为:计算、量取、_______ 、装瓶贴标签。
②需要6%的氯化钠溶液_______ mL。(结果取整数)
(1)自然界中的水都是混合物,通过多种途径可以使水得到不同程度的净化。活性炭具有良好的

(2)水是一种化学资源,保持水的化学性质的最小微粒是
(3)水在自然界的物质循环中起着至关重要的作用。
①水参加植物光合作用的化学方程式为:6CO2+6H2O
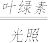 6O2+X,则X的化学式:
6O2+X,则X的化学式:②电解水可以产生氢气。氢气作为未来最理想的能源,主要优点是
③在图3和图4所示的水的两种变化中,其微观本质区别在于
(4)小明用已配制好的质量分数为6%的氯化钠溶液(密度约为1.04g/cm3),配制50g质量分数为3%的氯化钠溶液。①配制步骤为:计算、量取、
②需要6%的氯化钠溶液
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】水和双氧水在生活中都有重要的用途。
(1)水是人体必需的营养素。
①净水方法中,常用______ 吸附水的异味,常用______ 方法将硬水变为软水。
②日常生活中必须爱护水资源,写出保护水资源的一种措施:______ 。
(2)双氧水常用作消毒剂。
①双氧水需阴凉避光保存,用化学方程式解释其原因:______ 。
②双氧水溶液的溶剂是______ 。
③配制100g6%的双氧水,需要30%的双氧水的质量是______ g。用量筒量取30%的双氧水时,仰视读数,会造成所配制溶液的浓度______ (选填“偏大”“偏小”或“不变”)。
(3)水与过氧化氢性质不同的本质原因是______ 。
(1)水是人体必需的营养素。
①净水方法中,常用
②日常生活中必须爱护水资源,写出保护水资源的一种措施:
(2)双氧水常用作消毒剂。
①双氧水需阴凉避光保存,用化学方程式解释其原因:
②双氧水溶液的溶剂是
③配制100g6%的双氧水,需要30%的双氧水的质量是
(3)水与过氧化氢性质不同的本质原因是
您最近一年使用:0次



