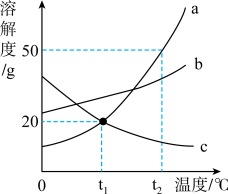
海水中含有氯化钠、氯化钙等物质,下面是从海水中提取氯化钠的大致过程(如图1)和氯化钠、氯化钙的溶解度表与溶解度曲线。
请回答下列问题:
(1)将粗盐从海水中结晶出来的方法是_____ 。
(2)经长时间日晒,氯化钙也不易大量结晶析出的原因是_____ ,40℃时,50g水中最多溶解氯化钙_____ g。
(3)根据海水晒盐的原理,下列说法中正确的是_____ (填序号)。
A 海水进入贮水池,海水的成分基本不变
B 在蒸发池里,海水中水的质量逐渐增加
C 析出晶体后的母液是氯化钠的不饱和溶液
(4)如图2溶解度曲线图中,能表示氯化钙溶解度曲线的是_____ (填“甲”或“乙”)。

| 温度/C | 0 | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| 氯化钙 | 59.5 | 65.0 | 74.5 | 100 | 128 | |
(1)将粗盐从海水中结晶出来的方法是
(2)经长时间日晒,氯化钙也不易大量结晶析出的原因是
(3)根据海水晒盐的原理,下列说法中正确的是
A 海水进入贮水池,海水的成分基本不变
B 在蒸发池里,海水中水的质量逐渐增加
C 析出晶体后的母液是氯化钠的不饱和溶液
(4)如图2溶解度曲线图中,能表示氯化钙溶解度曲线的是
20-21九年级下·全国·课时练习 查看更多[2]
更新时间:2021-01-04 00:15:34
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】一些物质的溶解度曲线如图所示,回答下列问题:
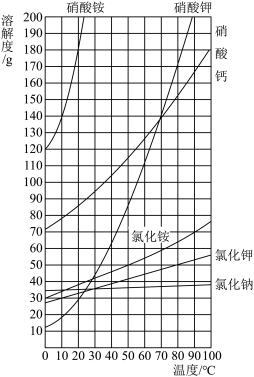
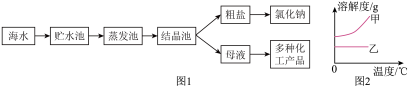
(1)70℃时,在100g水中加入110g硝酸钾固体,所形成的溶液是________________ (填“饱和”或“不饱和”)溶液。
(2)将上述溶液降温到10℃时,析出晶体的质量是________________ g,所得溶液中溶质质量分数为________________ 。
(3)工业上将硝酸钾和氯化钠的热混合溶液(两者均已达到饱和)冷却至室温,析出晶体:
①析出的晶体中主要物质是________________ ;
②关于剩余溶液,下列说法正确的是________________ (填字母序号)。
A只含氯化钠,不含硝酸钾,且氯化钠达到饱和
B.含有氯化钠,又含有硝酸钾,且只有氯化钠达到饱和
C.含有氯化钠,又含有硝酸钾,且两者都达到饱和
(4)剩余溶液中溶质的质量分数:氯化钠________________ (填“大于”“小于”或“等于”)硝酸钾。

(1)70℃时,在100g水中加入110g硝酸钾固体,所形成的溶液是
(2)将上述溶液降温到10℃时,析出晶体的质量是
(3)工业上将硝酸钾和氯化钠的热混合溶液(两者均已达到饱和)冷却至室温,析出晶体:
①析出的晶体中主要物质是
②关于剩余溶液,下列说法正确的是
A只含氯化钠,不含硝酸钾,且氯化钠达到饱和
B.含有氯化钠,又含有硝酸钾,且只有氯化钠达到饱和
C.含有氯化钠,又含有硝酸钾,且两者都达到饱和
(4)剩余溶液中溶质的质量分数:氯化钠
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是氧化沉淀法生产复印用高档Fe3O4粉的工艺流程简图,根据要求回答问题。

(1)加水溶解过程中,在实验室里通常要使用的玻璃仪器有烧杯和_________ 。
(2)副产品P是_______ ,由溶液N获得该副产品的操作顺序是b→_______ →_______ →d。
a、过滤 b、加热浓缩 c、冷却结晶 d、晶体加热至完全失去结晶水
(3)通空气时的化学方程式是4Fe(OH)2+2H2O+O2=4Fe(OH)3,由沉淀M获得Fe3O4的过程中发生的反应为 ,控制“一定量空气”的目的是
,控制“一定量空气”的目的是_______ ,沉淀M中Fe(OH)2和Fe(OH)3的最佳质量比为_______ 。

(1)加水溶解过程中,在实验室里通常要使用的玻璃仪器有烧杯和
(2)副产品P是
a、过滤 b、加热浓缩 c、冷却结晶 d、晶体加热至完全失去结晶水
(3)通空气时的化学方程式是4Fe(OH)2+2H2O+O2=4Fe(OH)3,由沉淀M获得Fe3O4的过程中发生的反应为
 ,控制“一定量空气”的目的是
,控制“一定量空气”的目的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】水和溶液在生产、生活中起着十分重要的作用,请回答下列问题。
(1)氢氧化钙的溶解度随温度升高而减小。要想把一瓶接近饱和的石灰水变成饱和溶液,具体措施有:①加入氢氧化钙;②加入氧化钙;③加入水;④蒸发水;⑤升高温度;⑥降低温度。以上方法中,能达到目的的是______ (选填数字序号)。
(2)向装有等量水的A、B、C 烧杯中分别加入10g、25g、25g NaNO3固体,充分溶解后,现象如图一所示。
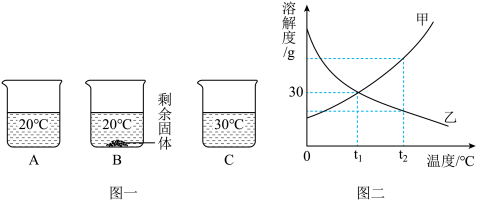
①烧杯中的溶液一定属于饱和溶液的是______ (填字母序号)。
②图二中能表示NaNO3溶解度曲线的是______ (选填“甲”或“乙”)。
③由图二分析,若分别将100g甲、乙的饱和溶液从t2 ℃降温到t1 ℃,对所得溶液的叙述正确的是______ (填序号)。
A.甲、乙都是饱和溶液
B.溶液质量:甲<乙
C.所含溶剂质量:甲>乙
D.溶质质量分数:甲=乙
④t1℃时NaNO3饱和溶液中溶质质量分数为______ 。
(1)氢氧化钙的溶解度随温度升高而减小。要想把一瓶接近饱和的石灰水变成饱和溶液,具体措施有:①加入氢氧化钙;②加入氧化钙;③加入水;④蒸发水;⑤升高温度;⑥降低温度。以上方法中,能达到目的的是
(2)向装有等量水的A、B、C 烧杯中分别加入10g、25g、25g NaNO3固体,充分溶解后,现象如图一所示。

①烧杯中的溶液一定属于饱和溶液的是
②图二中能表示NaNO3溶解度曲线的是
③由图二分析,若分别将100g甲、乙的饱和溶液从t2 ℃降温到t1 ℃,对所得溶液的叙述正确的是
A.甲、乙都是饱和溶液
B.溶液质量:甲<乙
C.所含溶剂质量:甲>乙
D.溶质质量分数:甲=乙
④t1℃时NaNO3饱和溶液中溶质质量分数为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】水是人类宝贵的自然资源。
(1)天然水中含有许多杂质,实验室常用过滤方法除去水中不溶性杂质,过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和__ (填仪器名称)。
(2)硬水给生活和生产带来很多麻烦,生活中常用___ 的方法降低水的硬度。
(3)在电解水的实验中,两电极相连的玻璃管上方产生的气体是氧气和氢气,一段时间后,氧气和氢气的体积比约为___ ;该过程的化学方程式为__________________ 。
(4)甲和乙两种固体物质的溶解度曲线如图所示
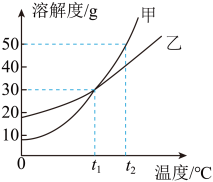
①t1℃时,甲和乙的溶解度____ (填“相等”或“不相等”)。
②t2℃时,甲和乙的饱和溶液各100g,两种溶液中溶剂的质量大小关系为:甲___ 乙(填“>”、“=”或“<”)。
③将t2℃时150g甲的饱和溶液降温至t1℃,所得溶液中溶质的质量分数为___ (计算结果精确到0.1%)。
(1)天然水中含有许多杂质,实验室常用过滤方法除去水中不溶性杂质,过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和
(2)硬水给生活和生产带来很多麻烦,生活中常用
(3)在电解水的实验中,两电极相连的玻璃管上方产生的气体是氧气和氢气,一段时间后,氧气和氢气的体积比约为
(4)甲和乙两种固体物质的溶解度曲线如图所示

①t1℃时,甲和乙的溶解度
②t2℃时,甲和乙的饱和溶液各100g,两种溶液中溶剂的质量大小关系为:甲
③将t2℃时150g甲的饱和溶液降温至t1℃,所得溶液中溶质的质量分数为
您最近一年使用:0次
【推荐3】水与人类的生活和生产密切相关,请回答下列问题:
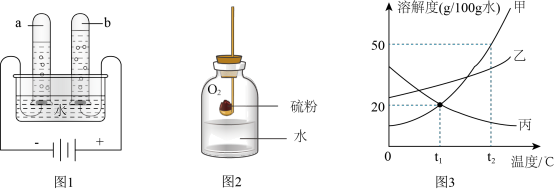
(1)图1是水通电分解的示意图,在实验过程中,观察到a、b两支试管中产生的气体的体积比为________ 。
(2)图2实验中的实验现象是________________________________________ ;实验结束后,用pH试纸测集气瓶中的液体,其pH________ (填“小于”“等于”或“大于”)7。
(3)图3为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线。
①t1 ℃时,甲物质的溶解度为________ g;此温度时甲物质的溶解度________ (填“>”“=”或“<”)乙物质的溶解度。
②将t2 ℃时接近饱和的丙溶液变成饱和溶液,下列方法不能达到目的的是( )
A.蒸发溶剂 B.降低温度
C.加溶质丙 D.升高温度
③将等质量甲、乙的饱和溶液从t2 ℃降温到t1 ℃,对所得溶液的叙述正确的是( )
A.都是饱和溶液
B.溶液质量:甲=乙
C.溶质质量分数:甲>乙
D.溶剂质量:甲>乙
(4)将100 g 8%的氢氧化钠溶液通电一段时间后,氢氧化钠溶液的质量分数变为10%,求生成的氢气的质量____________ (写出计算过程)。

(1)图1是水通电分解的示意图,在实验过程中,观察到a、b两支试管中产生的气体的体积比为
(2)图2实验中的实验现象是
(3)图3为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线。
①t1 ℃时,甲物质的溶解度为
②将t2 ℃时接近饱和的丙溶液变成饱和溶液,下列方法不能达到目的的是
A.蒸发溶剂 B.降低温度
C.加溶质丙 D.升高温度
③将等质量甲、乙的饱和溶液从t2 ℃降温到t1 ℃,对所得溶液的叙述正确的是
A.都是饱和溶液
B.溶液质量:甲=乙
C.溶质质量分数:甲>乙
D.溶剂质量:甲>乙
(4)将100 g 8%的氢氧化钠溶液通电一段时间后,氢氧化钠溶液的质量分数变为10%,求生成的氢气的质量
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
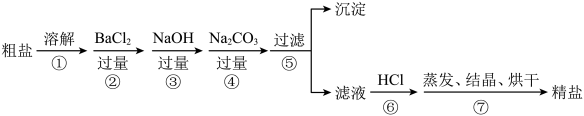
在第①步粗盐溶解操作中要用_____________ 搅拌,作用是_______________ 。
(2)第②步操作的目的是除去粗盐中的____________ (填化学式,下同),第⑥步操作的目的是除去滤液中的______________________ 。
(3)第②步与第④步不能颠倒顺序,理由是_________________ 。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是_________________ 。
(5)实验所得精盐质量_________ 粗盐中氯化钠质量(选填“大于”、“小于”或“等于”)。

在第①步粗盐溶解操作中要用
(2)第②步操作的目的是除去粗盐中的
(3)第②步与第④步不能颠倒顺序,理由是
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是
(5)实验所得精盐质量
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐2】卓筒井是手工制盐的活化石,发明于北宋庆历年间,比西方早800多年。卓筒井手工制盐的工艺流程如下。_________ (选填“Ⅱ”、“Ⅲ”或“Ⅳ”)之后;结合该工艺流程分析“晒卤”的目的是____________ (写一点)。
(2)下表是氯化钠和氯化钾固体在不同温度时的溶解度。分析表中数据回答下列问题。
①40℃时,将100g水加入盛有50g氯化钠的烧杯中,充分溶解后,得到氯化钠溶液的溶质质量分数为__________________ (列式即可)。保持温度不变,再加入10g水,充分搅拌后,氯化钠溶液的溶质质量分数_________ (填“变大”、“变小”或“不变”)。
②氯化钠与氯化钾溶解度相同的最小温度范围是_________ 。
③20℃时,100g卤水中氯化钠的质量分数为9%,含氯化钾1.00g,蒸发掉水大于_________ g,开始有氯化钠析出。
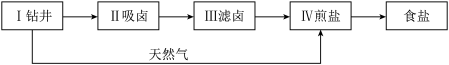
(2)下表是氯化钠和氯化钾固体在不同温度时的溶解度。分析表中数据回答下列问题。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 |
氯化钠溶解度/g | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
氯化钾溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |
②氯化钠与氯化钾溶解度相同的最小温度范围是
③20℃时,100g卤水中氯化钠的质量分数为9%,含氯化钾1.00g,蒸发掉水大于
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】联合国第63届大会的主题是“化学—人类的生活,人类的未来”,生活中“衣”,“食”、“住”、“行”等与化学密切相关。
(1)下列服装主要用有机合成材料制成的是_______ (填标号)。
A 羊毛衫 B 涤纶连衣裙 C 腈纶运动衣 D 纯棉T恤
(2)①豆腐是人们喜爱的食品,其主要成分如表所示
从上表中可知,此豆腐中含有_______ 类营养素。
②食品安全日益受到人们关注。下列食品因有毒而不能食用的是_______ (填序号)。
A 用含发酵粉(含碳酸氢钠和有机酸等)制作发面食品 B 霉变的大米 C 用亚硝酸钠(NaNO2)代替食盐烹调的食品 D 食盐腌制的咸鸭蛋
(3)氯化钠是人类不可缺少的调味品,也是重要的化工原料,由于粗盐中含有少量 MgC12、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。


①操作Ⅲ所用的玻璃仪器有:烧杯、玻璃棒和_______ 。
②在蒸发过程中,待_______ 时,停止加热,利用余热将滤液蒸干。
③加入稍过量的Na2CO3溶液除了能除去粗盐中的 CaCl2外,它还可以除去_______ 。
④通过操作Ⅲ所得滤液中的溶质有_______ (用化学式表示)。
⑤某同学配制100g质量分数为8.5%的氯化钠溶液,按要求回答问题:
【计算】需要氯化钠固体的质量为________ g;
【称量】用托盘天平称量氯化钠固体时,氯化钠固体应放在天平的_______ 盘(填“左”或“右”)。
(1)下列服装主要用有机合成材料制成的是
A 羊毛衫 B 涤纶连衣裙 C 腈纶运动衣 D 纯棉T恤
(2)①豆腐是人们喜爱的食品,其主要成分如表所示
| 项目 | 水 | 蛋白质 | 油脂 | 糖类 | 维生素B1 | 维生素B2 | 钙 | 铁 |
| 每100克 | 89.30 g | 4.70 g | 1.30g | 2.80 g | 0.06mg | 0.03mg | 0.24 g | 1.40g |
从上表中可知,此豆腐中含有
②食品安全日益受到人们关注。下列食品因有毒而不能食用的是
A 用含发酵粉(含碳酸氢钠和有机酸等)制作发面食品 B 霉变的大米 C 用亚硝酸钠(NaNO2)代替食盐烹调的食品 D 食盐腌制的咸鸭蛋
(3)氯化钠是人类不可缺少的调味品,也是重要的化工原料,由于粗盐中含有少量 MgC12、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。


①操作Ⅲ所用的玻璃仪器有:烧杯、玻璃棒和
②在蒸发过程中,待
③加入稍过量的Na2CO3溶液除了能除去粗盐中的 CaCl2外,它还可以除去
④通过操作Ⅲ所得滤液中的溶质有
⑤某同学配制100g质量分数为8.5%的氯化钠溶液,按要求回答问题:
【计算】需要氯化钠固体的质量为
【称量】用托盘天平称量氯化钠固体时,氯化钠固体应放在天平的
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】氯化钠的部分溶解度如下:
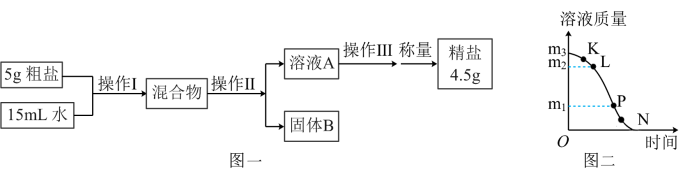
(1)20℃时,15g水中溶解_____ g氯化钠刚好形成饱和溶液。
(2)粗盐(含有泥沙的氯化钠)提纯的实验过程如图一所示,溶液A是溶液_____ (选填“饱和”或“不饱和”);操作Ⅱ是_____ 。
(3)操作Ⅲ过程中溶液质量与时间变化关系示意图如图二所示,相关分析正确的是_____ (填序号)。
a.m3<20g b.(m2-m1)是减少的水的质量
c.L、P表示的溶液,溶质质量分数相同 d.N点时,停止加热
| 温度(℃) | 10 | 20 | 30 | 40 | 60 | 80 | 100 |
| 溶解度(g/100g水) | 35.8 | 36.0 | 36.1 | 36.4 | 37.1 | 38.0 | 39.2 |

(1)20℃时,15g水中溶解
(2)粗盐(含有泥沙的氯化钠)提纯的实验过程如图一所示,溶液A是溶液
(3)操作Ⅲ过程中溶液质量与时间变化关系示意图如图二所示,相关分析正确的是
a.m3<20g b.(m2-m1)是减少的水的质量
c.L、P表示的溶液,溶质质量分数相同 d.N点时,停止加热
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】某校化学活动小组查阅资料发现,粗盐中除 外,还含有
外,还含有 、
、 、
、 以及泥沙等杂质。他们要除去杂质得到精盐,设计了下列实验方案。
以及泥沙等杂质。他们要除去杂质得到精盐,设计了下列实验方案。 序号①~⑧表示实验操作,用于沉淀的试剂稍过量
序号①~⑧表示实验操作,用于沉淀的试剂稍过量 :
:
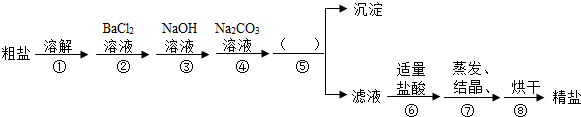
根据上述方案,回答下列问题:
(1)操作①中玻璃棒的作用是_______________ 。
(2)操作⑤的名称是_______________ 。
(3)实验中,加入“碳酸钠溶液”的目的是________________________________ 。
(4)操作⑧中加适量盐酸的目的是____________________________ 。
(5)操作②③④还可以的操作顺序是 。
 外,还含有
外,还含有 、
、 、
、 以及泥沙等杂质。他们要除去杂质得到精盐,设计了下列实验方案。
以及泥沙等杂质。他们要除去杂质得到精盐,设计了下列实验方案。 序号①~⑧表示实验操作,用于沉淀的试剂稍过量
序号①~⑧表示实验操作,用于沉淀的试剂稍过量 :
:
根据上述方案,回答下列问题:
(1)操作①中玻璃棒的作用是
(2)操作⑤的名称是
(3)实验中,加入“碳酸钠溶液”的目的是
(4)操作⑧中加适量盐酸的目的是
(5)操作②③④还可以的操作顺序是 。
| A.②④③ | B.③②④ | C.③④② | D.④③② |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】海水中含有泥沙等不溶性杂质和可溶性杂质(MgCl2、Na2SO4、CaCl2等),除去杂质可得到精盐,并用于生产和生活中、除去其中的可溶性杂质,可有以下操作顺序:①加过量的NaOH溶液;②加过量BaCl2溶液;③加过量Na2CO3溶液;④过滤;⑤加适量的稀盐酸;⑥蒸发结晶。
(1)写出除去MgCl2杂质时发生反应的化学方程式。
(2)加入过量的Na2CO3溶液的目的是______ 。
(3)操作⑤中加入的稀盐酸不能换成稀硫酸的原因是什么?
(1)写出除去MgCl2杂质时发生反应的化学方程式。
(2)加入过量的Na2CO3溶液的目的是
(3)操作⑤中加入的稀盐酸不能换成稀硫酸的原因是什么?
您最近一年使用:0次