甲、乙两种固体物质的溶解度曲线如下图所示。
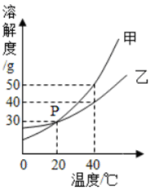
(1)40℃时,甲的饱和溶液中溶质与溶液的质量比为_________ (用最简整数比表示)
(2)将40℃等质量的甲、乙饱和溶液降温到20℃,所得溶液有关量甲<乙的是_____ 。
A 溶质质量分数 B 溶液质量 C 溶质质量 D 溶剂质量
(3)50℃时,将等质量甲、乙两种物质加入到等质量的水中,充分振荡后,所得溶液质量的大小关系为:甲_____ 乙(填“>”、“<”、“=”、“≥”、“≤”)。

(1)40℃时,甲的饱和溶液中溶质与溶液的质量比为
(2)将40℃等质量的甲、乙饱和溶液降温到20℃,所得溶液有关量甲<乙的是
A 溶质质量分数 B 溶液质量 C 溶质质量 D 溶剂质量
(3)50℃时,将等质量甲、乙两种物质加入到等质量的水中,充分振荡后,所得溶液质量的大小关系为:甲
更新时间:2019-06-28 09:24:20
|
相似题推荐
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐1】甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示。据图回答:

(1)常温时溶解度最大的物质是______ 。
(2)30℃时,等质量的三种物质的饱和溶液溶剂质量最大的是______ 。
(3)A点为图中的一个交点,A点的含义是______ 。
(4)50℃时,乙的饱和溶液中溶质与溶液的质量比为______ 。
(5)等质量的三种饱和溶液分别从40℃降温至10℃,析出晶体质量最大的是______ 。
(6)30℃时,10g水中至少溶解______ g丙物质可形成饱和溶液。
(7)满足溶解度乙>丙>甲的温度T的范围约是______ 。

(1)常温时溶解度最大的物质是
(2)30℃时,等质量的三种物质的饱和溶液溶剂质量最大的是
(3)A点为图中的一个交点,A点的含义是
(4)50℃时,乙的饱和溶液中溶质与溶液的质量比为
(5)等质量的三种饱和溶液分别从40℃降温至10℃,析出晶体质量最大的是
(6)30℃时,10g水中至少溶解
(7)满足溶解度乙>丙>甲的温度T的范围约是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。
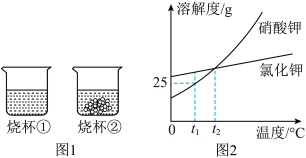
(1)烧杯②中的上层清液是否达到饱和状态?____ (填“是”、“否”或“无法判断”);
(2)烧杯②中溶解的溶质是____ (填化学式);
(3)t1℃时200g硝酸钾的饱和溶液中含有硝酸钾的质量为____ g;
(4)关于图1 中烧杯内的物质,下列说法正确的是____ 。
A 烧杯①内溶液中溶质的质量分数<烧杯②内上层清液中溶质的质量分数
B 蒸发一定量的水,烧杯②一定有固体析出
C 将两个烧杯中的溶液混合,充分搅拌后,烧杯中可能还有氯化钾没有溶解
D 将温度升高到t2℃,烧杯②中固体一定全部溶解(不考虑水的蒸发)
E 将温度升高到t2℃,烧杯①内溶液的质量 = 烧杯②内溶液的质量(不考虑水的蒸发)

(1)烧杯②中的上层清液是否达到饱和状态?
(2)烧杯②中溶解的溶质是
(3)t1℃时200g硝酸钾的饱和溶液中含有硝酸钾的质量为
(4)关于图1 中烧杯内的物质,下列说法正确的是
A 烧杯①内溶液中溶质的质量分数<烧杯②内上层清液中溶质的质量分数
B 蒸发一定量的水,烧杯②一定有固体析出
C 将两个烧杯中的溶液混合,充分搅拌后,烧杯中可能还有氯化钾没有溶解
D 将温度升高到t2℃,烧杯②中固体一定全部溶解(不考虑水的蒸发)
E 将温度升高到t2℃,烧杯①内溶液的质量 = 烧杯②内溶液的质量(不考虑水的蒸发)
您最近一年使用:0次
【推荐3】水是一种宝贵的自然资源,我们应该了解水的净化和水资源的保护。
(1)自来水厂的净水流程一般包括:沉淀、过滤、_______ 、消毒等步骤。
(2)在日常生活中,可以用_______ 区别硬水和软水。
(3)漂白粉可用于自来水的杀菌消毒,其有效成分是次氯酸钙(化学式为Ca(C1O)2),次氯酸钙在空气中可发生如下反应: ,则X的化学式为
,则X的化学式为_______ 。
(4)如图是甲、乙、丙三种物质的溶解度曲线。

①t1℃时,甲和_______ 两种物质饱和溶液的溶质质量分数相等。
②t2℃时,向50克水中加入35克固体甲,得到溶液_______ 克。
③从甲、乙的混合物中分离提纯甲物质,一般采用______ 的方法。
(1)自来水厂的净水流程一般包括:沉淀、过滤、
(2)在日常生活中,可以用
(3)漂白粉可用于自来水的杀菌消毒,其有效成分是次氯酸钙(化学式为Ca(C1O)2),次氯酸钙在空气中可发生如下反应:
 ,则X的化学式为
,则X的化学式为(4)如图是甲、乙、丙三种物质的溶解度曲线。

①t1℃时,甲和
②t2℃时,向50克水中加入35克固体甲,得到溶液
③从甲、乙的混合物中分离提纯甲物质,一般采用
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐1】有一工业过程:
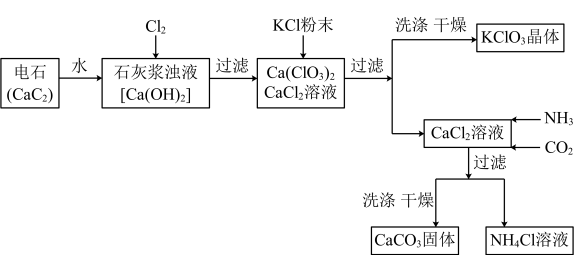
按要求回答下列问题:
(1)请将电石与水反应的化学方程式补充完整:
CaC2+2H2O═Ca(OH)2+__________ ↑。
(2)有关物质常温下的溶解度如表:
上述流程中加入了KCl粉末,KCl与__________ (填化学式)发生了复分解反应得KClO3晶体,该过程得到KClO3晶体的原因是__________ 。
(3)写出向CaCl2溶液中通入两种气体生成CaCO3的化学方程式:__________ 。

按要求回答下列问题:
(1)请将电石与水反应的化学方程式补充完整:
CaC2+2H2O═Ca(OH)2+
(2)有关物质常温下的溶解度如表:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
上述流程中加入了KCl粉末,KCl与
(3)写出向CaCl2溶液中通入两种气体生成CaCO3的化学方程式:
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】如图所示为X、Y、Z三种固体物质的溶解度曲线,请据图回答下列问题:
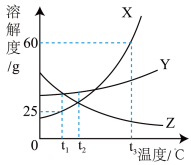
(1)______ ℃时,X与Z的溶解度相等。
(2)当X中混有少量Y时,若要提纯X,可采取的方法是______ 。
(3)t3℃时,将等质量X、Y、Z三种物质的饱和溶液分别降温到t1℃时,所得溶液中溶剂质量由大到小的顺序是______ 。
(4)在t3℃时,向盛有30gX物质的烧杯中加入50g水,充分溶解,若要增大该溶液的溶质质量分数,可采用的方法是______ 。

(1)
(2)当X中混有少量Y时,若要提纯X,可采取的方法是
(3)t3℃时,将等质量X、Y、Z三种物质的饱和溶液分别降温到t1℃时,所得溶液中溶剂质量由大到小的顺序是
(4)在t3℃时,向盛有30gX物质的烧杯中加入50g水,充分溶解,若要增大该溶液的溶质质量分数,可采用的方法是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐3】水是人类宝贵的自然资源。
(1)判断生活用水是硬水还是软水,可加入_________ 进行检验。
(2)下列净化水的单一操作中,相对净化程度较高的是_________ (填字母)。
A 静置沉淀 B 吸附沉淀 C 蒸馏 D 过滤
(3)在电解水实验中,正负极产生的气体体积比约为_________ 。
(4) 和
和 在不同温度时的溶解度如下表所示。
在不同温度时的溶解度如下表所示。
请回答下列问题:
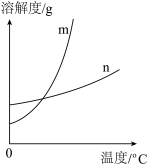
①依据上表数据,绘制 和
和 的溶解度曲线,如图中能表示
的溶解度曲线,如图中能表示 溶解度曲线的是
溶解度曲线的是__________ (填“m”或“n”)。
②由表中数据分析可知, 和
和 在某一温度时具有相同的溶解度x,则x的取值范围是
在某一温度时具有相同的溶解度x,则x的取值范围是__________ 。
③现有40℃时等质量的硝酸钾、氯化钾饱和溶液,加热蒸发等质量的水后恢复至40℃,剩余溶液的质量关系大小为硝酸钾溶液__________ 氯化钾溶液(填“>”、“<”或“=”)。
A是80℃含有120g水的 溶液,经过如下操作,得到102g
溶液,经过如下操作,得到102g 固体。
固体。
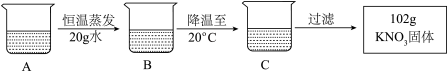
下列对以上过程的分析,正确的是_________ (填字母编号)
a A到B的过程中,溶质质量没有改变 b B中溶质与溶剂的质量比为169:100
c 开始析出 固体的温度在60℃至70℃之间 d A溶液的质量等于222g
固体的温度在60℃至70℃之间 d A溶液的质量等于222g
(1)判断生活用水是硬水还是软水,可加入
(2)下列净化水的单一操作中,相对净化程度较高的是
A 静置沉淀 B 吸附沉淀 C 蒸馏 D 过滤
(3)在电解水实验中,正负极产生的气体体积比约为
(4)
 和
和 在不同温度时的溶解度如下表所示。
在不同温度时的溶解度如下表所示。| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
| 溶解度/g |  | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 |
 | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 4.55 | 48.3 | 51.1 | |
①依据上表数据,绘制
 和
和 的溶解度曲线,如图中能表示
的溶解度曲线,如图中能表示 溶解度曲线的是
溶解度曲线的是
②由表中数据分析可知,
 和
和 在某一温度时具有相同的溶解度x,则x的取值范围是
在某一温度时具有相同的溶解度x,则x的取值范围是③现有40℃时等质量的硝酸钾、氯化钾饱和溶液,加热蒸发等质量的水后恢复至40℃,剩余溶液的质量关系大小为硝酸钾溶液
A是80℃含有120g水的
 溶液,经过如下操作,得到102g
溶液,经过如下操作,得到102g 固体。
固体。
下列对以上过程的分析,正确的是
a A到B的过程中,溶质质量没有改变 b B中溶质与溶剂的质量比为169:100
c 开始析出
 固体的温度在60℃至70℃之间 d A溶液的质量等于222g
固体的温度在60℃至70℃之间 d A溶液的质量等于222g
您最近一年使用:0次
【推荐1】请根据下图a、b、c三种固体物质的溶解度曲线,回答下列问题:
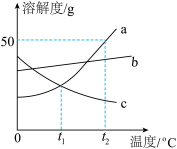
(1)在___________ ℃时,a、c两种物质的溶解度相等。
(2)在t2℃时,向盛有50ga物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为___________ g。
(3)若a物质中混有少量b物质,最好采用___________ 的方法提纯。(填“降温结晶”或“蒸发结晶”)。
(4)t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是___________
(5)将t2℃时等质量的a、b、c三种物质的饱和溶液降温到t1℃,所得溶液的质量分数由小到大的顺序为___________ 。
(6)下列说法正确的是___________。
(7)如图所示是利用海水提取粗盐的过程:

根据海水晒盐的原理,下列说法中正确的是

(1)在
(2)在t2℃时,向盛有50ga物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为
(3)若a物质中混有少量b物质,最好采用
(4)t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是
(5)将t2℃时等质量的a、b、c三种物质的饱和溶液降温到t1℃,所得溶液的质量分数由小到大的顺序为
(6)下列说法正确的是___________。
| A.将a物质的饱和溶液变为不饱和溶液,其溶质的质量分数⼀定减小 |
| B.将t1℃时c物质的饱和溶液升温到t2℃,其溶液的质量⼀定减小 |
| C.配制⼀定溶质质量分数的b物质溶液,若量取水时俯视读数,其它操作均正确,则配制的b溶液中溶质的质量分数将偏高 |

根据海水晒盐的原理,下列说法中正确的是
| A.海水进入贮水池,海水的成分基本不变 |
| B.在蒸发池中,海水中氯化钠的质量逐渐增加 |
| C.在蒸发池中,海水中水的质量逐渐增加 |
| D.析出晶体后的母液是氯化钠的饱和溶液 |
您最近一年使用:0次
【推荐2】溶液在生活、生产、科研中具有广泛的用途。如图1是A、B、C三种固体物质的溶解度曲线。请回答下列问题:
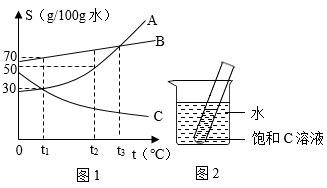
(1)t1°C时,将A、B、C固体各a g分别加入100 g 水中,得到两种饱和溶液,则a的取值范围是______ 。
(2)为使图2试管中饱和C溶液变浑浊,可向烧杯中加入物质______ (填字母)。
a.生石灰 b.冰块 c.氯化钠 d.浓硫酸
(3)t2°C时,向50 g水中加入25 g物质B配成溶液,将该溶液降温至t1°C时,其属于______ (填“饱和”或“不饱和”)溶液。
(4)根据A、B、C三种物质溶解度曲线,分析下列说法正确的是______ (填序号)。
①将C物质不饱和溶液变为饱和溶液,溶质的质量分数一定变大
②t2°C时,取等质量的A、B两种物质的饱和溶液分别蒸发等质量的水后,恢复到t2°C,析出晶体的质量A<B
⑨t3°C时,A、B、C三种物质溶解度的大小关系是A=B>C

(1)t1°C时,将A、B、C固体各a g分别加入100 g 水中,得到两种饱和溶液,则a的取值范围是
(2)为使图2试管中饱和C溶液变浑浊,可向烧杯中加入物质
a.生石灰 b.冰块 c.氯化钠 d.浓硫酸
(3)t2°C时,向50 g水中加入25 g物质B配成溶液,将该溶液降温至t1°C时,其属于
(4)根据A、B、C三种物质溶解度曲线,分析下列说法正确的是
①将C物质不饱和溶液变为饱和溶液,溶质的质量分数一定变大
②t2°C时,取等质量的A、B两种物质的饱和溶液分别蒸发等质量的水后,恢复到t2°C,析出晶体的质量A<B
⑨t3°C时,A、B、C三种物质溶解度的大小关系是A=B>C
您最近一年使用:0次
【推荐3】研究物质的溶解对于生产、生活有着重要意义。
(1)下表是碳酸钠的部分溶解度数据。
①由表中数据可知,碳酸钠的溶解度随温度升高______ (合理即可)。
②20℃时,将装有饱和碳酸钠溶液(底部有碳酸钠粉末)的小试管放入盛水的烧杯中(如图)。向烧杯中加入某物质后,试管底部的粉末减少,则加入的物质可能是______ (填字母序号),该物质形成的溶液中存在的微粒有______ 。
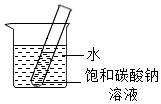
A.氢氧化钠 B.碳酸钙 C.硝酸铵 D.氯化钠
(2)t℃时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量关系绘制成如图所示斜线。下列说法错误的是______ 。
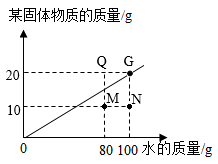
a.t℃时该物质的溶解度是20
b.该物质的溶解度随温度的升高而增大
c.N点所示的溶液中溶质质量分数是10%
d.图中4个点所示的溶液中溶质质量分数大小关系是:N<M<G=Q
(1)下表是碳酸钠的部分溶解度数据。
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| 溶解度/g | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 | 45.1 | 44.7 |
②20℃时,将装有饱和碳酸钠溶液(底部有碳酸钠粉末)的小试管放入盛水的烧杯中(如图)。向烧杯中加入某物质后,试管底部的粉末减少,则加入的物质可能是

A.氢氧化钠 B.碳酸钙 C.硝酸铵 D.氯化钠
(2)t℃时,根据某固体物质在不同质量的水中达到饱和状态时所溶解的质量关系绘制成如图所示斜线。下列说法错误的是

a.t℃时该物质的溶解度是20
b.该物质的溶解度随温度的升高而增大
c.N点所示的溶液中溶质质量分数是10%
d.图中4个点所示的溶液中溶质质量分数大小关系是:N<M<G=Q
您最近一年使用:0次



