盐城濒临黄海,拥有巨大的天然宝库。
(1)海堤树林茂密,让人清新呼吸。
①树林中的绿色植物通过光合作用,吸收_____ (填化学式),放出O2,将_____ 能转化为化学能。
②树林中富含抗氧化防衰老的负氧离子。一种负氧离子(O2-)的一个原子团是由一个O2分子俘获了空气中一个自由电子形成的微粒,每个O2-中共含有_____ 个电子。
(2)滩涂花海飘香,使人流连忘返。
①鲜花的香味在空气中扩散,是大量的带有香味的分子_____ 的结果。
②培育鲜花的某种营养液呈蓝色,可能由KNO3、Ca(NO3)2、CuCl2中的一种或几种物质配制而成,其中Ca、N的元素质量比为1:1,则该营养液中含有_____ 种溶质。从均衡植物所需营养元素的角度分析,营养液中还需补充_____ (填元素符号)。
(3)大海资源丰富,引人不断探索。
从海水中可以提取粗盐(含少量泥沙和CaCl2、MgSO4等可溶性杂质)。小明利用如图流程进行除杂,得到精盐。

①操作1需要在____ (填字母序号)中进行。
A.研钵 B.量筒 C.烧杯 D.广口瓶
②操作2的步骤为溶解、过滤、_____ 、结晶,过滤操作中玻璃棒的作用是_____ 。
③操作3的步骤为“盐洗”(即用NaCl溶液浸洗粗盐,以溶解除去其中可溶性杂质),过滤、烘干,则“盐洗”溶液应选用NaCl的_____ (填“饱和”或“不饱和”)溶液。
④在农业生产上,常用质量分数为16%的NaCl溶液选种。小明称取实验制得的精盐l6g,加入盛有84mL蒸馏水的烧杯里(实验条件下,水的密度为1g•mL-1),完全溶解。配制所得的NaCl溶液的浓度低于16%,原因是____ 。
⑤若利用化学方法除去粗盐中CaCl2、MgSO4两种杂质,可在粗盐溶液中依次加入稍过量的三种溶液:BaCl2溶液、_____ (填化学式)溶液、Na2CO3溶液。充分反应后过滤,加入过量稀盐酸,搅拌、煮沸。
(1)海堤树林茂密,让人清新呼吸。
①树林中的绿色植物通过光合作用,吸收
②树林中富含抗氧化防衰老的负氧离子。一种负氧离子(O2-)的一个原子团是由一个O2分子俘获了空气中一个自由电子形成的微粒,每个O2-中共含有
(2)滩涂花海飘香,使人流连忘返。
①鲜花的香味在空气中扩散,是大量的带有香味的分子
②培育鲜花的某种营养液呈蓝色,可能由KNO3、Ca(NO3)2、CuCl2中的一种或几种物质配制而成,其中Ca、N的元素质量比为1:1,则该营养液中含有
(3)大海资源丰富,引人不断探索。
从海水中可以提取粗盐(含少量泥沙和CaCl2、MgSO4等可溶性杂质)。小明利用如图流程进行除杂,得到精盐。

①操作1需要在
A.研钵 B.量筒 C.烧杯 D.广口瓶
②操作2的步骤为溶解、过滤、
③操作3的步骤为“盐洗”(即用NaCl溶液浸洗粗盐,以溶解除去其中可溶性杂质),过滤、烘干,则“盐洗”溶液应选用NaCl的
④在农业生产上,常用质量分数为16%的NaCl溶液选种。小明称取实验制得的精盐l6g,加入盛有84mL蒸馏水的烧杯里(实验条件下,水的密度为1g•mL-1),完全溶解。配制所得的NaCl溶液的浓度低于16%,原因是
⑤若利用化学方法除去粗盐中CaCl2、MgSO4两种杂质,可在粗盐溶液中依次加入稍过量的三种溶液:BaCl2溶液、
2019·江苏盐城·中考真题 查看更多[3]
(已下线)《单元测试定心卷》第三单元 物质构成的奥秘(能力提升)-2020-2021学年九年级化学上册单元测试定心卷(沪教版)备战2020中考化学章节强化训练——专题二:盐和化肥江苏省盐城市2019年中考化学试题
更新时间:2019-06-28 20:57:22
|
相似题推荐
综合应用题
|
较难
(0.4)
【推荐1】科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环(如图所示)。
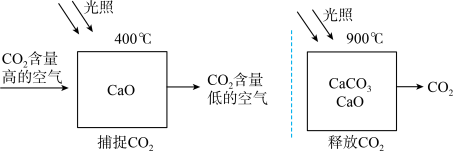
某化学小组的同学对此 非常感兴趣,在老师的指导下,设计了如图装置探究上述设想的反应原理是否可行。

(1)能证明装置A“释放出CO2”的现象是_______________ ;
(2)装置B在实验结束撤掉酒精喷灯时的作用是_____________
(3)上述反应结束后,小组同学对D中固体的成分进行探究,以证明是否“捕捉”到CO2。
【资料卡片】氧化钙和水反应生成氢氧化钙,此反应放出大量的热。氢氧化钙是一种微溶于水的白色粉末。
【猜想与假设】D中的固体可能为:I.只有氧化钙;Ⅱ.氧化钙与碳酸钙;Ⅲ.只有碳酸钙。
【进行实验】(1)甲同学从D中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,认为猜想Ⅲ成立。
乙同学认为甲同学实验不足以证明猜想Ⅲ成立,其原因是________________ 。
(2)乙同学从D中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热。乙同学据此认为试管中的固体有氧化钙,即猜想I成立。
(3)丙同学认为乙同学的实验不够严谨,于是向D物质中加稀盐酸,再结合乙同学的结论,完成了下面的实验报告后,得出猜想Ⅱ成立的结论。
(4)通过以上探究,小组同学认为科学家的设想在反应原理上是可行的。该设想的优点有__________ (填字母序号)。
A.原料易得 B.充分利用太阳能 C.释放出的CO2可作为资源加以利用
(5)请写出上述实验过程中的任何一个化学方程式:____________ 。

某化学小组的同学对此 非常感兴趣,在老师的指导下,设计了如图装置探究上述设想的反应原理是否可行。

(1)能证明装置A“释放出CO2”的现象是
(2)装置B在实验结束撤掉酒精喷灯时的作用是
(3)上述反应结束后,小组同学对D中固体的成分进行探究,以证明是否“捕捉”到CO2。
【资料卡片】氧化钙和水反应生成氢氧化钙,此反应放出大量的热。氢氧化钙是一种微溶于水的白色粉末。
【猜想与假设】D中的固体可能为:I.只有氧化钙;Ⅱ.氧化钙与碳酸钙;Ⅲ.只有碳酸钙。
【进行实验】(1)甲同学从D中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,认为猜想Ⅲ成立。
乙同学认为甲同学实验不足以证明猜想Ⅲ成立,其原因是
(2)乙同学从D中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热。乙同学据此认为试管中的固体有氧化钙,即猜想I成立。
(3)丙同学认为乙同学的实验不够严谨,于是向D物质中加稀盐酸,再结合乙同学的结论,完成了下面的实验报告后,得出猜想Ⅱ成立的结论。
| 实验步骤 | 实验现象 | 实验结论 |
| 猜想Ⅱ成立 |
(4)通过以上探究,小组同学认为科学家的设想在反应原理上是可行的。该设想的优点有
A.原料易得 B.充分利用太阳能 C.释放出的CO2可作为资源加以利用
(5)请写出上述实验过程中的任何一个化学方程式:
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】题4 自然界中碳、氧循环简单示意图如图所示:请回答下列问题。
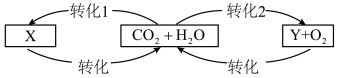
(1)转化1表示水吸收二氧化碳的过程,化学反应方程式为______________________ ;科技小组设计验证该反应的实验如下图所示,甲瓶中盛放的是浓 ,乙瓶中盛放的是用石蕊溶液染成紫色的干燥小花。若关闭阀门Ⅰ,打开阀门Ⅱ,紫色小花
,乙瓶中盛放的是用石蕊溶液染成紫色的干燥小花。若关闭阀门Ⅰ,打开阀门Ⅱ,紫色小花_________ ;若关闭阀门Ⅱ,打开阀门Ⅰ,紫色小花_________ ,则证明该反应发生。

(2)转化2是绿色植物光合作用生成葡萄糖( )与氧气的过程,写出该反应的化学方程式
)与氧气的过程,写出该反应的化学方程式___________________________ ,生成的葡萄糖供植物生长,由此推断绿色植物中肯定有的元素是____________ 。
(3)转化1与转化2两个反应的反应物相同,但得到的产物却完全不同,原因是___________ 。上述碳、氧循环对人类的意义是_______________________________________________________________________ 。
(4)化学物质是一把“双刃剑”,有利也有弊。大气中的二氧化碳能产生温室效应。温室效应的利是__________________________ ,弊是_______________________________________________________ 。
(5)近年来大气中 含量不断上升,为了控制
含量不断上升,为了控制 引起的温室效应,科学家提出建立如下图所示的二氧化碳循环流程:
引起的温室效应,科学家提出建立如下图所示的二氧化碳循环流程:
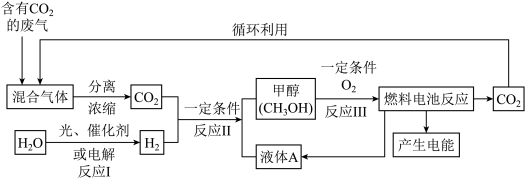
①上述反应Ⅱ的化学方程式为: ,其中A的化学式为
,其中A的化学式为_____________ , 在该反应中表现出来的性质是
在该反应中表现出来的性质是__________ 。
②燃料电池反应Ⅲ的化学方程式是______________________________ ,该反应没有燃烧现象,具有洁净、高效的特点,其工作时主要是将__________ 能转化为电能。
③使原料中各原子的利用率尽可能达到100%是“绿色化学”的核心理念之一。上述流程中除 得到循环利用外,还可以循环利用的物质是
得到循环利用外,还可以循环利用的物质是_____________ (填化学式)。

(1)转化1表示水吸收二氧化碳的过程,化学反应方程式为
 ,乙瓶中盛放的是用石蕊溶液染成紫色的干燥小花。若关闭阀门Ⅰ,打开阀门Ⅱ,紫色小花
,乙瓶中盛放的是用石蕊溶液染成紫色的干燥小花。若关闭阀门Ⅰ,打开阀门Ⅱ,紫色小花
(2)转化2是绿色植物光合作用生成葡萄糖(
 )与氧气的过程,写出该反应的化学方程式
)与氧气的过程,写出该反应的化学方程式(3)转化1与转化2两个反应的反应物相同,但得到的产物却完全不同,原因是
(4)化学物质是一把“双刃剑”,有利也有弊。大气中的二氧化碳能产生温室效应。温室效应的利是
(5)近年来大气中
 含量不断上升,为了控制
含量不断上升,为了控制 引起的温室效应,科学家提出建立如下图所示的二氧化碳循环流程:
引起的温室效应,科学家提出建立如下图所示的二氧化碳循环流程:
①上述反应Ⅱ的化学方程式为:
 ,其中A的化学式为
,其中A的化学式为 在该反应中表现出来的性质是
在该反应中表现出来的性质是②燃料电池反应Ⅲ的化学方程式是
③使原料中各原子的利用率尽可能达到100%是“绿色化学”的核心理念之一。上述流程中除
 得到循环利用外,还可以循环利用的物质是
得到循环利用外,还可以循环利用的物质是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】化学体现在自然,生活,科技等各个领域。
(一)化学与自然
(1)“水循环”、“氧循环”和“碳循环”是自然界中重要的三大循环,下列用化学学科观点分析“碳、氧循环”的说法中,正确的是 (填字母)。
(2)碳、氧循环过程中,绿色植物进行了最高效的能量转化,将太阳能转化为_____ 能,并提供了人类生存的氧气,写出该反应的化学方程式______
(二)化学与科技
2022年11月29日,神舟十五号飞船再送3名宇航员进入天宫空间站,天宫空间站史无前例迎来6名宇航员在岗。空间站“循环”系统为宇航员提供了氧气。(如1图 )


(3)二氧化碳收集系统可以采用分子筛或固态胺。其中分子筛表面布满孔穴,类似于活性炭,具有____ 性。
(4)实验室中模拟水电解系统,装置(如2图 )所示,a管内气体的化学式是______ ,a、b管中气体的质量比为______ 。
(5)电解后的氢气需要储存,新型镁铝合金(Mg17Al12)是一种储氢材料,在氩气的氛围中,将一定比例的金属镁和铝熔炼得到镁铝合金。熔炼时须通入氩气,其目的是______ 。镁铝合金储氢和释氢过程(如3图)释放的比贮存的H2_______ (填“多”或“少”)。
(6)萨巴蒂尔反应系统:系统的核心部件是萨巴蒂尔反应器。气体在萨巴蒂尔反应器内570-580K的温度下,以及催化剂的作用下反应,试写出萨巴蒂尔反应器中发生反应的化学方程式_____ 。
(三)化学与生活
目前市售蔬菜农药残留量虽然已达到国家标准,但通过科学的清洗方法仍可进一步降低农药残留。

实验人员分别选取含甲、乙农药的蔬菜,研究了不同清洗方法对农药去除率的影响。
清水浸泡:图1呈现出两种农药的去除率随浸泡时间的变化。
洗洁精清洗:实验选择了6种洗洁精进行测试,结果表明,多数洗洁精对农药的去除率可达到60%以上,最高可达到84%。
碱性溶液浸泡:食用碱(Na2CO3和 NaHCO3)溶液有利于农药分解。图2表示不同浓度的食用碱溶液对农药去除率的影响。希望同学们可以选择科学的清洗方法,更加安全的食用蔬菜。
依据文章内容,回答下列问题。
(7)依据图1分析,去除农药残留的最佳浸泡时间是______ min。
(8)食用碱中阳离子是____ (填化学符号)。Na2CO3可以使无色酚酞溶液变红,原因是____ 。
(9)用食用碱溶液浸泡含有农药甲的蔬菜时,可以选取最佳浓度是______ (填序号,下同)。
A .15% B. 10% C. 2% D. 8%
配制该浓度的食用碱溶液200克,需要食用碱______ 克。
(10)下列说法正确的是 。
(一)化学与自然
(1)“水循环”、“氧循环”和“碳循环”是自然界中重要的三大循环,下列用化学学科观点分析“碳、氧循环”的说法中,正确的是 (填字母)。
| A.变化观:碳,氧循环能体现自然界中的物质和能量循环 |
| B.守恒观:碳、氧循环过程中各元素守恒,其化合价不变 |
| C.微粒观:绿色植物能使自然界中的氧原子总数增加 |
| D.平衡观:碳、氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定 |
(二)化学与科技
2022年11月29日,神舟十五号飞船再送3名宇航员进入天宫空间站,天宫空间站史无前例迎来6名宇航员在岗。空间站“循环”系统为宇航员提供了氧气。(如1图 )


(3)二氧化碳收集系统可以采用分子筛或固态胺。其中分子筛表面布满孔穴,类似于活性炭,具有
(4)实验室中模拟水电解系统,装置(如2图 )所示,a管内气体的化学式是
(5)电解后的氢气需要储存,新型镁铝合金(Mg17Al12)是一种储氢材料,在氩气的氛围中,将一定比例的金属镁和铝熔炼得到镁铝合金。熔炼时须通入氩气,其目的是
(6)萨巴蒂尔反应系统:系统的核心部件是萨巴蒂尔反应器。气体在萨巴蒂尔反应器内570-580K的温度下,以及催化剂的作用下反应,试写出萨巴蒂尔反应器中发生反应的化学方程式
(三)化学与生活
目前市售蔬菜农药残留量虽然已达到国家标准,但通过科学的清洗方法仍可进一步降低农药残留。

实验人员分别选取含甲、乙农药的蔬菜,研究了不同清洗方法对农药去除率的影响。
清水浸泡:图1呈现出两种农药的去除率随浸泡时间的变化。
洗洁精清洗:实验选择了6种洗洁精进行测试,结果表明,多数洗洁精对农药的去除率可达到60%以上,最高可达到84%。
碱性溶液浸泡:食用碱(Na2CO3和 NaHCO3)溶液有利于农药分解。图2表示不同浓度的食用碱溶液对农药去除率的影响。希望同学们可以选择科学的清洗方法,更加安全的食用蔬菜。
依据文章内容,回答下列问题。
(7)依据图1分析,去除农药残留的最佳浸泡时间是
(8)食用碱中阳离子是
(9)用食用碱溶液浸泡含有农药甲的蔬菜时,可以选取最佳浓度是
A .15% B. 10% C. 2% D. 8%
配制该浓度的食用碱溶液200克,需要食用碱
(10)下列说法正确的是 。
| A.多数洗洁精对农药的清洗效果比清水浸泡的好 |
| B.采用清水浸泡去除农药的时间越长越好 |
| C.食用碱的去除效果较好,是因为在浸泡过程中农药发生了化学变化 |
您最近一年使用:0次
【推荐1】水是宝贵的自然资料,让我们一起走进“水”的世界。
①下图电解水实验中,反应的化学方程式是___ 。水电解过程发生改变的微粒名称是______ 。

②医疗上常用0.9%NaCl溶液作生理盐水,配制1000g生理盐水需要氯化钠固体的质量为_______ 还可以制取碳酸饮料,该过程中发生反应的化学方程式为_____________ 。
③某化学兴趣小组欲进行粗盐的初步提纯。粗盐的提纯实验步骤包括:a计算产率,b过滤,c溶解,d蒸发,e称量。实验步骤的正确顺序是:e、_________ 、a(填序号)。若NaCl的产率偏低,则可能的原因是_________ (填字母)。
A.过滤时滤纸有破损
B.蒸发后所得精盐未完全蒸干,含有水
C.溶解含泥沙的粗食盐时,加入的水量不足
提示:产率= ×100%
×100%
④已知KCl的溶解度20℃时为34g/100g水,40℃时为40g/100g水。某实验小组做了如下实验。
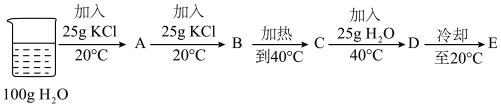
A中所得溶液中溶质与溶剂的质量比为__________ ;溶质的质量分数相等的是___________ 。
I. B和C II. B和E Ⅲ. C和D IV. D和E
①下图电解水实验中,反应的化学方程式是

②医疗上常用0.9%NaCl溶液作生理盐水,配制1000g生理盐水需要氯化钠固体的质量为
③某化学兴趣小组欲进行粗盐的初步提纯。粗盐的提纯实验步骤包括:a计算产率,b过滤,c溶解,d蒸发,e称量。实验步骤的正确顺序是:e、
A.过滤时滤纸有破损
B.蒸发后所得精盐未完全蒸干,含有水
C.溶解含泥沙的粗食盐时,加入的水量不足
提示:产率=
 ×100%
×100%④已知KCl的溶解度20℃时为34g/100g水,40℃时为40g/100g水。某实验小组做了如下实验。

A中所得溶液中溶质与溶剂的质量比为
I. B和C II. B和E Ⅲ. C和D IV. D和E
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】钠及其化合物是中学化学学习和研究的重要内容。

(1)图1是钠的原子结构示意图。下列说法不正确的是_____(填字母序号)。
(2)钠与水反应生成氢氧化钠和氢气,化学方程式为_______ ;小苏打受热分解成碳酸钠、二氧化碳和水,化学方程式为______ 。
(3)配制一瓶如图2所示的溶液需氯化钠_____ g;配制50g6%的氯化钠溶液,若用量筒量取水时俯视读数(其他操作正确),则溶液的质量分数______ 6%(填“>”“<”或“=”)。
(4)已知 ;
;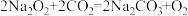 。实验室敞口放置的过氧化钠(Na2O2)已部分变质,取少量该固体样品于试管中,加足量水,可观察到什么现象:
。实验室敞口放置的过氧化钠(Na2O2)已部分变质,取少量该固体样品于试管中,加足量水,可观察到什么现象:_______ ;如何检验该水溶液中含有氢氧化钠:_______ 。(请简要写出实验的步骤和现象)
(5)某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?

(1)图1是钠的原子结构示意图。下列说法不正确的是_____(填字母序号)。
| A.钠属于金属元素 | B.钠原子的质子数为11 |
| C.钠离子的符号为Na+ | D.钠在化学反应中易得到电子 |
(2)钠与水反应生成氢氧化钠和氢气,化学方程式为
(3)配制一瓶如图2所示的溶液需氯化钠
(4)已知
 ;
;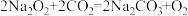 。实验室敞口放置的过氧化钠(Na2O2)已部分变质,取少量该固体样品于试管中,加足量水,可观察到什么现象:
。实验室敞口放置的过氧化钠(Na2O2)已部分变质,取少量该固体样品于试管中,加足量水,可观察到什么现象:(5)某钢铁厂用赤铁矿石炼铁。若该厂每天需消耗6000t含氧化铁80%的赤铁矿石,则理论上可日产含铁96%的生铁的质量是多少?
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】化学体现在自然,生活,科技等各个领域。
(一)化学与自然
(1)“水循环”、“氧循环”和“碳循环”是自然界中重要的三大循环,下列用化学学科观点分析“碳、氧循环”的说法中,正确的是 (填字母)。
(2)碳、氧循环过程中,绿色植物进行了最高效的能量转化,将太阳能转化为_____ 能,并提供了人类生存的氧气,写出该反应的化学方程式______
(二)化学与科技
2022年11月29日,神舟十五号飞船再送3名宇航员进入天宫空间站,天宫空间站史无前例迎来6名宇航员在岗。空间站“循环”系统为宇航员提供了氧气。(如1图 )


(3)二氧化碳收集系统可以采用分子筛或固态胺。其中分子筛表面布满孔穴,类似于活性炭,具有____ 性。
(4)实验室中模拟水电解系统,装置(如2图 )所示,a管内气体的化学式是______ ,a、b管中气体的质量比为______ 。
(5)电解后的氢气需要储存,新型镁铝合金(Mg17Al12)是一种储氢材料,在氩气的氛围中,将一定比例的金属镁和铝熔炼得到镁铝合金。熔炼时须通入氩气,其目的是______ 。镁铝合金储氢和释氢过程(如3图)释放的比贮存的H2_______ (填“多”或“少”)。
(6)萨巴蒂尔反应系统:系统的核心部件是萨巴蒂尔反应器。气体在萨巴蒂尔反应器内570-580K的温度下,以及催化剂的作用下反应,试写出萨巴蒂尔反应器中发生反应的化学方程式_____ 。
(三)化学与生活
目前市售蔬菜农药残留量虽然已达到国家标准,但通过科学的清洗方法仍可进一步降低农药残留。

实验人员分别选取含甲、乙农药的蔬菜,研究了不同清洗方法对农药去除率的影响。
清水浸泡:图1呈现出两种农药的去除率随浸泡时间的变化。
洗洁精清洗:实验选择了6种洗洁精进行测试,结果表明,多数洗洁精对农药的去除率可达到60%以上,最高可达到84%。
碱性溶液浸泡:食用碱(Na2CO3和 NaHCO3)溶液有利于农药分解。图2表示不同浓度的食用碱溶液对农药去除率的影响。希望同学们可以选择科学的清洗方法,更加安全的食用蔬菜。
依据文章内容,回答下列问题。
(7)依据图1分析,去除农药残留的最佳浸泡时间是______ min。
(8)食用碱中阳离子是____ (填化学符号)。Na2CO3可以使无色酚酞溶液变红,原因是____ 。
(9)用食用碱溶液浸泡含有农药甲的蔬菜时,可以选取最佳浓度是______ (填序号,下同)。
A .15% B. 10% C. 2% D. 8%
配制该浓度的食用碱溶液200克,需要食用碱______ 克。
(10)下列说法正确的是 。
(一)化学与自然
(1)“水循环”、“氧循环”和“碳循环”是自然界中重要的三大循环,下列用化学学科观点分析“碳、氧循环”的说法中,正确的是 (填字母)。
| A.变化观:碳,氧循环能体现自然界中的物质和能量循环 |
| B.守恒观:碳、氧循环过程中各元素守恒,其化合价不变 |
| C.微粒观:绿色植物能使自然界中的氧原子总数增加 |
| D.平衡观:碳、氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定 |
(二)化学与科技
2022年11月29日,神舟十五号飞船再送3名宇航员进入天宫空间站,天宫空间站史无前例迎来6名宇航员在岗。空间站“循环”系统为宇航员提供了氧气。(如1图 )


(3)二氧化碳收集系统可以采用分子筛或固态胺。其中分子筛表面布满孔穴,类似于活性炭,具有
(4)实验室中模拟水电解系统,装置(如2图 )所示,a管内气体的化学式是
(5)电解后的氢气需要储存,新型镁铝合金(Mg17Al12)是一种储氢材料,在氩气的氛围中,将一定比例的金属镁和铝熔炼得到镁铝合金。熔炼时须通入氩气,其目的是
(6)萨巴蒂尔反应系统:系统的核心部件是萨巴蒂尔反应器。气体在萨巴蒂尔反应器内570-580K的温度下,以及催化剂的作用下反应,试写出萨巴蒂尔反应器中发生反应的化学方程式
(三)化学与生活
目前市售蔬菜农药残留量虽然已达到国家标准,但通过科学的清洗方法仍可进一步降低农药残留。

实验人员分别选取含甲、乙农药的蔬菜,研究了不同清洗方法对农药去除率的影响。
清水浸泡:图1呈现出两种农药的去除率随浸泡时间的变化。
洗洁精清洗:实验选择了6种洗洁精进行测试,结果表明,多数洗洁精对农药的去除率可达到60%以上,最高可达到84%。
碱性溶液浸泡:食用碱(Na2CO3和 NaHCO3)溶液有利于农药分解。图2表示不同浓度的食用碱溶液对农药去除率的影响。希望同学们可以选择科学的清洗方法,更加安全的食用蔬菜。
依据文章内容,回答下列问题。
(7)依据图1分析,去除农药残留的最佳浸泡时间是
(8)食用碱中阳离子是
(9)用食用碱溶液浸泡含有农药甲的蔬菜时,可以选取最佳浓度是
A .15% B. 10% C. 2% D. 8%
配制该浓度的食用碱溶液200克,需要食用碱
(10)下列说法正确的是 。
| A.多数洗洁精对农药的清洗效果比清水浸泡的好 |
| B.采用清水浸泡去除农药的时间越长越好 |
| C.食用碱的去除效果较好,是因为在浸泡过程中农药发生了化学变化 |
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐1】酸碱盐是初中化学学习的重要内容,在生产和生活中有重要的用途
(1)下列物质中,一定含有氧元素的是______(填序号)。
(2)学习小组对中和反应进行探究:将稀盐酸倒入NaOH溶液中,无明显现象,再向混合后的溶液滴加酚酞溶液,溶液不变色。
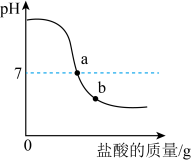
①此时溶液的pH可能位于a点,也可能位于b点,取少量氧化铜粉末加入溶液中,发现______ ,说明溶液pH位于a点。
②若取少量b点溶液蒸干,所得固体为______ 。(填“纯净物”或“混合物”)
③中和反应在工农业生产中有着广泛的应用,如硫酸厂的污水中含有硫酸等,可用熟石灰进行处理,反应的化学方程式为______ 。
(3)化肥已逐渐成为农业增产的措施。常见的化肥有:磷酸钙、碳酸氢铵、硝酸铵、硫酸钾、氯化钾等。
①上述化肥中含有的营养元素有______ 。(填元素名称)
②有一包用剩的肥料,可能是碳酸氢铵、硝酸铵、硫酸钾、氯化钾中的一种或几种,为确定其成分,进行了如下实验:
a.取少量肥料样品于研钵中,加入少量熟石灰混合研磨,有刺激性气味。
b.取少量肥料样品于烧杯中,加水,得到无色溶液A。
c.取少量溶液A于试管中,滴加氯化钡溶液,无明显现象
d.取少量溶液A于试管中,滴加稀盐酸,无明显现象
分析上述实验过程,该肥料中一定含有______ 。
③该肥料中还有一种成分未能证明,请设计实验证明该肥料中含有这种成分______ 。(简要写出操作、现象和结论)
(4)工业上常用纯碱和熟石灰为原料制备烧碱,现要制备10t烧碱,需要含熟石灰50%的石灰浆多少吨?
(1)下列物质中,一定含有氧元素的是______(填序号)。
| A.酸 | B.碱 | C.盐 | D.有机物 |
(2)学习小组对中和反应进行探究:将稀盐酸倒入NaOH溶液中,无明显现象,再向混合后的溶液滴加酚酞溶液,溶液不变色。

①此时溶液的pH可能位于a点,也可能位于b点,取少量氧化铜粉末加入溶液中,发现
②若取少量b点溶液蒸干,所得固体为
③中和反应在工农业生产中有着广泛的应用,如硫酸厂的污水中含有硫酸等,可用熟石灰进行处理,反应的化学方程式为
(3)化肥已逐渐成为农业增产的措施。常见的化肥有:磷酸钙、碳酸氢铵、硝酸铵、硫酸钾、氯化钾等。
①上述化肥中含有的营养元素有
②有一包用剩的肥料,可能是碳酸氢铵、硝酸铵、硫酸钾、氯化钾中的一种或几种,为确定其成分,进行了如下实验:
a.取少量肥料样品于研钵中,加入少量熟石灰混合研磨,有刺激性气味。
b.取少量肥料样品于烧杯中,加水,得到无色溶液A。
c.取少量溶液A于试管中,滴加氯化钡溶液,无明显现象
d.取少量溶液A于试管中,滴加稀盐酸,无明显现象
分析上述实验过程,该肥料中一定含有
③该肥料中还有一种成分未能证明,请设计实验证明该肥料中含有这种成分
(4)工业上常用纯碱和熟石灰为原料制备烧碱,现要制备10t烧碱,需要含熟石灰50%的石灰浆多少吨?
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】Ⅰ、近几年,某小型火力发电厂附近农民利用电厂排出的污水灌溉农田,发现农作物长势不好。当地某校初三年级同学们查阅资料发现:大多数植物在pH>8.0或pH<4的情况下都不适宜种植。针对此情况展开如下探究,请你一起参与。
(1)【提出问题】电厂排放污水的酸碱性怎样?
【作出猜想】猜想一:污水显碱性;猜想二:______
【实验探究】
【实验反思】实验结束后,请你结合实验结论对电厂或有关部门提出以下合理化建议______ 。
Ⅱ、火力发电厂燃烧煤时产生含氧化铝的粉煤灰。回收粉煤灰中氧化铝的一种工艺如下:
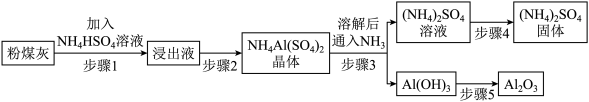
(2)NH4HSO4溶液的作用是溶解氧化铝,说明NH4HSO4溶液中除了有 、
、 外,还含有大量的
外,还含有大量的______ (填粒子符号)。
(3)结合溶解度曲线分析,步骤2采用______ (填“蒸发结晶”或“降温结晶”)可控制只析出NH4Al(SO4)2晶体。图中Q点含义为______
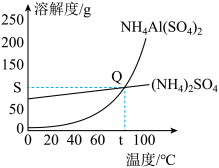
(4)副产物(NH4)2SO4用途广泛,受热不稳定。
①在农业上可用作______ 。
②(NH4)2SO4在280℃可发生分解,产物在步骤1和步骤3中循环利用,将该分解反应的化学方程式补充完整:(NH4)2SO4
______ ↑+ H2SO4。
(5)回收的氧化铝可用于冶炼金属铝。若粉煤灰中含30%的氧化铝,10.2t粉煤灰可冶炼得到金属铝的质量为______ t。
(1)【提出问题】电厂排放污水的酸碱性怎样?
【作出猜想】猜想一:污水显碱性;猜想二:
【实验探究】
实验方案 | 实验现象与化学方程式 | 实验结论 |
方案l:用 | 测得pH=5 | 猜想二正确 |
方案2:取少量污水于一支试管中, 向其中加入 | 实验现象:产生气泡 |
Ⅱ、火力发电厂燃烧煤时产生含氧化铝的粉煤灰。回收粉煤灰中氧化铝的一种工艺如下:

(2)NH4HSO4溶液的作用是溶解氧化铝,说明NH4HSO4溶液中除了有
 、
、 外,还含有大量的
外,还含有大量的(3)结合溶解度曲线分析,步骤2采用

(4)副产物(NH4)2SO4用途广泛,受热不稳定。
①在农业上可用作
②(NH4)2SO4在280℃可发生分解,产物在步骤1和步骤3中循环利用,将该分解反应的化学方程式补充完整:(NH4)2SO4

(5)回收的氧化铝可用于冶炼金属铝。若粉煤灰中含30%的氧化铝,10.2t粉煤灰可冶炼得到金属铝的质量为
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐3】某氮肥硫酸铵中混有硫酸氢铵。为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用。已知:
氢氧化钠少量时2NH4HSO4+2NaOH=(NH4)2SO4+Na2SO4+2H2O
氢氧化钠过量时NH4HSO4+2NaOH=Na2SO4+X+2H2O
(1)根据上述信息,回答下列问题
①氢氧化钠过量时NH4HSO4+2NaOH=Na2SO4+X+2H2O,该反应中X的化学式为________ 。
②“化肥用得巧,庄稼‘身体好’”,下列物质可作为植物生长所需肥料的是______ 。
(2)氨气是一种无色、有强烈刺激性气味的气体,极易溶于水.水溶液呈碱性.实验室常用加热氯化铵和熟石灰两种固体混合物来制取氨气.某兴趣小组的同学设计如图G~J所示装置对氨气的制取、性质进行探究.
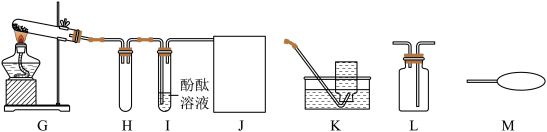
①装置I中的现象是__ 。②装置H的作用是___ 。
③根据氨气的性质,J处应选择的最佳收集装置为__ .(填“K”、“L”或“M”)
(3)同学们设计的实验装置图如右,请回答相关问题。
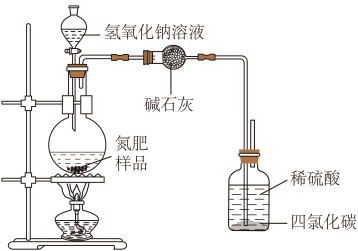
①装置中碱石灰的作用是__________ ,广口瓶内四氯化碳的作用是_________ 。
②指导老师指出,用该装置进行实验,即使氢氧化钠足量且实验过程中无氨气外逸,测得的样品含氮量仍将偏低,其原因可能是__________________________ 。
(4)同学们改进实验装置后(改进装置图略),进行如下实验。
称取不同质量的上述样品分别与100g相同浓度的氢氧化钠溶液混合,完全溶解后,加热充分反应(此温度下铵盐不分解),并使生成的氨气全部被稀硫酸吸收,测得氨气的质量。部分实验数据如下:
请计算(计算结果保留两位小数):样品中氮元素的质量分数是_________ %。
氢氧化钠少量时2NH4HSO4+2NaOH=(NH4)2SO4+Na2SO4+2H2O
氢氧化钠过量时NH4HSO4+2NaOH=Na2SO4+X+2H2O
(1)根据上述信息,回答下列问题
①氢氧化钠过量时NH4HSO4+2NaOH=Na2SO4+X+2H2O,该反应中X的化学式为
②“化肥用得巧,庄稼‘身体好’”,下列物质可作为植物生长所需肥料的是
| A.CaCl2 | B.Ca3(PO4)2 | C.K2CO3 | D.KNO3 |

①装置I中的现象是
③根据氨气的性质,J处应选择的最佳收集装置为
(3)同学们设计的实验装置图如右,请回答相关问题。

①装置中碱石灰的作用是
②指导老师指出,用该装置进行实验,即使氢氧化钠足量且实验过程中无氨气外逸,测得的样品含氮量仍将偏低,其原因可能是
(4)同学们改进实验装置后(改进装置图略),进行如下实验。
称取不同质量的上述样品分别与100g相同浓度的氢氧化钠溶液混合,完全溶解后,加热充分反应(此温度下铵盐不分解),并使生成的氨气全部被稀硫酸吸收,测得氨气的质量。部分实验数据如下:
| 氢氧化钠溶液的质量(g) | 100 | ||
| 样品质量(g) | 7.750 | 15.50 | 23.25 |
| 氨气质量(g) | 1.870 | 1.870 | 1.700 |
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐1】浩瀚大海给我们提供很多资源,海水中含有大量氯化钠,工业上可以用氯化钠原料来制取碳酸钠、氢氧化钠、氯气和盐酸等。
(1)海水晒盐是海水在常温下蒸发得到氯化钠的过程,实验室用氯化钠溶液模拟该过程:

根据上图所示现象,与B 溶液中溶质质量相等的溶液是_____ (填字母);一定是饱和溶液的是_____ (填字母)。
(2)氯化钠、硝酸钾、硫酸钠的溶解度曲线如图所示。40℃时,在三个各盛有 100g 水的容器中分别加入甲、乙、丙三种纯净物(不含结晶水,不与水反应)各 55g,充分溶解后,情况如下表:
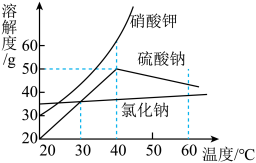
则 40℃时甲物质的溶解度是_____ ;物质丙是_____ (填化学式)。
(3)为了除去氯化钠固体中混有的少量硫酸钠杂质,我们可以先把固体放入适量的水中全部溶解, 然后进行下列选项中的操作________ (填字母),紧接着再进行操作________ (填字母)得到较纯净的氯化钠固体。
A 加热蒸发至出现较多固体时,停止加热,利用余热使液体蒸干
B 加热蒸发至剩余少量液体
C 过滤后取滤液
D 过滤后取滤渣
(4)工业上把浓海水除钙后,再加入碱性沉淀剂可以制备氢氧化镁。若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度。某研究小组在控制反应温度是 20~25℃和浓海水质量为 1109g 不变的条件下,进行下述对比实验, 数据如下:
①进行实验c和d 的目的是_____ 。
②搅拌速率越快,反应时间越长,则消耗能源越多。为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件。在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是________ (填选项)。
A 200r/min,3.5h B 200r/min,4.5h C 175 r/min,4h D 175 r/min,3.5h
(1)海水晒盐是海水在常温下蒸发得到氯化钠的过程,实验室用氯化钠溶液模拟该过程:

根据上图所示现象,与B 溶液中溶质质量相等的溶液是
(2)氯化钠、硝酸钾、硫酸钠的溶解度曲线如图所示。40℃时,在三个各盛有 100g 水的容器中分别加入甲、乙、丙三种纯净物(不含结晶水,不与水反应)各 55g,充分溶解后,情况如下表:
| 物质 | 甲 | 乙 | 丙 |
| 未溶解固体的质量/g | 19 | 5 | 0 |

则 40℃时甲物质的溶解度是
(3)为了除去氯化钠固体中混有的少量硫酸钠杂质,我们可以先把固体放入适量的水中全部溶解, 然后进行下列选项中的操作
A 加热蒸发至出现较多固体时,停止加热,利用余热使液体蒸干
B 加热蒸发至剩余少量液体
C 过滤后取滤液
D 过滤后取滤渣
(4)工业上把浓海水除钙后,再加入碱性沉淀剂可以制备氢氧化镁。若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度。某研究小组在控制反应温度是 20~25℃和浓海水质量为 1109g 不变的条件下,进行下述对比实验, 数据如下:
| 实验 | 碳酸钠加入量/g | 搅拌速度. r/min | 反应时间/h | 钙除去率/% |
| a | 1.78 | 200 | 3 | 44.8 |
| b | 2.32 | 200 | 3 | 60.2 |
| c | 2.32 | 125 | 4 | 55.1 |
| d | 2.32 | 200 | 4 | 64.6 |
②搅拌速率越快,反应时间越长,则消耗能源越多。为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件。在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是
A 200r/min,3.5h B 200r/min,4.5h C 175 r/min,4h D 175 r/min,3.5h
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】为了除去粗食盐中所含有的CaCl2、MgSO4杂质,某化学小组设计了如下实验步骤:①将粗食盐溶于水;②加入过量的X溶液;③加入过量的Na2CO3溶液;④过滤;③向滤液中加入适量盐酸;⑥蒸发、结晶。
(1)请确定X的化学式___________ 。
(2)写出加入Na2CO3溶液时发生反应的化学方程式。(写出一个即可)
(3)操作过程步骤6中用到玻璃棒的作用是___________ 。
(4)请设计实验证明过滤后溶液中既有氢氧化钠又有碳酸钠(写出步骤、现象) 。
(5)某固体氢氧化钠在空气中敞口放置一段时间后部分变质,取10g该固体,加入质量分数为9%的盐酸至不再产生气泡,共产生气体质量为2.2g。试计算固体中氢氧化钠的质量分数。
(1)请确定X的化学式
(2)写出加入Na2CO3溶液时发生反应的化学方程式。(写出一个即可)
(3)操作过程步骤6中用到玻璃棒的作用是
(4)请设计实验证明过滤后溶液中既有氢氧化钠又有碳酸钠(写出步骤、现象) 。
(5)某固体氢氧化钠在空气中敞口放置一段时间后部分变质,取10g该固体,加入质量分数为9%的盐酸至不再产生气泡,共产生气体质量为2.2g。试计算固体中氢氧化钠的质量分数。
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】21世纪是海洋开发与利用的世纪。烟台的“十二五”规划确立了“蓝色经济”发展战略,海洋化学资源的综合利用将是重点发展领域之一。
(1)海水淡化:蒸馏法淡化海水是利用海水中各成份的_________ 不同分离出淡水;高压反渗透膜法淡化海水是利用海水中各成份的_________ 不同分离出淡水。
(2)制盐:①制粗盐。从卤水中提取粗盐用的结晶方法是__________ 。
②粗盐提纯。粗盐中含有泥沙、硫酸镁、氯化钙等杂质。将粗盐溶于水,然后通过如下操作即可得到较纯的氯化钠:a过滤;b加过量的Ba(OH)2溶液;c加适量的盐酸;d加过量的Na2CO3溶液;e蒸发。正确的操作顺序是________ (填字母)。以上操作加入过量的Ba(OH)2溶液的作用是________ (用化学方程式表示)。
(3)制镁:工业上一般用电解熔融状态的氯化镁制金属镁,若以卤水(含有氯化镁、氯化钠和氯化钙)和石灰乳为起始原料来制取金属镁,请画出制镁的流程图:__________ 。写出该流程中属于中和反应的化学方程式为__________ 。利用苦卤制取氢氧化镁比“直接向海水中加入石灰乳制取氢氧化镁”的优势是_________ 。
(1)海水淡化:蒸馏法淡化海水是利用海水中各成份的
(2)制盐:①制粗盐。从卤水中提取粗盐用的结晶方法是
②粗盐提纯。粗盐中含有泥沙、硫酸镁、氯化钙等杂质。将粗盐溶于水,然后通过如下操作即可得到较纯的氯化钠:a过滤;b加过量的Ba(OH)2溶液;c加适量的盐酸;d加过量的Na2CO3溶液;e蒸发。正确的操作顺序是
(3)制镁:工业上一般用电解熔融状态的氯化镁制金属镁,若以卤水(含有氯化镁、氯化钠和氯化钙)和石灰乳为起始原料来制取金属镁,请画出制镁的流程图:
您最近一年使用:0次



