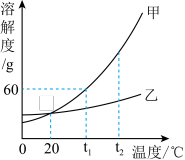
如图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:
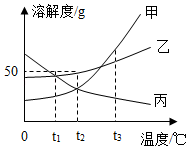
(1)t3℃时,甲、乙、丙三种物质的溶解度大小关系是_____ (用“甲”、“乙”,“丙”及“>”、“<”或“=”表示);
(2)t2℃时,乙物质的饱和溶液中溶质、溶剂的质量之比为_____ (填最简整数比)。
(3)欲配制相同质量分数的乙,丙饱和溶液,应保持温度在_____ ℃;
(4)将t3℃时甲、乙、丙三种物质的饱和溶液各100g,分别降温至t1℃,所得溶液质量的大小关系是_____ (用“甲”、“乙”,“丙”及“>”“<”或“=”表示)。

(1)t3℃时,甲、乙、丙三种物质的溶解度大小关系是
(2)t2℃时,乙物质的饱和溶液中溶质、溶剂的质量之比为
(3)欲配制相同质量分数的乙,丙饱和溶液,应保持温度在
(4)将t3℃时甲、乙、丙三种物质的饱和溶液各100g,分别降温至t1℃,所得溶液质量的大小关系是
2019·辽宁营口·中考真题 查看更多[4]
辽宁省营口市2019年中考化学试题(已下线)必刷卷02-2021年中考化学考前信息必刷卷(兰州专用)辽宁省营口市西市区营口市实验中学2020-2021学年九年级下学期期中化学试题2021年辽宁省营口市鲅鱼圈区中考一模化学试题
更新时间:2019-07-24 17:20:50
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
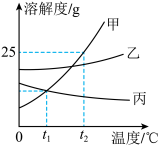
【推荐1】甲、乙、丙三种固体物质的溶解度曲线如图所示:___________ ℃时,甲、丙两种物质的溶解度相等。
(2)t2°C时,向盛有25g甲物质的烧杯中加入50g水,充分溶解后,所得溶液质量为_______ 。
(3)若乙物质中混有少量甲物质,最好采用______ (填“降温结晶”“蒸发结晶”)的方法提纯。
(4)在没有称量仪器的条件下,想配制t2℃时20%的甲溶液,你的方法是___________ 。
(5)t2℃时,甲、乙、丙三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是___ 。
(2)t2°C时,向盛有25g甲物质的烧杯中加入50g水,充分溶解后,所得溶液质量为
(3)若乙物质中混有少量甲物质,最好采用
(4)在没有称量仪器的条件下,想配制t2℃时20%的甲溶液,你的方法是
(5)t2℃时,甲、乙、丙三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是
您最近一年使用:0次
【推荐2】列表法和作图法是常用的数据处理方法,已知KNO3和KC1在不同温度时的溶解度如表所示,请回答下列问题:
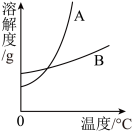
(1)依据如表数据,绘制KNO3和KC1的溶解度曲线,如图中能表示KNO3溶解度曲线的是______ (填“A”或“B”)。
(2)分析表中数据可知,KNO3和KC1在某一温度时具有相同的溶解度,则这一温度的取值范围是__________ 。
(3)40℃时,将140 gKC1的饱和溶液恒温蒸发10g水后,剩余溶液的质量为_______ g。
(4)要使A物质的不饱和溶液转化为饱和溶液,方法是__________ 。
(5)分别将60℃时KNO3和KC1的饱和溶液降温至20℃,析出晶体质量关系为 。

| 温度/g | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KC1 | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
(1)依据如表数据,绘制KNO3和KC1的溶解度曲线,如图中能表示KNO3溶解度曲线的是
(2)分析表中数据可知,KNO3和KC1在某一温度时具有相同的溶解度,则这一温度的取值范围是
(3)40℃时,将140 gKC1的饱和溶液恒温蒸发10g水后,剩余溶液的质量为
(4)要使A物质的不饱和溶液转化为饱和溶液,方法是
(5)分别将60℃时KNO3和KC1的饱和溶液降温至20℃,析出晶体质量关系为 。
| A.KNO3>KCl | B.KNO3<KCl | C.KNO3=KCl | D.无法确定 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】硝酸钾和氯化钾两种物质的溶解度曲线见下图,这两种物质的溶解度见下表。
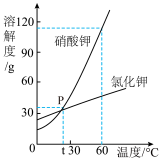
请回答下列问题:
(1)观察溶解度曲线和溶解度表,判断物质乙是指______ (填写化学式)。
(2)图中P点的含义:______
(3)如图所示, 时,将一定质量的硝酸钾固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解。则加入的物质可以是
时,将一定质量的硝酸钾固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解。则加入的物质可以是______ (填写字母标号)。
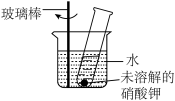
①冰块 ②生石灰固体 ③硝酸铵固体 ④干冰 ⑤氢氧化钠固体
A.③④ B.②⑤ C.①⑤ D.②④
温度 | 10 | 20 | 30 | 40 | 50 | 60 | ||
溶解度 | 甲 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 110 |
| 乙 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 45.5 | |

请回答下列问题:
(1)观察溶解度曲线和溶解度表,判断物质乙是指
(2)图中P点的含义:
(3)如图所示,
 时,将一定质量的硝酸钾固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解。则加入的物质可以是
时,将一定质量的硝酸钾固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解。则加入的物质可以是
①冰块 ②生石灰固体 ③硝酸铵固体 ④干冰 ⑤氢氧化钠固体
A.③④ B.②⑤ C.①⑤ D.②④
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】根据如图中的硝酸钾和氯化钠的溶解度曲线,回答下列问题。
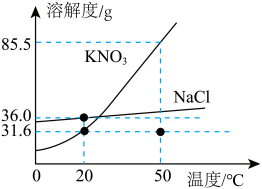
(1)20 ℃时,氯化钠的溶解度是______ g;
(2)50℃时,在50g水中加入65g硝酸钾固体,充分搅拌后得到______ (选填“饱和”或“不饱和”)溶液;
(3)40℃时,硝酸钾饱和溶液和氯化钠饱和溶液各100g,分别蒸发掉10g水,恢复至40℃时,______ 饱和溶液析出的晶体较多。

(1)20 ℃时,氯化钠的溶解度是
(2)50℃时,在50g水中加入65g硝酸钾固体,充分搅拌后得到
(3)40℃时,硝酸钾饱和溶液和氯化钠饱和溶液各100g,分别蒸发掉10g水,恢复至40℃时,
您最近一年使用:0次
【推荐2】请回答下列问题。
(1)神舟十三号乘组航天员翟志刚、王亚平、叶光富作为“太空教师”,在空间站开设了“天宫课堂”。他们在轨演示的太空实验,激发起大家追寻“科学梦”“航天梦”的热情。
①航天员王亚平通过化学实验“变”出五色的奥运五环。这个化学实验用到的试剂中有CH3COOH溶液、KI溶液、KIO3溶液、Na2CO3溶液,在这四种溶液的溶质中,属于有机物的是下列的______ (填选项序号之一)。

A.CH3COOH B.KI C.KIO3 D.Na2CO3
②在空间站中有电解水制氧系统,该系统利用循环水制取氧气,从而使氧气可重复供人呼吸,而生成的氢气可以与收集到的CO2在特殊反应器内转化为水和甲烷(CH4)。

a.在18kg水中,含有氧元素的质量为_______ kg。
b.写出氢气与二氧化碳在催化剂作用下反应生成水和甲烷(CH4)的化学方程式:_______ 。
(2)我国著名化学家侯德榜先生创立了联合制碱法,促进了世界制碱技术的发展。Na2CO3和NaCl的溶解度曲线如右图所示,试回答下列问题:

①t1℃时,Na2CO3的溶解度为_________ g。
②t1℃时,向50g水中加入6gNa2CO3固体,经搅拌充分溶解,所得溶液中溶质与溶剂的质量之比为_____ (填最简整数比)。
③将t2℃时相同质量的Na2CO3饱和溶液和NaCl饱和溶液均降温至t1℃,此时所得两溶液的溶质质量分数相比较为______ (选填“前者大”“后者大”“相等”之一)。
(1)神舟十三号乘组航天员翟志刚、王亚平、叶光富作为“太空教师”,在空间站开设了“天宫课堂”。他们在轨演示的太空实验,激发起大家追寻“科学梦”“航天梦”的热情。
①航天员王亚平通过化学实验“变”出五色的奥运五环。这个化学实验用到的试剂中有CH3COOH溶液、KI溶液、KIO3溶液、Na2CO3溶液,在这四种溶液的溶质中,属于有机物的是下列的

A.CH3COOH B.KI C.KIO3 D.Na2CO3
②在空间站中有电解水制氧系统,该系统利用循环水制取氧气,从而使氧气可重复供人呼吸,而生成的氢气可以与收集到的CO2在特殊反应器内转化为水和甲烷(CH4)。

a.在18kg水中,含有氧元素的质量为
b.写出氢气与二氧化碳在催化剂作用下反应生成水和甲烷(CH4)的化学方程式:
(2)我国著名化学家侯德榜先生创立了联合制碱法,促进了世界制碱技术的发展。Na2CO3和NaCl的溶解度曲线如右图所示,试回答下列问题:

①t1℃时,Na2CO3的溶解度为
②t1℃时,向50g水中加入6gNa2CO3固体,经搅拌充分溶解,所得溶液中溶质与溶剂的质量之比为
③将t2℃时相同质量的Na2CO3饱和溶液和NaCl饱和溶液均降温至t1℃,此时所得两溶液的溶质质量分数相比较为
您最近一年使用:0次
【推荐1】20℃时,将等质量的甲、乙两种固体(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图中①所示,加热到50℃时现象如图②所示,甲、乙两种物质的溶解度曲线如图③所示。

请回答下列问题。
(1)图①中一定是饱和溶液的是________ (填“甲”或“乙”)溶液;图②中乙溶液一定是________ (填“饱和”或“不饱和”)溶液。
(2)图③中表示乙的溶解度曲线的是________ (填“M”或“N”);图②中乙溶液降温至30℃________ (填“会”或“不会”)析出晶体。
(3)50℃时甲的饱和溶液中溶质质量分数为________ 。

请回答下列问题。
(1)图①中一定是饱和溶液的是
(2)图③中表示乙的溶解度曲线的是
(3)50℃时甲的饱和溶液中溶质质量分数为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】如图是甲、乙两种固体物质的溶解度曲线,请回答:
(1)在___ 时,甲、乙两种物质的溶解度相同。
(2)不改变溶剂的质量,将t1℃甲的饱和溶液变为不饱和溶液可 采用方法是___ 。
(3)t2℃时,将25g甲放入装有100g水中,充分搅拌发现固体先全部溶解,一段时间后又有晶体析出,请解释甲固体全部溶解的原因___ 。
(4)下列有关说法正确的是___ (填序号)。
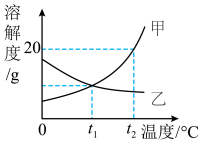
①甲中含有少量的乙可采用降温结晶的方法提纯甲
②t2℃时,甲溶液的溶质质量分数比乙溶液溶质质量分数大
③t2℃时,将等质量甲、乙分别加水配成饱和溶液,所得甲溶液质量比乙溶液小
④将t2℃时甲、乙饱和溶液降温至t1℃时,所得甲、乙溶液的溶质质量分数相等
⑤将t2℃时120g甲的饱和溶液降温至t1℃时,可析出20g甲晶体
(1)在
(2)不改变溶剂的质量,将t1℃甲的饱和溶液变为不饱和溶液可 采用方法是
(3)t2℃时,将25g甲放入装有100g水中,充分搅拌发现固体先全部溶解,一段时间后又有晶体析出,请解释甲固体全部溶解的原因
(4)下列有关说法正确的是

①甲中含有少量的乙可采用降温结晶的方法提纯甲
②t2℃时,甲溶液的溶质质量分数比乙溶液溶质质量分数大
③t2℃时,将等质量甲、乙分别加水配成饱和溶液,所得甲溶液质量比乙溶液小
④将t2℃时甲、乙饱和溶液降温至t1℃时,所得甲、乙溶液的溶质质量分数相等
⑤将t2℃时120g甲的饱和溶液降温至t1℃时,可析出20g甲晶体
您最近一年使用:0次
【推荐3】溶液与人们日常生活密切相关。
(1)衣服上不慎粘上油污,可选用_____ (填“汽油”或“洗洁精”)轻松将其溶解而除去。
(2)农业上常用氯化钠溶液选用颗粒饱满的种子,以确保发芽率和苗木壮实。现需要配制2000g溶质质量为11%的氯化钠溶液,则需要称取固体的质量为_____ g。
(3)现有a、b两种固体物质,其溶解度曲线如图所示。结合图示完成下列问题。
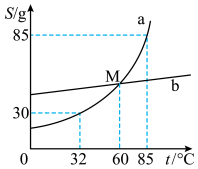
①在保持85℃不变的前提下,将b物质的不饱和溶液转化为饱和溶液的方法为_____ 。
②在32℃时,将30g的a物质放入50g水中,所得溶液的质量为_____ 。
(1)衣服上不慎粘上油污,可选用
(2)农业上常用氯化钠溶液选用颗粒饱满的种子,以确保发芽率和苗木壮实。现需要配制2000g溶质质量为11%的氯化钠溶液,则需要称取固体的质量为
(3)现有a、b两种固体物质,其溶解度曲线如图所示。结合图示完成下列问题。

①在保持85℃不变的前提下,将b物质的不饱和溶液转化为饱和溶液的方法为
②在32℃时,将30g的a物质放入50g水中,所得溶液的质量为
您最近一年使用:0次