某兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金,将60g稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到实验数据如下。
(1)从以上数据可知,最后剩余的0.6g固体的成分是______;这六次实验中,第______次加入稀硫酸时样品中的镁已经完全反应;表格中,m=______。
(2)计算合金样品中镁的质量分数。_____________
(3)计算所用稀硫酸中 的质量分数。__________
的质量分数。__________
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g |  |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | l.0g |
| 第五次加入l0g | 0.6g |
| 第六次加入l0g | 0.6g |
(1)从以上数据可知,最后剩余的0.6g固体的成分是______;这六次实验中,第______次加入稀硫酸时样品中的镁已经完全反应;表格中,m=______。
(2)计算合金样品中镁的质量分数。_____________
(3)计算所用稀硫酸中
 的质量分数。__________
的质量分数。__________
更新时间:2019-08-19 10:38:13
|
相似题推荐
计算题
|
适中
(0.65)
真题
解题方法
【推荐1】为了分析铁粉和铜粉混合物样品的组成,某同学称取12.0g样品,加入到足量的稀H2SO4溶液中,充分反应完全后,过滤、洗涤、干燥,称量剩余固体的质量为3.6g。
(1)样品中铁粉的质量为_____ g。
(2)若在上述反应条件时H2的密度为0.09g/L,试计算产生H2的体积(写出详细的计算过程,保留小数点后一位)。
(1)样品中铁粉的质量为
(2)若在上述反应条件时H2的密度为0.09g/L,试计算产生H2的体积(写出详细的计算过程,保留小数点后一位)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】日常生活中接触的金属材料,大多属于合金。其中黄铜是以锌作主要添加元素的铜合金。已知组成某弹壳的黄铜中只含有锌和铜,现将22 g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示。试计算:

(1)由题意可知,反应生成氢气的质量共_____ g;
(2)弹壳中铜的质量(精确至0.1)
(3)若欲计算反应后所得溶液的质量,你认为至少还应该补充的一个条件是_________________ 。

(1)由题意可知,反应生成氢气的质量共
(2)弹壳中铜的质量(精确至0.1)
(3)若欲计算反应后所得溶液的质量,你认为至少还应该补充的一个条件是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】小王同学取适量Cu-Zn合金粉末,向其中逐渐加入一定溶质质量分数的稀硫酸,所加稀硫酸与生成氢气的质量关系如图所示。请完成下列分析及计算:
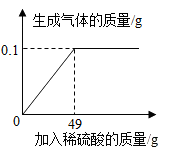
(1)反应生成氢气的总质量为______ g。
(2)求该硫酸溶液溶质的质量分数。

(1)反应生成氢气的总质量为
(2)求该硫酸溶液溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】向34g过氧化氢溶液中加入1g二氧化锰粉末。反应开始后产生氧气的总质量随时间的变化关系如图所示,请回答:
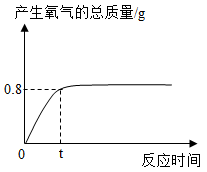
(1)从反应开始到t时,产生氧气的总质量是_________ g。
(2)请计算该过氧化氢溶液的溶质质量分数。

(1)从反应开始到t时,产生氧气的总质量是
(2)请计算该过氧化氢溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】为测定部分变质的NaOH溶液中的NaOH质量分数,取该溶液100g,向其中加入7.3%的稀盐酸,产生气体与加入稀盐酸的关系如图所示. 计算溶液中NaOH的质量分数.(写出计算过程)
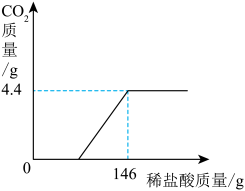

您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】为测定某盐酸的溶质质量分数,化学兴趣小组在200g碳酸钠溶液中,逐滴加入盐酸,记录所加盐酸的质量与产生气体的质量关系如图所示(不考虑气体的溶解和盐酸的挥发)。

试计算:
(1)m点溶液的pH______ 7(填“<”“>”或“=”);
(2)所用盐酸的溶质质量分数。

试计算:
(1)m点溶液的pH
(2)所用盐酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将10.6g碳酸钠加入水中形成50g溶液,然后向此溶液中加入一定量氯化钙溶液恰好完全反应,过滤后得溶液质量为151g。请计算所用氯化钙溶液的质量分数。(写计算过程)
您最近一年使用:0次



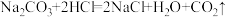 ]
]


