化学小组同学发现在面包制作过程中加入了一些白色粉末,使面包变得松软。同学们对白色粉末的成分进行探究。
【查阅资料】①经调查,市场上有以下3种主要产品。
②2NaHCO3 Na2CO3+H2O+CO2↑;NH4HCO3
Na2CO3+H2O+CO2↑;NH4HCO3 NH3↑+H2O+CO2↑;2NH3+H2SO4=(NH4)2SO4
NH3↑+H2O+CO2↑;2NH3+H2SO4=(NH4)2SO4
【实验准备】同学们选用下列实验装置,经组合进行实验:
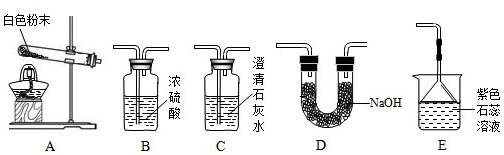
【实验记录】
【实验分析】
根据上述实验,甲同学认为该粉末的主要成分为食臭粉,乙同学认为上述实验不能确定该粉末为食臭粉。为进一步确认其组成及含量,同学们设计了如下定量实验:
(1)实验3中装置B的作用是_____ 。
(2)实验3中测得装置D增重ag,则a>_____ g。
(3)若测得a为92.4,该碱性膨松剂中NaHCO3与NH4HCO3的质量比为_____
【查阅资料】①经调查,市场上有以下3种主要产品。
| 商品名称 | 小苏打 | 食臭粉 | 混合碱性膨松剂 |
| 主要成分 | 碳酸氢钠 | 碳酸氢铵 | 碳酸氢钠和碳酸氢铵 |
②2NaHCO3
 Na2CO3+H2O+CO2↑;NH4HCO3
Na2CO3+H2O+CO2↑;NH4HCO3 NH3↑+H2O+CO2↑;2NH3+H2SO4=(NH4)2SO4
NH3↑+H2O+CO2↑;2NH3+H2SO4=(NH4)2SO4【实验准备】同学们选用下列实验装置,经组合进行实验:

【实验记录】
| 实验序号 | 实验装置 | 实验现象 | 实验结论及分析 |
| 实验1 | 选用A、B、C | C中澄清石灰水变浑浊 | 有CO2生成,C中反应的化学方程式是 |
| 实验2 | 选用A、 | E中紫色石蕊溶液变 | 有NH3生成 |
【实验分析】
根据上述实验,甲同学认为该粉末的主要成分为食臭粉,乙同学认为上述实验不能确定该粉末为食臭粉。为进一步确认其组成及含量,同学们设计了如下定量实验:
| 实验序号 | 实验目的 | 实验装置 | 数据记录 | 实验结论 |
| 实验3 | 测定生成CO2的质量 | 选用A、B、D | 装置D增重ag | 该粉末为“混合碱性膨松剂” |
| 实验4 | 测定生成NH3的质量 | 选用A、D、B | 装置B增重1.7g |
(1)实验3中装置B的作用是
(2)实验3中测得装置D增重ag,则a>
(3)若测得a为92.4,该碱性膨松剂中NaHCO3与NH4HCO3的质量比为
更新时间:2019-11-16 16:40:09
|
相似题推荐
科学探究题
|
较难
(0.4)
【推荐1】某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.
[查阅资料]
[实验探究]
(1)探究两者水溶液酸碱性的差异
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变_____ 色,但食用纯碱溶液中颜色更深,由此推测可能_____ 溶液碱性更强.小欢认为要比较两种溶液的碱性强弱,可直接用_____ 进行测定.
(2)验证两种粉末的稳定性
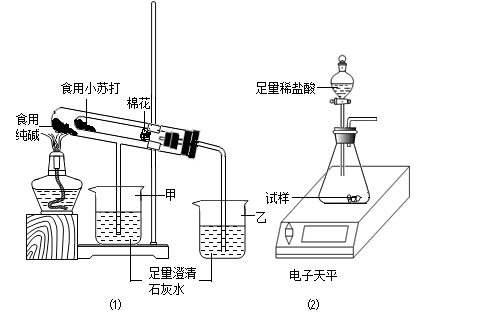
在老师的指导下,该小组按如图1装置进行实验操作,观察到_____ (填“甲”或“乙”)烧杯中澄清石灰水变浑浊,试管中发生反应的化学方程式为_____ ,装置中棉花的作用是_____ .
(3)测定食用纯碱粉末的纯度
取食用纯碱粉末试样,利用如图2装置进行实验测定.
数据记录如下:
①反应生成CO2的质量为_____ g.
②通过计算确定食用纯碱粉末中Na2CO3的质量分数____ .(写出计算过程,结果保留一位小数.)
③如果测得的结果比实际纯度高,可能的原因是_____ .(答一种即可)

[查阅资料]
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
[实验探究]
(1)探究两者水溶液酸碱性的差异
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变
(2)验证两种粉末的稳定性
在老师的指导下,该小组按如图1装置进行实验操作,观察到
(3)测定食用纯碱粉末的纯度
取食用纯碱粉末试样,利用如图2装置进行实验测定.
数据记录如下:
| 称量项目 | 称量时间 | 质量/g |
| 试样 | 11.0 | |
| 装置+稀盐酸 | 160.0 | |
| 装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+试样 | 反应开始后90s | 166.6 |
①反应生成CO2的质量为
②通过计算确定食用纯碱粉末中Na2CO3的质量分数
③如果测得的结果比实际纯度高,可能的原因是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐2】某化学兴趣小组同学将二氧化碳通入室温下(20℃)氢氧化钠的饱和溶液中,观察到有白色沉淀生成,过滤得到白色固体和无色滤液,他们对无色滤液的溶质成分进行如下探究:
【查阅资料】(1)
(2)NaHCO3能与NaOH发生反应: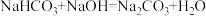
(3)通常情况下,CaCl2溶液与NaHCO3溶液混合无明显现象。
(4)20℃时NaOH、Na2CO3、NaHCO3在水中的溶解度
(5)碳酸氢钠受热易分解:
【提出问题】无色滤液中的溶质有哪些物质?
【作出猜想】猜想一:有NaOH猜想二:有Na2CO3猜想三:有NaHCO3
【实验探究】
结论:无色滤液中的溶质成分为_______ (填化学式)。
【拓展延伸】经过进一步实验,同学们确定了过滤得到的白色固体中也含有NaHCO3,为确定白色固体中NaHCO3的质量分数,兴趣小组同学另取5.00g白色固体完成如下实验。

(1)装置B中盛装的药品是_______ (填名称)。
(2)装置D的作用是_______ 。
(3)实验结束后测得装置C增重0.22g,则白色固体中NaHCO3的质量分数为_______ %(结果精确到0.1%)。
【查阅资料】(1)

(2)NaHCO3能与NaOH发生反应:
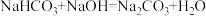
(3)通常情况下,CaCl2溶液与NaHCO3溶液混合无明显现象。
(4)20℃时NaOH、Na2CO3、NaHCO3在水中的溶解度
| 物质 | NaOH | Na2CO3 | NaHCO3 |
| 溶解度 | 109g | 21.5g | 9.6g |

【提出问题】无色滤液中的溶质有哪些物质?
【作出猜想】猜想一:有NaOH猜想二:有Na2CO3猜想三:有NaHCO3
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 取无色滤液于试管中,加入过量CaCl2溶液 | 产生白色沉淀 | 猜想 |
| 实验二 | 取实验一中的上层清液滴加适量稀盐酸 | 猜想三成立 |
【拓展延伸】经过进一步实验,同学们确定了过滤得到的白色固体中也含有NaHCO3,为确定白色固体中NaHCO3的质量分数,兴趣小组同学另取5.00g白色固体完成如下实验。

(1)装置B中盛装的药品是
(2)装置D的作用是
(3)实验结束后测得装置C增重0.22g,则白色固体中NaHCO3的质量分数为
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
【推荐3】“84”消毒液在新冠肺炎预防措施中使用较为广泛,其还具有漂白、杀菌、消毒的功效。某化学兴趣小组对 一瓶敞口久置的“84”消毒液的成分产生兴趣,在老师的指导下,展开探究。
已知:“84”消毒液和洁厕灵作用会产生氯气。
【提出问题】该敞口久置的消毒液中溶质有哪些?
【查阅资料】“84”消毒液的主要成分是次氯酸钠(NaClO)和氯化钠;NaClO 为有效成分,有腐蚀性并 易与空气中的 CO2 反应(2NaClO+CO2+H2O==2HClO+Na2CO3)。NaClO溶液、HClO都具有漂白、杀菌、消毒功效。HClO 不稳定,受热或光照条件下会发生分解。
【分析讨论】小组同学经过讨论,认为该消毒液中的溶质一定有____________________ ,可能还有 NaClO、Na2CO3、HClO中的一种或多种。
【实验探究】
【交流反思】生活中,“84”消毒液贮藏时应注意________________ ;一般不用“84”消毒液对蔬菜、水果进行消毒,其原因可能是________________ 。
【拓展延伸】
(1)次氯酸钠与稀硫酸可发生复分解反应,化学方程式为__________________ 。
(2)“84”消毒液______ (“能”或“不能”)与洁厕灵混合使用。
已知:“84”消毒液和洁厕灵作用会产生氯气。
【提出问题】该敞口久置的消毒液中溶质有哪些?
【查阅资料】“84”消毒液的主要成分是次氯酸钠(NaClO)和氯化钠;NaClO 为有效成分,有腐蚀性并 易与空气中的 CO2 反应(2NaClO+CO2+H2O==2HClO+Na2CO3)。NaClO溶液、HClO都具有漂白、杀菌、消毒功效。HClO 不稳定,受热或光照条件下会发生分解。
【分析讨论】小组同学经过讨论,认为该消毒液中的溶质一定有
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| Ⅰ.向装入红色布条的试管中加入适量该消毒液 | 布条长时间不褪色 | 消毒液中不含 |
| Ⅱ.另取少量该消毒液于试管中,滴入氯化钡溶液 | 白色沉淀 | 消毒液中含 |
【交流反思】生活中,“84”消毒液贮藏时应注意
【拓展延伸】
(1)次氯酸钠与稀硫酸可发生复分解反应,化学方程式为
(2)“84”消毒液
您最近一年使用:0次
【推荐1】化学兴趣小组同学绘制了碱的化学性质知识网络图,并选取四种碱来验证,设计实验如下:

(1)实验二中澄清石灰水变浑浊,验证了上述知识网络图中碱能够与______________ 反应。
(2)实验三发生反应的化学方程式为______________ 。
(3)向实验四后的试管中滴加几滴酚酞溶液,观察到的现象是______________ 。
【提出问题】实验四所得滤液中溶质除了氢氧化钠还有什么?同学们对滤液中溶质的成分进行了猜想和实验探究。
【猜想与假设】
(4)猜想一:溶质只有NaOH;
猜想二:溶质为NaOH和______________ 。
猜想三:溶质为NaOH和Ba(OH)2
【实验探究】
(5)
【反思与评价】
(6)I.同学们经过讨论认为,如果向滤液中只加入过量的一种试剂,也能得出猜想一正确的结论,该试剂为______________ 。
Ⅱ.实验后将废液直接倒入下水道,会造成环境污染,需将废液处理后再排放。

(1)实验二中澄清石灰水变浑浊,验证了上述知识网络图中碱能够与
(2)实验三发生反应的化学方程式为
(3)向实验四后的试管中滴加几滴酚酞溶液,观察到的现象是
【提出问题】实验四所得滤液中溶质除了氢氧化钠还有什么?同学们对滤液中溶质的成分进行了猜想和实验探究。
【猜想与假设】
(4)猜想一:溶质只有NaOH;
猜想二:溶质为NaOH和
猜想三:溶质为NaOH和Ba(OH)2
【实验探究】
(5)
| 实验操作 | 实验现象 | 实验结论 |
| a.取少量滤液于试管中,加入过量稀盐酸 | 无明显现象 | 由a、b两个实验的现象,得出猜想一正确。 |
| b.另取少量滤液于试管中,加入过量碳酸钠溶液 |
【反思与评价】
(6)I.同学们经过讨论认为,如果向滤液中只加入过量的一种试剂,也能得出猜想一正确的结论,该试剂为
Ⅱ.实验后将废液直接倒入下水道,会造成环境污染,需将废液处理后再排放。
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐2】小组同学对老师演示的趣味实验“化学红绿灯”兴趣浓厚,并进行了如下探究。
【查阅资料】
靛蓝胭脂红(C16H8N2Na2O8S2),是一种生物染色剂。在碱性条件下与空气成分或葡萄糖反应,会呈现不同颜色。pH不同颜色也不同。
【实验准备】
(1)量取20mL0.05%的靛蓝胭脂红溶液和10mL15%的葡萄糖溶液时,所用仪器为____ 。
(2)为满足碱性条件应使用NaOH溶液
①根据表中数据分析,为了能观察到“红绿灯”的实验现象,NaOH溶液的质量分数应为____ 。
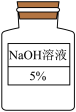
②实验时需使用70mLNaOH溶液(密度约为1g/mL),实验台上有如图所示的NaOH溶液(密度约为1g/mL),为了达到实验效果,应从试剂瓶中取出____ mLNaOH溶液。
(3)向锥形瓶中加入准备好的三种试剂,振荡锥形瓶,溶液颜色发生改变,是因为空气中的____ (填“O2”或“CO2”)氧化了靛蓝胭脂红。
(4)振荡时应该注意的问题是____ 。停止振荡,葡萄糖将靛蓝胭脂红还原,又恢复到原来的颜色。
【交流讨论】
(5)实验进行过程中意外发现试剂瓶中出现了绿→紫→红→橙→黄的现象,小明认为是配制的NaOH溶液质量分数偏低,其原因是实验台上的NaOH溶液放置时间过长,已经变质,该反应的化学方程式为____________ ,为了证明NaOH溶液已经变质,可采用的方法是_____ 。
(6)小红认为NaOH溶液变质,不一定会影响溶液的碱性,其理由是___ 。若想证明氢氧化钠变质是否对“红绿灯”实验有影响,我们还应该知道的信息是_____ 。
【拓展延伸】
(7)“红绿灯”实验变色时间除了受NaOH溶液浓度影响外,还可能存在的影响因素是____ 。
【查阅资料】
靛蓝胭脂红(C16H8N2Na2O8S2),是一种生物染色剂。在碱性条件下与空气成分或葡萄糖反应,会呈现不同颜色。pH不同颜色也不同。
【实验准备】
(1)量取20mL0.05%的靛蓝胭脂红溶液和10mL15%的葡萄糖溶液时,所用仪器为
(2)为满足碱性条件应使用NaOH溶液
| 序号 | 1 | 2 | 3 | 4 |
| NaOH溶液的质量分数/% | 0.4 | 2 | 7.5 | 10 |
| 溶液变色 | 绿→紫→红→橙→黄 | 绿→红→黄 | 黄→红→黄 | 黄 |
| 变色总时间/s | 106 | 43 | 34 | |
| pH | pH<11.4 | 11.4<pH<13 | pH>13 | |
②实验时需使用70mLNaOH溶液(密度约为1g/mL),实验台上有如图所示的NaOH溶液(密度约为1g/mL),为了达到实验效果,应从试剂瓶中取出
(3)向锥形瓶中加入准备好的三种试剂,振荡锥形瓶,溶液颜色发生改变,是因为空气中的
(4)振荡时应该注意的问题是
【交流讨论】
(5)实验进行过程中意外发现试剂瓶中出现了绿→紫→红→橙→黄的现象,小明认为是配制的NaOH溶液质量分数偏低,其原因是实验台上的NaOH溶液放置时间过长,已经变质,该反应的化学方程式为
(6)小红认为NaOH溶液变质,不一定会影响溶液的碱性,其理由是
【拓展延伸】
(7)“红绿灯”实验变色时间除了受NaOH溶液浓度影响外,还可能存在的影响因素是
您最近一年使用:0次
【推荐3】某化学学习小组的同学对一瓶久置的氢氧化钠的化学成分产生了兴趣,他们根据自己已学的知识进行如下探究,请你共同参与并填空:
【猜想假设】
猜想一:只有氢氧化钠
猜想二:是氢氧化钠和碳酸钠的混合物
猜想三:_____ 。
【查阅资料】
(1)BaCl2溶液显中性;
(2)Na2CO3溶液与BaCl2溶液能反应产生白色沉淀。
【实验探究】
【实验结论】
该氢氧化钠样品已部分变质,其化学成分是NaOH与Na2CO3的混合物,引起NaOH变质的化学方程式为_____ 。
【反思交流】
(1)实验室应_____ 保存氢氧化钠。
(2)某同学认为用Ba(OH)2溶液代替BaCl2溶液也可以得到同样的结论,你认为该同学的说法是否正确?_____ (填“正确”或“不正确”)。
【猜想假设】
猜想一:只有氢氧化钠
猜想二:是氢氧化钠和碳酸钠的混合物
猜想三:
【查阅资料】
(1)BaCl2溶液显中性;
(2)Na2CO3溶液与BaCl2溶液能反应产生白色沉淀。
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)用小试管取少量固体样品加水完全溶解,再滴加过量BaCl2溶液 | 产生白色沉淀 | 猜想 |
| (2)取(1)中的少量上层清液于试管中,滴加酚酞溶液 | 猜想二正确、猜想三不正确 |
【实验结论】
该氢氧化钠样品已部分变质,其化学成分是NaOH与Na2CO3的混合物,引起NaOH变质的化学方程式为
【反思交流】
(1)实验室应
(2)某同学认为用Ba(OH)2溶液代替BaCl2溶液也可以得到同样的结论,你认为该同学的说法是否正确?
您最近一年使用:0次



