现有一包Na2CO3和NaOH固体样品,为了测定Na2CO3的质量分数,取该样品20g,加水搅拌至全部溶解.然后逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示。请计算:
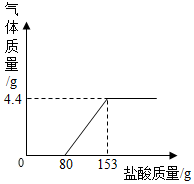
(1)生成气体的质量____;
(2)该样品中Na2CO3的质量分数____;
(3)所用稀盐酸溶质的质量分数____.

(1)生成气体的质量____;
(2)该样品中Na2CO3的质量分数____;
(3)所用稀盐酸溶质的质量分数____.
更新时间:2019-10-12 10:31:52
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】某兴趣小组用如图装置(碱石灰是氧化钙和固体氢氧化钠的混合物,极易吸收水蒸气,经常用作干燥剂),整套装置质量为16克,测定过氧化氢溶液中溶质的质量分数.测得相关数据如下:整套装置16克.
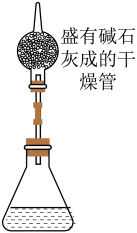
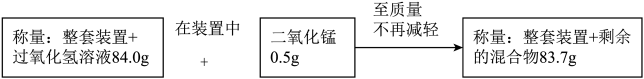
请回答:
(1)双氧水样品中加入二氧化锰,二氧化锰起_____作用,反应生成氧气的物质的量为_____.
(2)计算该过氧化氢溶液中溶质的质量分数._____(写出计算过程)
(3)实验装置中锥形瓶上加接盛有碱石灰的干燥管作用是_____.如果实验装置中不接盛有碱石灰的干燥管,测得的过氧化氢溶液溶质的质量分数会偏大,原因是_____.


请回答:
(1)双氧水样品中加入二氧化锰,二氧化锰起_____作用,反应生成氧气的物质的量为_____.
(2)计算该过氧化氢溶液中溶质的质量分数._____(写出计算过程)
(3)实验装置中锥形瓶上加接盛有碱石灰的干燥管作用是_____.如果实验装置中不接盛有碱石灰的干燥管,测得的过氧化氢溶液溶质的质量分数会偏大,原因是_____.
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组对含有杂质的石灰石样品进行如下实验分析:取12g样品放入烧杯中,将100g稀盐酸分4次加入到烧杯中,充分反应后(杂质不溶于水,也不与酸反应),测得剩余固体的质量记录如下。请计算:
求:(1)m的值;
(2)样品中碳酸钙的质量;
(3)求反应生成的二氧化碳的质量(写出计算过程)。
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
| 剩余固体的质量/g | 8 | 4 | m | 2 |
求:(1)m的值;
(2)样品中碳酸钙的质量;
(3)求反应生成的二氧化碳的质量(写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】某校同学在实验室发现一瓶敞口放置的氢氧化钠固体,她为了测定这瓶氢氧化钠的质量分数,做了如下实验:取瓶中17.3g样品溶于足量的水中,向所得溶液中逐滴加入200g一定溶质质量分数的稀盐酸。实验过程如图所示:

试计算:
(1)恰好完全反应时,产生气体的质量是______ g。
(2)所取样品中除了有氢氧化钠还有的物质是______ (填化学式)。
(3)所加稀盐酸的溶质质量分数是多少?
(4)所取样品中氢氧化钠的质量是______ g。

试计算:
(1)恰好完全反应时,产生气体的质量是
(2)所取样品中除了有氢氧化钠还有的物质是
(3)所加稀盐酸的溶质质量分数是多少?
(4)所取样品中氢氧化钠的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】铅蓄电池放电过程中发生反应的工作原理为: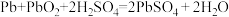 ,现有47.8gPbO2参加反应,需要消耗溶质质量分数为28%的稀硫酸
,现有47.8gPbO2参加反应,需要消耗溶质质量分数为28%的稀硫酸_____ 克?
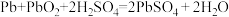 ,现有47.8gPbO2参加反应,需要消耗溶质质量分数为28%的稀硫酸
,现有47.8gPbO2参加反应,需要消耗溶质质量分数为28%的稀硫酸
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
解题方法
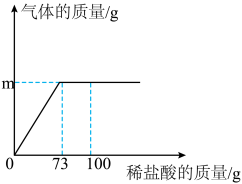
【推荐2】实验室用12.5g含碳酸钙80%的石灰石和一定质量的稀盐酸反应制取二氧化碳〔石灰石中的杂质不溶于水,也不与稀盐酸反应),加入稀盐酸的质量与产生气体的质量关系如图所示,试计算该稀盐酸中溶质的质量分数。

您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】现有100g氯化铜溶液,向其中加入一定溶质质量分数的氢氧化钠溶液,实验过程中生成沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。请计算:

(1)生成沉淀的质量为___________ g。
(2)所用氢氧化钠溶液的溶质质量分数。(写出计算过程,计算结果精确到0.1%)
[温馨提示:2NaOH+CuCl2=Cu(OH)2↓+2NaCl]

(1)生成沉淀的质量为
(2)所用氢氧化钠溶液的溶质质量分数。(写出计算过程,计算结果精确到0.1%)
[温馨提示:2NaOH+CuCl2=Cu(OH)2↓+2NaCl]
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某化学兴趣小组对胃药“碳酸氢钠片”进行了探究,具体做法如下:
Ⅰ.取一片胃药研碎,加水完全溶解得100g溶液;
Ⅱ.配制100g溶质质量分数0.365%的稀盐酸模拟胃酸;
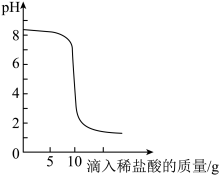
Ⅲ.取上述20g碳酸氢钠溶液加入锥形瓶,再逐滴滴加稀盐酸,
用数据传感技术测得溶液pH变化如图。
请回答下列问题:
(1)碳酸氢钠属于___(填“氧化物““酸”“碱”或“盐”);当滴入稀盐酸质量为5g,混合溶液呈___(填“酸”“碱”或“中”)性。当滴入稀盐酸质量为15g,混合溶液中溶质有____。
(2)用7.3%的稀盐酸配制100g溶质质量分数0.365%的稀盐酸,需要量取___mL蒸馏水。
(3)步骤Ⅲ中向锥形瓶中滴入10g溶质质量分数0.365%稀盐酸时,两种物质恰好完全反应(胃药中其它成份不参加反应)。请依据实验数据计算每片胃药中碳酸氢钠的质量是多少? ___
Ⅰ.取一片胃药研碎,加水完全溶解得100g溶液;
Ⅱ.配制100g溶质质量分数0.365%的稀盐酸模拟胃酸;
Ⅲ.取上述20g碳酸氢钠溶液加入锥形瓶,再逐滴滴加稀盐酸,
用数据传感技术测得溶液pH变化如图。

请回答下列问题:
(1)碳酸氢钠属于___(填“氧化物““酸”“碱”或“盐”);当滴入稀盐酸质量为5g,混合溶液呈___(填“酸”“碱”或“中”)性。当滴入稀盐酸质量为15g,混合溶液中溶质有____。
(2)用7.3%的稀盐酸配制100g溶质质量分数0.365%的稀盐酸,需要量取___mL蒸馏水。
(3)步骤Ⅲ中向锥形瓶中滴入10g溶质质量分数0.365%稀盐酸时,两种物质恰好完全反应(胃药中其它成份不参加反应)。请依据实验数据计算每片胃药中碳酸氢钠的质量是多少? ___
您最近一年使用:0次
【推荐2】金属及金属材料在生产、生活中应用广泛。
(1)铝具有良好的抗腐蚀性,是因为它的表面有一层致密的氧化膜,化学式为_____ ;
(2)向一定质量的氧化铁粉末中加入稀硫酸,恰好完全反应,再向该溶液中加入一定量镁粉,充分反应,取出滤渣,向其中滴加稀盐酸,有气泡产生,则此时滤液中一定有的溶质是_____ ;
(3)钠离子是最常见的阳离子之一,它的用处有很多,例如氯化钠可以调味。过氧化钠(Na2O2)是一种新型材料,常用作防毒面具,其原理是过氧化钠和二氧化碳反应生成可以制肥皂的碱和一种空气中常见且助燃的气体,请你写出其化学反应方程式_____ ;
(4)“芳芳”实验小组模拟湿法炼铜,向50.0gCuSO4溶液中加入10.0g铁粉(铁粉过量),CuSO4完全反应,过滤,称的滤渣的质量是10.4g,组长芳芳物理很好但化学不行,请你来帮忙算一算,原来溶液的质量分数是_____ 。
(1)铝具有良好的抗腐蚀性,是因为它的表面有一层致密的氧化膜,化学式为
(2)向一定质量的氧化铁粉末中加入稀硫酸,恰好完全反应,再向该溶液中加入一定量镁粉,充分反应,取出滤渣,向其中滴加稀盐酸,有气泡产生,则此时滤液中一定有的溶质是
(3)钠离子是最常见的阳离子之一,它的用处有很多,例如氯化钠可以调味。过氧化钠(Na2O2)是一种新型材料,常用作防毒面具,其原理是过氧化钠和二氧化碳反应生成可以制肥皂的碱和一种空气中常见且助燃的气体,请你写出其化学反应方程式
(4)“芳芳”实验小组模拟湿法炼铜,向50.0gCuSO4溶液中加入10.0g铁粉(铁粉过量),CuSO4完全反应,过滤,称的滤渣的质量是10.4g,组长芳芳物理很好但化学不行,请你来帮忙算一算,原来溶液的质量分数是
您最近一年使用:0次



