a、b、c三种固体物质的溶解度曲线如图所示,据图回答问题
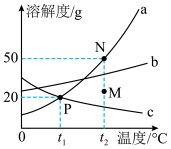
(1)P点的含义_____ ;
(2)t2℃时,将30g的a物质加到50g的水中,形成的溶液的质量为_____ ;
(3)将t1℃的a、b、c三种饱和溶液升温到t2℃,则此时溶液的溶质质量分数由大到小分别为_____ ;
(4)若要除去a中含有的少量b,可采用的方法为_____ 。

(1)P点的含义
(2)t2℃时,将30g的a物质加到50g的水中,形成的溶液的质量为
(3)将t1℃的a、b、c三种饱和溶液升温到t2℃,则此时溶液的溶质质量分数由大到小分别为
(4)若要除去a中含有的少量b,可采用的方法为
更新时间:2019-10-05 22:39:36
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】在做实验时,欣欣用到200g溶质质量分数为15%的氯化钠溶液,但实验室只有50g溶质质量分数为30%的氯化钠溶液,于是她便自己动手并利用已有的溶液来配置所需的氯化钠溶液。
(1)在称量时,她需要把氯化钠固体放到天平垫有纸片的_____ (选填“左侧”或“右侧”)托盘中,并且应当称量 _____ g氯化钠固体
(2)她把称量好的氯化钠和实验室中现有的氯化钠溶液全部转移到一个大烧杯中,并应向其中加入体积为_____ mL的水,边加水边搅拌(水的密度为1.0g/mL)。
(3)如表是氯化钠在不同温度下的溶解度。若此时室温为20℃,经对照,欣欣配置的溶液为_____ (选填“饱和”或“不饱和”)溶液;假如她想通过升高溶液的温度来得到氯化钠晶体,则你认为她的作法_____ (选填“可行”或“不可行”) 。
(1)在称量时,她需要把氯化钠固体放到天平垫有纸片的
(2)她把称量好的氯化钠和实验室中现有的氯化钠溶液全部转移到一个大烧杯中,并应向其中加入体积为
(3)如表是氯化钠在不同温度下的溶解度。若此时室温为20℃,经对照,欣欣配置的溶液为
| 温度/℃ | 20 | 40 | 60 | 80 |
| 溶解度/g | 36.0 | 36.6 | 37.3 | 38.4 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】图1表示M、N两种固体物质的溶解度曲线。试回答下列问题:

(1)t1℃时,M、N物质的溶解度均为_______ g。
(2)t2℃时,向80g水中加入50gM物质充分溶解,所得溶液的质量是_______ g,降到t1℃时析出晶体质量为_______ g。
(3)t2℃时。N物质的饱和溶液降温到t1℃,所得溶液的溶质质量分数_______ (填“变大”“变小”“不变”)。
(4)如图2所示。甲、乙两试管中分别盛有一定温度时M、N的饱和溶液(试管底部分别有少量各自的固体存在)。若向试管外盛有水的烧杯中加入少量浓硫酸。则下列有关说法中错误的是_______ (填序号)。
a.甲试管中固体增多 b.乙试管中固体减少
c.甲试管中溶液的溶质质量分数不变 d.乙试管中溶液仍饱和
(5)当M固体中含有少量N时,可采用_______ 的方法提纯M。

(1)t1℃时,M、N物质的溶解度均为
(2)t2℃时,向80g水中加入50gM物质充分溶解,所得溶液的质量是
(3)t2℃时。N物质的饱和溶液降温到t1℃,所得溶液的溶质质量分数
(4)如图2所示。甲、乙两试管中分别盛有一定温度时M、N的饱和溶液(试管底部分别有少量各自的固体存在)。若向试管外盛有水的烧杯中加入少量浓硫酸。则下列有关说法中错误的是
a.甲试管中固体增多 b.乙试管中固体减少
c.甲试管中溶液的溶质质量分数不变 d.乙试管中溶液仍饱和
(5)当M固体中含有少量N时,可采用
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】下表是硝酸钾和氯化钾的部分溶解度数据,回答下列问题。
(1)30℃,50g水中最多能溶解氯化钾固体的质量为___________ g。
(2)曲线甲是表中___________ (填化学式)的溶解度曲线。
(3)请在图中补充画出另一种物质的溶解度曲线____ 。

(4)将40℃相同质量的硝酸钾、氯化钾饱和溶液分别降温至10℃,___________ 析出的晶体多。
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | |
| 溶解度(g/100g水) | 氯化钾 | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 |
| 硝酸钾 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | |
(2)曲线甲是表中
(3)请在图中补充画出另一种物质的溶解度曲线

(4)将40℃相同质量的硝酸钾、氯化钾饱和溶液分别降温至10℃,
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】化学兴趣小组探究碳酸氢钠、氯化钾、氯化钠和氯化铵的溶解性时,查阅资料如下:
表1物质在不同温度时的溶解度
表2溶解度的相对大小(20℃)
回答下列问题:
(1)10℃时,NaCl的溶解度为______ 。
(2)根据20℃时上述四种物质的溶解度,判断其中属于“可溶”的物质是______ 。
(3)将30℃时上述四种物质的饱和溶液各ag分别降温到0℃,析出同体质量最大的物质是______ 。
(4)20℃时,将氯化钠和氯化铵各mg分别放入两只烧杯中,再分别加入ng水,充分搅拌。下列说法正确的是______。(填标号)
表1物质在不同温度时的溶解度
温度/℃ | 0 | 10 | 20 | 30 | |
溶解度/g | NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | |
溶解度/g | 一般称为 |
<0.01 | 难溶 |
0.01~1 | 微溶 |
1~10 | 可溶 |
>10 | 易溶 |
(1)10℃时,NaCl的溶解度为
(2)根据20℃时上述四种物质的溶解度,判断其中属于“可溶”的物质是
(3)将30℃时上述四种物质的饱和溶液各ag分别降温到0℃,析出同体质量最大的物质是
(4)20℃时,将氯化钠和氯化铵各mg分别放入两只烧杯中,再分别加入ng水,充分搅拌。下列说法正确的是______。(填标号)
| A.若两只烧杯中均无固体剩余,则所得氯化铵溶液一定是不饱和溶液 |
| B.若两只烧杯中均有固体剩余,则所得溶液中溶质的质量分数:氯化铵>氯化钠 |
| C.若m≤0.36,则所得溶液中溶质的质量分数:氯化铵=氯化钠 |
| D.若所得溶液中只有一种是饱和溶液,则0.36n≤m≤0.372n |
您最近一年使用:0次
【推荐3】如图是a、b、c三种物质的溶解度曲线,据图回答下列问题

(1)a、b、c三种物质的溶解度随着温度升高而减小的是______ 。
(2)t3℃时,把80g物质a加入200g水中充分搅拌、静置,形成的是______ (填“饱和”或“不饱和”)溶液。
(3)t3℃时,将等质量a和b的饱和溶液降到t1℃时,析出晶体的质量关系正确的是______(填字母序号)。
(4)如果a中混有少量固体b,若提纯a,一般采用______ 的方法。
(5)将t3℃时a、b、c三种物质的饱和溶液降温到t1℃,所得三种溶液的溶质质量分数大小关系是______ 。

(1)a、b、c三种物质的溶解度随着温度升高而减小的是
(2)t3℃时,把80g物质a加入200g水中充分搅拌、静置,形成的是
(3)t3℃时,将等质量a和b的饱和溶液降到t1℃时,析出晶体的质量关系正确的是______(填字母序号)。
| A.a>b | B.a=b | C.a<b | D.不能确定 |
(5)将t3℃时a、b、c三种物质的饱和溶液降温到t1℃,所得三种溶液的溶质质量分数大小关系是
您最近一年使用:0次
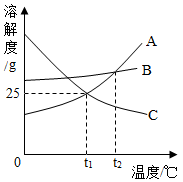
【推荐1】A、B、C三种物质的溶解度曲线如图所示。请回答下列问题:

(1)t1℃时A物质的溶解度是________ 。
(2)在t1℃时,将足量的三种物质的饱和溶液各恒温蒸发10g水后,它们析出的晶体的质量关系为________ (选填序号)。
①B>A=C②A>B>C③B>C>A④C=B=A
(3)在t1℃时,将质量均为25g的上述三种物质分别加入到100g水中,不能形成饱和溶液的是________ 。
(4)写出符合C曲线特点的一种物质的化学式_______ 。
(5)将t2℃的这三种物质的饱和溶液分别降温至t1℃,所得溶液中溶质的质量分数从大到小的颜序是______ (选填序号)。
①A>B>C②B>A>C③B>C>A④C=B=A

(1)t1℃时A物质的溶解度是
(2)在t1℃时,将足量的三种物质的饱和溶液各恒温蒸发10g水后,它们析出的晶体的质量关系为
①B>A=C②A>B>C③B>C>A④C=B=A
(3)在t1℃时,将质量均为25g的上述三种物质分别加入到100g水中,不能形成饱和溶液的是
(4)写出符合C曲线特点的一种物质的化学式
(5)将t2℃的这三种物质的饱和溶液分别降温至t1℃,所得溶液中溶质的质量分数从大到小的颜序是
①A>B>C②B>A>C③B>C>A④C=B=A
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】下图是A、B两种物质的溶解度曲线图。请回答下列问题。

(1)写出P点的含义___________ 。
(2)在t2℃时,A物质的溶解度___________ B物质的溶解度(填“>”、“<”或“=”)。
(3)已知在M点时,A物质的溶液是不饱和溶液,要使其变为饱和溶液的方法有___________ (填一种即可)。

(1)写出P点的含义
(2)在t2℃时,A物质的溶解度
(3)已知在M点时,A物质的溶液是不饱和溶液,要使其变为饱和溶液的方法有
您最近一年使用:0次
【推荐3】图一是a、b、c三种物质的溶解度曲线,据图回答下列问题:

(1)t1℃时,c物质的溶解度为___________ 。
(2)气体的溶解度随温度变化的情况与___________ (填“a”、“b”或“c”)相似。
(3)要使接近饱和的b溶液变为饱和溶液,可呆用的方法有(写出两种方法)___________ 或___________ 。
(4)t3℃时,将150ga的饱和溶液降温到t1℃,析出晶体的质量是___________ g。
(5)t3℃时,将a、b、c三种物质的饱和溶液降温到t1,此时三者质量分数由大到小的关系是___________ 。
(6)取固体a进行如图二实验、属于饱和溶液的是___________ (填字母序号),烧杯C中溶质的质量分数为___________ (精确到0.1%)。
(7)欲配制6%的氯化钠溶液,如图:

①用上述图示的序号表示配制溶液的操作顺序:___________ (填字母序号)。
②经检测,所配制的溶液质量分数偏小,其原因可能是___________ (填字母序号)。
a.称量前天平未调平,指针偏右
b.氯化钠固体不纯
c.量取水时,仰视读数
d.装瓶时,有少量溶液洒出

(1)t1℃时,c物质的溶解度为
(2)气体的溶解度随温度变化的情况与
(3)要使接近饱和的b溶液变为饱和溶液,可呆用的方法有(写出两种方法)
(4)t3℃时,将150ga的饱和溶液降温到t1℃,析出晶体的质量是
(5)t3℃时,将a、b、c三种物质的饱和溶液降温到t1,此时三者质量分数由大到小的关系是
(6)取固体a进行如图二实验、属于饱和溶液的是
(7)欲配制6%的氯化钠溶液,如图:

①用上述图示的序号表示配制溶液的操作顺序:
②经检测,所配制的溶液质量分数偏小,其原因可能是
a.称量前天平未调平,指针偏右
b.氯化钠固体不纯
c.量取水时,仰视读数
d.装瓶时,有少量溶液洒出
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐1】 和
和 的溶解度曲线如图1所示;某化学兴趣小组同学进行了如图2所示实验(忽略水的损失)。根据图示回答下列问题。
的溶解度曲线如图1所示;某化学兴趣小组同学进行了如图2所示实验(忽略水的损失)。根据图示回答下列问题。 时,
时, 的溶解度是
的溶解度是______ g。
(2)烧杯②中的 溶液是
溶液是______ (填“饱和”或“不饱和”)溶液。烧杯④中析出固体的质量是______ g。
(3)下列有关说法正确的是______。
 和
和 的溶解度曲线如图1所示;某化学兴趣小组同学进行了如图2所示实验(忽略水的损失)。根据图示回答下列问题。
的溶解度曲线如图1所示;某化学兴趣小组同学进行了如图2所示实验(忽略水的损失)。根据图示回答下列问题。
 时,
时, 的溶解度是
的溶解度是(2)烧杯②中的
 溶液是
溶液是(3)下列有关说法正确的是______。
A. 固体中含有少量 固体中含有少量 ,可用降温结晶的方法提纯 ,可用降温结晶的方法提纯 |
B.分别将 时 时 和 和 的饱和溶液升温至 的饱和溶液升温至 ,所得溶液中 ,所得溶液中 的质量分数更大 的质量分数更大 |
C. 时,分别用两种固体配制质量相等的饱和溶液, 时,分别用两种固体配制质量相等的饱和溶液, 中加水更多 中加水更多 |
您最近一年使用:0次
【推荐2】如图是甲、乙、丙三种不含结晶水的固体物质的溶解度曲线,请回答下列问题:

(1)t1℃时,将10克甲物质加入到25克水中,充分溶解后,所得溶液中溶质和溶剂的质量比是______ (写出最简整数比)。
(2)t2℃时,甲溶液的溶质质量分数与丙溶液的溶质质量分数相比,前者和后者的关系是______(填字母)。
(3)将t2℃时等质量甲、乙、丙三种物质的饱和溶液降温到t1℃时,所得溶液的质量由大到小的顺序是______ 。

(1)t1℃时,将10克甲物质加入到25克水中,充分溶解后,所得溶液中溶质和溶剂的质量比是
(2)t2℃时,甲溶液的溶质质量分数与丙溶液的溶质质量分数相比,前者和后者的关系是______(填字母)。
| A.大于 | B.等于 | C.小于 | D.无法确定 |
您最近一年使用:0次