已知废旧干电池填料中含有二氧化锰、氯化铵和氯化锌等,某化学兴趣小组想回收利用废旧干电池中的二氧化锰和氯化铵,设计了如下流程:

(1)操作1和操作2的名称都是_____ ,该操作中用到的玻璃仪器除漏斗、烧杯外,还需要_____ ,其作用是_____ 。
(2)灼烧滤渣l时,会产生一种使澄清石灰水变浑浊的气体,由此推测滤渣1中除含有MnO2外,还存在的物质是_____ 。
(3)已知滤液1中氯化铵和氯化锌的浓度相近.在某温度下蒸发滤液1时,大量的氯化铵晶体先析出,说明该温度下氯化铵溶解度_____ 氯化锌的溶解度(填“<”、“=”或“>”)。
(4)同学们还设计了下列实验探究滤液2中的溶质成分。
【猜想】猜想一:氯化锌 猜想二:_____ 猜想三:氯化锌和氯化铵
【查阅资料】在氯化锌溶液中逐滴滴入稀氨水,先会生成白色沉淀,继续滴加白色沉淀会溶解。
【实验探究】
【结论】猜想三成立。

(1)操作1和操作2的名称都是
(2)灼烧滤渣l时,会产生一种使澄清石灰水变浑浊的气体,由此推测滤渣1中除含有MnO2外,还存在的物质是
(3)已知滤液1中氯化铵和氯化锌的浓度相近.在某温度下蒸发滤液1时,大量的氯化铵晶体先析出,说明该温度下氯化铵溶解度
(4)同学们还设计了下列实验探究滤液2中的溶质成分。
【猜想】猜想一:氯化锌 猜想二:
【查阅资料】在氯化锌溶液中逐滴滴入稀氨水,先会生成白色沉淀,继续滴加白色沉淀会溶解。
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液2,加入到过量氢氧化钠溶液中,并加热 | 滤液2中含有氯化铵 | |
| 另取少量滤液2, | 滤液2中含有氯化锌 |
【结论】猜想三成立。
更新时间:2019/10/04 23:23:01
|
相似题推荐
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐1】依据文意内容,回答下列问题。
多孔活性炭具有较好的吸附性能,是一种优良的催化剂载体材料,广泛应用于各行各业,其生产一直以煤、竹子、木材等宝贵资源为原料。随着可持续发展理念的不断深入,越来越多的研究者尝试以清洁廉价的资源作为原料(如白酒糟),制备多孔活性炭。
白酒糟是酿酒过程的副产物,富含纤维素【(C6H10O5)n】。以白酒糟为原料生产多孔活性炭的过程主要包括干燥、炭化、活化三步。炭化过程是将干燥的白酒糟在充满氮气的环境中,加热至650℃,将其中的纤维素转化为炭质原料(主要成为单质碳)。活化过程是以水蒸气或CO2为活化剂,在一定条件下使其在炭质原料内部发生反应,生成气体,形成孔隙结构,制备多孔活性炭。
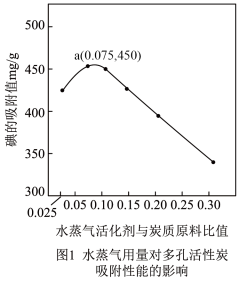
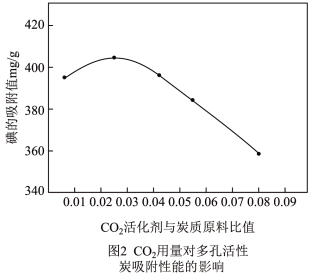
也有研究者在其他条件相同的情况下,通过实验测定所得多孔活性炭对碘的吸附值与水蒸气、CO2用量的关系分别如图1、2所示。
尽管以白酒糟为原料,制备多孔活性炭材料的技术仍有许多问题有待于进一步探索、解决,但已有研究为富含纤维素工业残渣的利用提供了可能途径。
(1)以白酒糟为原料制备多孔活性炭的优点是_________ 。
(2)纤维素中碳、氢元素质量比为_________ 。
(3)炭化过程中需要在充满氮气的环境中,此处氮气的作用是_______ 。
(4)分析图1得出的结论是_______ 。
(5)由图1、图2可知,为了达到最佳吸附效果,应选用的活化剂是______ 。(填“水蒸气”或“二氧化碳”)
多孔活性炭具有较好的吸附性能,是一种优良的催化剂载体材料,广泛应用于各行各业,其生产一直以煤、竹子、木材等宝贵资源为原料。随着可持续发展理念的不断深入,越来越多的研究者尝试以清洁廉价的资源作为原料(如白酒糟),制备多孔活性炭。
白酒糟是酿酒过程的副产物,富含纤维素【(C6H10O5)n】。以白酒糟为原料生产多孔活性炭的过程主要包括干燥、炭化、活化三步。炭化过程是将干燥的白酒糟在充满氮气的环境中,加热至650℃,将其中的纤维素转化为炭质原料(主要成为单质碳)。活化过程是以水蒸气或CO2为活化剂,在一定条件下使其在炭质原料内部发生反应,生成气体,形成孔隙结构,制备多孔活性炭。
也有研究者在其他条件相同的情况下,通过实验测定所得多孔活性炭对碘的吸附值与水蒸气、CO2用量的关系分别如图1、2所示。


尽管以白酒糟为原料,制备多孔活性炭材料的技术仍有许多问题有待于进一步探索、解决,但已有研究为富含纤维素工业残渣的利用提供了可能途径。
(1)以白酒糟为原料制备多孔活性炭的优点是
(2)纤维素中碳、氢元素质量比为
(3)炭化过程中需要在充满氮气的环境中,此处氮气的作用是
(4)分析图1得出的结论是
(5)由图1、图2可知,为了达到最佳吸附效果,应选用的活化剂是
您最近一年使用:0次
【推荐2】燃烧是人类最早利用的化学反应之一、
(1)《墨经》中记载了“立窑烧烟法”制墨。将松木置于炉膛中燃烧,瓮中收集的烟可用于制墨。“立窑烧烟法”利用了松木的_____ (填“完全”或“不完全”)燃烧。
(2)火善用之为福,不善用之为锅。下面是一些常用的灭火方法。请你从灭火原理角度看,属于隔绝空气(或氧气)的有_____。
(3)化学链燃烧是利用载氧体在两个反应器之间的循环,实现燃料在较温度下燃烧。以氧化镍(NiO)作载氧体的“化学链燃烧“过程如下:_____ ,Ni(固体)的颗粒越_____ (选填“大”或“小”),则反应越充分。
②一定温度下,反应器2中发生反应的化学方程式是_____ ,该容器中反应引发后,不需要再加热,可能的原因是_____ 。
(1)《墨经》中记载了“立窑烧烟法”制墨。将松木置于炉膛中燃烧,瓮中收集的烟可用于制墨。“立窑烧烟法”利用了松木的
(2)火善用之为福,不善用之为锅。下面是一些常用的灭火方法。请你从灭火原理角度看,属于隔绝空气(或氧气)的有_____。
| A.熄灭液化气灶火焰时,关闭阀门 | B.木材着火时,用泡沫灭火器灭火 |
| C.油锅着火时,用锅盖盖灭 | D.熄灭酒精灯时,用灯帽盖灭 |
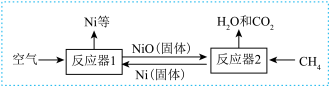
②一定温度下,反应器2中发生反应的化学方程式是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】铁和铁的化合物在工农业生产中有广泛的应用。
(一)铁的应用和防护
(1)我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其反应原理__ ,其反应类型为 __ 反应。
(2)将生铁百炼成钢,其原理用化学方程式表示为_____ 。
(二)铁的化合物应用
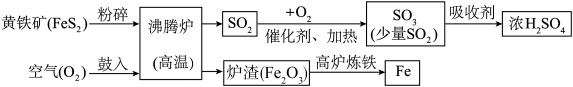
黄铁矿(主要成分是FeS2),是一种重要的化工原料,可用来制备硫酸和炼铁。
(1)工业上将黄铁矿粉碎的目的是__ 。
(2)高炉炼铁的化学方程式为__ 。
(三)铁的冶炼和探究
取Fe2O3粉末,小组同学用下图装置模拟炼铁,并测定反应后固体成分。

资料:碱石灰可吸收H2O和CO2。
(1)连接装置,先__ ,再装入药品。
(2)控制A中温度在700℃至固体全部变黑,继续通CO至冷却。通过测定装置B中固体的质量变化,可准确求得装置A中剩余固体质量。装置C的作用是__ 。
(一)铁的应用和防护
(1)我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其反应原理
(2)将生铁百炼成钢,其原理用化学方程式表示为
(二)铁的化合物应用
黄铁矿(主要成分是FeS2),是一种重要的化工原料,可用来制备硫酸和炼铁。

(1)工业上将黄铁矿粉碎的目的是
(2)高炉炼铁的化学方程式为
(三)铁的冶炼和探究
取Fe2O3粉末,小组同学用下图装置模拟炼铁,并测定反应后固体成分。

资料:碱石灰可吸收H2O和CO2。
(1)连接装置,先
(2)控制A中温度在700℃至固体全部变黑,继续通CO至冷却。通过测定装置B中固体的质量变化,可准确求得装置A中剩余固体质量。装置C的作用是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】对于农作物来说,科学合理的施肥有助于作物增产增收。
(1)草木灰(主要成分是K2CO3) 是农村里常见的一种肥料,它是植物体燃烧后所产生的灰烬。K2CO3和Na2CO3具有相似的化学性质,其水溶液显碱性。下列有关草木灰的说法中,不正确的是 (填下列选项序号之一)。
(2)干净的烧杯中盛有K2CO3和 KCl的固体混合物样品20g,加入一定质量的水使其完全溶解,然后向所得溶液中逐滴加入溶质质量分数为7.3%的稀盐酸,烧杯中溶液的质量与滴入稀盐酸的质量关系如图所示。试回答下列问题:_____ (写化学式)。
②当滴入上述稀盐酸至100g(即图中A 点)时,恰好完全反应。试通过计算,求原固体混合物样品中KCl 的质量_____ (计算结果精确到0.1g)。
(1)草木灰(主要成分是K2CO3) 是农村里常见的一种肥料,它是植物体燃烧后所产生的灰烬。K2CO3和Na2CO3具有相似的化学性质,其水溶液显碱性。下列有关草木灰的说法中,不正确的是 (填下列选项序号之一)。
| A.草木灰与铵态氮肥混合使用效果更好 |
| B.草木灰在农业生产中,主要作为钾肥使用 |
| C.草木灰可促使植株生长健壮,增强其抗病虫和抗倒伏的能力 |
(2)干净的烧杯中盛有K2CO3和 KCl的固体混合物样品20g,加入一定质量的水使其完全溶解,然后向所得溶液中逐滴加入溶质质量分数为7.3%的稀盐酸,烧杯中溶液的质量与滴入稀盐酸的质量关系如图所示。试回答下列问题:
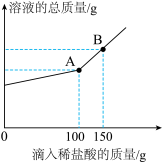
②当滴入上述稀盐酸至100g(即图中A 点)时,恰好完全反应。试通过计算,求原固体混合物样品中KCl 的质量
您最近一年使用:0次
【推荐2】2021年世界环境日主题为生态系统恢复(Ecosystem Restoration)
(1)下列属于空气污染物的是_____ 。
a、二氧化硫 b、一氧化碳 c、二氧化氮 d、可吸入颗粒物
(2)下列措施能减少或控制汽车尾气对空气污染的是_____ 。
a.汽车改用压缩天然气为燃料
b.开发清洁能源汽车,如太阳能汽车
c.改进发动机的燃烧方式,使汽油能充分燃烧
d.使用含铅汽油
(3)在汽油中加入适量乙醇作为汽车燃料,能在一定程度上减少汽车尾气的污染。写出乙醇充分燃烧的化学方程式为___________ 。
(4)含氮化合物是重要的化工原料。
①氨气是由_____ (填“分子”、“原子”或“离子”)构成的。
②氨气溶于水显碱性,是因为氨气与水反应生成了碱,请写出这种碱的化学式_____ 。
③NH4NO3是一种重要的氮肥。已知NH4NO3和KCl固体混合物中氮元素的质量分数为28%,则混合物中KCl的质量分数为_____ 。
④请完成鉴别氯化铵和硝酸铵两种溶液的实验报告。
(1)下列属于空气污染物的是
a、二氧化硫 b、一氧化碳 c、二氧化氮 d、可吸入颗粒物
(2)下列措施能减少或控制汽车尾气对空气污染的是
a.汽车改用压缩天然气为燃料
b.开发清洁能源汽车,如太阳能汽车
c.改进发动机的燃烧方式,使汽油能充分燃烧
d.使用含铅汽油
(3)在汽油中加入适量乙醇作为汽车燃料,能在一定程度上减少汽车尾气的污染。写出乙醇充分燃烧的化学方程式为
(4)含氮化合物是重要的化工原料。
①氨气是由
②氨气溶于水显碱性,是因为氨气与水反应生成了碱,请写出这种碱的化学式
③NH4NO3是一种重要的氮肥。已知NH4NO3和KCl固体混合物中氮元素的质量分数为28%,则混合物中KCl的质量分数为
④请完成鉴别氯化铵和硝酸铵两种溶液的实验报告。
| 实验步骤 | 实验现象 | 实验结论 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】硫酸铵是开采稀土的重要原料,根据国家质量标准,工业用硫酸铵的部分指标如下表,某公司生产的硫酸铵包装袋上部分文字如图所示。
化学社团同学对该硫酸铵进行如下实验:称取7.0g干燥的硫酸铵与足量的熟石灰混合均匀,按下图进行实验,充分反应后通入一会氮气,反应前后烧杯及其内溶液的总质量增加1.7g。[已知硫酸铵与熟石灰反应的化学方程式为 ,杂质不参加反应,忽略实验过程中烧杯中水分损失]
,杂质不参加反应,忽略实验过程中烧杯中水分损失]
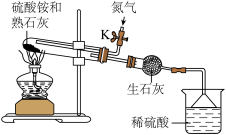
(1)将硫酸铵与熟石灰混合均匀的目的是___________ 。
(2)根据化学社团的数据,从硫酸铵的含量判断,该硫酸铵包装袋上的文字是否属实。(写出计算过程)
(3)如果烧杯中的稀硫酸用浓硫酸代替,则所测硫酸铵的质量分数___________ (填“偏大”、“不变”或“偏小”)。
(4)硫酸铵在农业上是一种化肥,下列关于化肥的说法中正确的是___________(双选)。
| 项目 | 指标 | ||
| 优等品 | 一等品 | 合格品 | |
| 硫酸铵含量≥ | 99.5 | 99.0 | 96.6 |
| 硫酸铵 按执行标准:  一等品 净重: 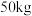 XX公司 |
 ,杂质不参加反应,忽略实验过程中烧杯中水分损失]
,杂质不参加反应,忽略实验过程中烧杯中水分损失]
(1)将硫酸铵与熟石灰混合均匀的目的是
(2)根据化学社团的数据,从硫酸铵的含量判断,该硫酸铵包装袋上的文字是否属实。(写出计算过程)
(3)如果烧杯中的稀硫酸用浓硫酸代替,则所测硫酸铵的质量分数
(4)硫酸铵在农业上是一种化肥,下列关于化肥的说法中正确的是___________(双选)。
| A.化肥对农业增产增收有重要作用 | B.滥用化肥可引起环境污染 |
| C.常见化肥中,根据颜色可将钾肥鉴别开来 | D.硫酸铵可与碱性物质混合施用 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】纳米级 颗粒可应用在磁流体领域。制备
颗粒可应用在磁流体领域。制备 的一种方法如下图所示。
的一种方法如下图所示。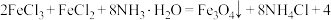
______ 。
(2)向盐酸酸化的 溶液中通入
溶液中通入 可生成
可生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为______ 。
(3)“沉淀”时需控制溶液的pH与反应的温度。
①“沉淀”时反应温度需要控制在50℃,适宜的加热方式为______ 。
②判断“沉淀”已完全的方法是______ 。
③“溶解”时,实际投料比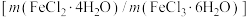 远大于理论值,为了尽可能的使实际投料比接近理论值,可采取的措施为
远大于理论值,为了尽可能的使实际投料比接近理论值,可采取的措施为______ 。
(4)在实验室过滤操作中,所需的仪器有铁架台、玻璃棒以及______ (填下图仪器字母序号),其玻璃棒的作用是______ ,过滤所得滤液的溶质主要成分 在农业上的作用是做
在农业上的作用是做______ 。 样品中混有少量
样品中混有少量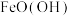 ,为了测定
,为了测定 的纯度,取2.000g样品,进行控温加热,该温度下,
的纯度,取2.000g样品,进行控温加热,该温度下,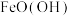 分解成
分解成 和水,而
和水,而 不发生反应。充分加热后,所得固体的质量为1.982g,计算该样品中
不发生反应。充分加热后,所得固体的质量为1.982g,计算该样品中 的纯度(写出计算过程)
的纯度(写出计算过程)
(6)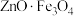 的性能比
的性能比 更好。
更好。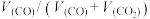 对还原产物的影响如图所示。温度在200~1000℃范围里,要保证还原产物始终为ZnO和
对还原产物的影响如图所示。温度在200~1000℃范围里,要保证还原产物始终为ZnO和 ,则控制体系中CO的体积分数的范围为
,则控制体系中CO的体积分数的范围为______ 。
 颗粒可应用在磁流体领域。制备
颗粒可应用在磁流体领域。制备 的一种方法如下图所示。
的一种方法如下图所示。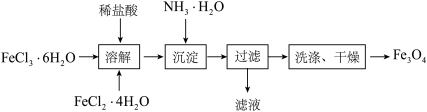
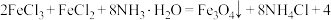
(2)向盐酸酸化的
 溶液中通入
溶液中通入 可生成
可生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(3)“沉淀”时需控制溶液的pH与反应的温度。
①“沉淀”时反应温度需要控制在50℃,适宜的加热方式为
②判断“沉淀”已完全的方法是
③“溶解”时,实际投料比
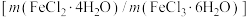 远大于理论值,为了尽可能的使实际投料比接近理论值,可采取的措施为
远大于理论值,为了尽可能的使实际投料比接近理论值,可采取的措施为(4)在实验室过滤操作中,所需的仪器有铁架台、玻璃棒以及
 在农业上的作用是做
在农业上的作用是做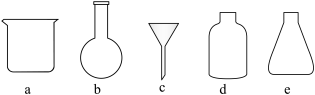
 样品中混有少量
样品中混有少量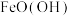 ,为了测定
,为了测定 的纯度,取2.000g样品,进行控温加热,该温度下,
的纯度,取2.000g样品,进行控温加热,该温度下,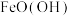 分解成
分解成 和水,而
和水,而 不发生反应。充分加热后,所得固体的质量为1.982g,计算该样品中
不发生反应。充分加热后,所得固体的质量为1.982g,计算该样品中 的纯度(写出计算过程)
的纯度(写出计算过程)(6)
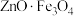 的性能比
的性能比 更好。
更好。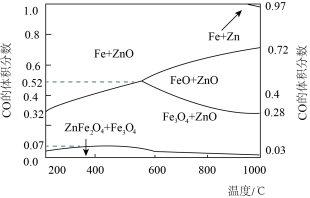
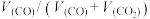 对还原产物的影响如图所示。温度在200~1000℃范围里,要保证还原产物始终为ZnO和
对还原产物的影响如图所示。温度在200~1000℃范围里,要保证还原产物始终为ZnO和 ,则控制体系中CO的体积分数的范围为
,则控制体系中CO的体积分数的范围为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】以下是在实验室里制取气体时常用的部分仪器。

(1)编号为E的仪器名称是___________ 。
(2)实验室若用高锰酸钾制氧气。
①除选用上图中可用的部分仪器外,还必须补充的玻璃仪器是___________ 。
②若制取3.2g氧气,理论上至少需要取用高锰酸钾___________ g。
(3)若实验室用氯酸钾和二氧化锰制取氧气,充分反应后可通过溶解、___________ 、洗涤、干燥操作,回收剩余固体中的二氧化锰(已知氯化钾、氯酸钾能溶于水)。

(1)编号为E的仪器名称是
(2)实验室若用高锰酸钾制氧气。
①除选用上图中可用的部分仪器外,还必须补充的玻璃仪器是
②若制取3.2g氧气,理论上至少需要取用高锰酸钾
(3)若实验室用氯酸钾和二氧化锰制取氧气,充分反应后可通过溶解、
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】工业上用电石(主要成分CaC2)生产乙炔(C2H2),反应的化学方程式为CaC2+2H2O=Ca(OH)2+C2H2↑。电石渣是反应后含Ca(OH)2的废渣。
(1)请计算:生产2.6t的C2H2时,生成Ca(OH)2的质量(写出计算过程及结果)。
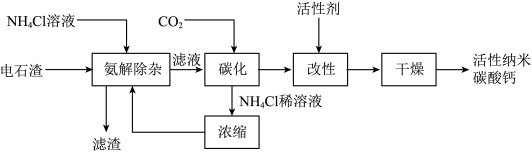
(2)电石渣可用于制备活性纳米碳酸钙,其主要工艺流程如下图。
已知:Ⅰ、电石渣中含有SiO2、Al2O3、Fe2O3等杂质,不与NH4Cl反应、难溶于水。
Ⅱ、Ca(OH)2+2NH4Cl=CaCl2+2NH3∙H2O
Ⅲ、CO2+2NH3∙H2O+CaCl2=CaCO3↓+2NH4Cl+H2O
①氨解除杂中,需要进行过滤操作,目的是______ 。
②发生化学反应,生成碳酸钙的步骤是______ (填序号)。
A.氨解除杂 B.碳化 C.改性 D.干燥
③活性纳米碳酸钙中碳元素,来自的原料物质是______ 。
④该生产工艺中,可被循环使用的物质是______ 。
(1)请计算:生产2.6t的C2H2时,生成Ca(OH)2的质量(写出计算过程及结果)。
(2)电石渣可用于制备活性纳米碳酸钙,其主要工艺流程如下图。

已知:Ⅰ、电石渣中含有SiO2、Al2O3、Fe2O3等杂质,不与NH4Cl反应、难溶于水。
Ⅱ、Ca(OH)2+2NH4Cl=CaCl2+2NH3∙H2O
Ⅲ、CO2+2NH3∙H2O+CaCl2=CaCO3↓+2NH4Cl+H2O
①氨解除杂中,需要进行过滤操作,目的是
②发生化学反应,生成碳酸钙的步骤是
A.氨解除杂 B.碳化 C.改性 D.干燥
③活性纳米碳酸钙中碳元素,来自的原料物质是
④该生产工艺中,可被循环使用的物质是
您最近一年使用:0次



