人类文明的发展和社会的进步同金属材料关系十分密切。
(一)铁的应用及防护
(1)生活中常用铁锅烹饪,主要利用铁的_____ (填字母)。
a 导电性 b 导热性 c 耐腐蚀
(2)“发蓝“处理是在铁表面形成致密氧化膜,以防止其腐蚀。“发蓝”的原理是:36Fe + 4NaNO2 + 9NaNO3 + 26H2O=12X + 13NaOH + 13NH3↑,X的化学式为_____
(3)患贫血症的人体内需要补铁____ (填字母)。
a 分子 b 原子 c 元素
(4)如图为某兴趣小组探究铁生锈的三个实验,最先观察到铁锈的是____ (选填序号)。

(5)铁生锈的主要过程为:
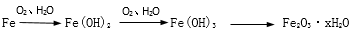
写出Fe(OH)2→Fe(OH)3反应的化学方程式______ 。
(二)铁的冶炼和探究
取20.0g Fe2O3粉末,小组同学用下图装置模拟炼铁,并测定反应后固体成分。
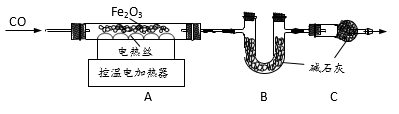
资料:碱石灰可吸收H2O和CO2。
(1)连接装置,先____ ,再装入药品。
(2)实验时先通入CO,目的是___ 。
(3)该实验装置有一个明显缺陷,你认为是___ 。
(4)控制A中温度在700℃至固体全部 变黑,继续通CO至冷却。
①通过测定装置B中固体的质量变化,可准确求得装置A中剩余固体质量。装置C的作用是____ 。
②现直接测得装置A中剩余固体质量为17.2g。则装置B中固体应增重___ g。
(5)经分析A中剩余固体17.2g为Fe和FexOy的混合物,向其中加入足量的稀H2SO4,充分反应,得H2 质量为0.1g。(FexOy和稀H2SO4反应,但无气体产生)
①固体中Fe质量为______ g。 ②FexOy的化学式为____ 。
(三)成分探究
【查阅资料】用CO还原Fe2O3炼铁的过程大致分为三个阶段:
阶段1:3Fe2O3+CO 2Fe3O4+CO2
2Fe3O4+CO2
阶段2:Fe3O4+CO 3FeO+CO2
3FeO+CO2
阶段3:FeO+CO Fe+CO2
Fe+CO2
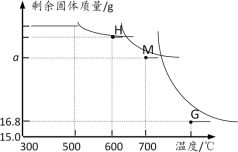
另取一定量Fe2O3进行上述实验,加热时固体质量随温度变化的曲线如图所示.回答下列问题:
(1)温度控制在300℃—500℃范围时,固体质量没有发生变化,原因是____ 。
(2)图中H点对应的固体成分的化学式是____
(3)图中M点对应a的数值=___
(一)铁的应用及防护
(1)生活中常用铁锅烹饪,主要利用铁的
a 导电性 b 导热性 c 耐腐蚀
(2)“发蓝“处理是在铁表面形成致密氧化膜,以防止其腐蚀。“发蓝”的原理是:36Fe + 4NaNO2 + 9NaNO3 + 26H2O=12X + 13NaOH + 13NH3↑,X的化学式为
(3)患贫血症的人体内需要补铁
a 分子 b 原子 c 元素
(4)如图为某兴趣小组探究铁生锈的三个实验,最先观察到铁锈的是

(5)铁生锈的主要过程为:
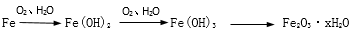
写出Fe(OH)2→Fe(OH)3反应的化学方程式
(二)铁的冶炼和探究
取20.0g Fe2O3粉末,小组同学用下图装置模拟炼铁,并测定反应后固体成分。

资料:碱石灰可吸收H2O和CO2。
(1)连接装置,先
(2)实验时先通入CO,目的是
(3)该实验装置有一个明显缺陷,你认为是
(4)控制A中温度在700℃至固体
①通过测定装置B中固体的质量变化,可准确求得装置A中剩余固体质量。装置C的作用是
②现直接测得装置A中剩余固体质量为17.2g。则装置B中固体应增重
(5)经分析A中剩余固体17.2g为Fe和FexOy的混合物,向其中加入足量的稀H2SO4,充分反应,得H2 质量为0.1g。(FexOy和稀H2SO4反应,但无气体产生)
①固体中Fe质量为
(三)成分探究
【查阅资料】用CO还原Fe2O3炼铁的过程大致分为三个阶段:

阶段1:3Fe2O3+CO
 2Fe3O4+CO2
2Fe3O4+CO2阶段2:Fe3O4+CO
 3FeO+CO2
3FeO+CO2阶段3:FeO+CO
 Fe+CO2
Fe+CO2另取一定量Fe2O3进行上述实验,加热时固体质量随温度变化的曲线如图所示.回答下列问题:
(1)温度控制在300℃—500℃范围时,固体质量没有发生变化,原因是
(2)图中H点对应的固体成分的化学式是
(3)图中M点对应a的数值=
更新时间:2019-12-13 10:18:40
|
相似题推荐
综合应用题
|
较难
(0.4)
名校
【推荐1】厨师在厨房炒菜时加了料后再加醋,就让菜肴变得香美可口,这其实隐藏了一个化学的小秘密:醋中的乙酸与料酒中的乙醇反应生成了有香味的乙酸乙酯,下表中是几种常见的酯,请完成下列问题:
(1)甲酸甲酯中碳元素、氢元素、氟元素的质量比为_____ ,其中氢元素的质量分数为_____ ;(保留0.1%)
(2)比较归纳是学习的重要方法,根据表推测X的化学式是_____ ;
(3)丙酸丙酯中氧元素的质量分数_____ (填“大于”、“小于”或“等于”)丁酸丁酯中氧元素的质量分数;
(4)若菜肴中的乙酸乙酯在人体内代谢时其中的碳元素完全部转化为CO2,则44mg的乙酸乙酯完全代谢产生的CO2的质量为多少?(请写出计算过程)_________
| 酯的名称 | 甲酸甲酯 | 乙酸乙酯 | 丙酸丙酯 | 丁酸丁酯 |
| 化学式 | C2H4O2 | C4H8O2 | C6H12O2 | X |
(1)甲酸甲酯中碳元素、氢元素、氟元素的质量比为
(2)比较归纳是学习的重要方法,根据表推测X的化学式是
(3)丙酸丙酯中氧元素的质量分数
(4)若菜肴中的乙酸乙酯在人体内代谢时其中的碳元素完全部转化为CO2,则44mg的乙酸乙酯完全代谢产生的CO2的质量为多少?(请写出计算过程)
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】“二十四节气”是我国古代农耕文化的产物,农耕生产与节气息息相关。
(1)“立春”:万物复苏,春暖花开。乙酸苯甲酯(C9H10O2)是一种具有茉莉花香的物质,其中氢、氧元素的质量比是___________ (填最简整数比)。
(2)“清明”:清明有霜梅雨少。正常雨水略显酸性,原因是___________ (用方程式表示)。pH<5.6的雨水容易导致土壤酸化,常用___________ 改良酸性土壤。
(3)“谷雨”:谷雨麦挑旗,立夏麦头齐。为促进小麦生长,应追加肥料。
①下列肥料属于复合肥料的是___________ (填字母)。
A CO(NH2)2 B.Ca3(PO4)2 C.NH4NO3 D.KNO3
②草木灰是一种钾肥,主要成分是K2CO3,一般不与铵态氮肥混合使用。据此推测,K2CO3溶液中含有的阴离子是___________ (填离子符号)。
(4)“秋风”:一粒好种,万担好粮。农业上常用质量分数为16%的NaCl溶液来选种。现有100g质量分数为26%的NaCl溶液,加___________ g水即可配成质量分数为16%的NaCl溶液。
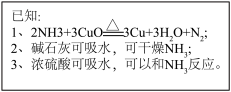
(5)“小雪”:小雪雪满天,来年必丰年。农作物的丰收离不开化肥的加持,常用的化肥“碳铵”受热易分解产生NH3.某小组同学根据NH3还原CuO的反应,设计测定Cu相对原子质量Ar(Cu)的实验。
【反思评价】
①从图中选择并组装一套合理、简单的装置,连接顺序为:制氨气发生装置→C→A___________ (填“B→C”或“C→B”);___________ (用含a、b的代数式表示)。
③在本实验中,使测定结果 Ar(Cu)偏大的是___________ (填字母)。
A.CuO未完全起反应 B.CuO中混有不反应的杂质 C.NH3通入A装置前未用C装置干燥
(1)“立春”:万物复苏,春暖花开。乙酸苯甲酯(C9H10O2)是一种具有茉莉花香的物质,其中氢、氧元素的质量比是
(2)“清明”:清明有霜梅雨少。正常雨水略显酸性,原因是
(3)“谷雨”:谷雨麦挑旗,立夏麦头齐。为促进小麦生长,应追加肥料。
①下列肥料属于复合肥料的是
A CO(NH2)2 B.Ca3(PO4)2 C.NH4NO3 D.KNO3
②草木灰是一种钾肥,主要成分是K2CO3,一般不与铵态氮肥混合使用。据此推测,K2CO3溶液中含有的阴离子是
(4)“秋风”:一粒好种,万担好粮。农业上常用质量分数为16%的NaCl溶液来选种。现有100g质量分数为26%的NaCl溶液,加
(5)“小雪”:小雪雪满天,来年必丰年。农作物的丰收离不开化肥的加持,常用的化肥“碳铵”受热易分解产生NH3.某小组同学根据NH3还原CuO的反应,设计测定Cu相对原子质量Ar(Cu)的实验。
【反思评价】
①从图中选择并组装一套合理、简单的装置,连接顺序为:制氨气发生装置→C→A
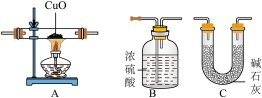
③在本实验中,使测定结果 Ar(Cu)偏大的是
A.CuO未完全起反应 B.CuO中混有不反应的杂质 C.NH3通入A装置前未用C装置干燥
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】某兴趣小组通过以下实验探究气体的制取方法和性质。已知:白色的无水硫酸铜粉末与水反应生成蓝色的硫酸铜晶体,小华同学用设计的实验装置(如下图 1)来制取气体。
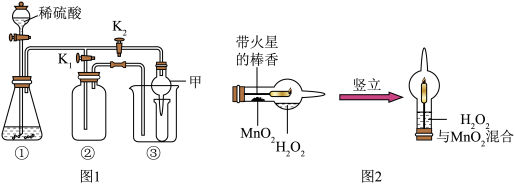
(1)装置①中添加液体的仪器名称_____ 。当打开 K1、关闭 K2时,利用①、②装置可直接进行的实验是_____ (填字母)。
A. 过氧化氢溶液和二氧化锰混合制取氧气 B. 锌与稀硫酸反应制取氢气
(2)利用①、②装置中制得的气体不纯,小明同学认为杂质可能为水蒸气,这是科学探究中的 (填字母)。
(3)打开 K2、关闭 K1,利用①、③装置来验证产生的气体中含水蒸气,此时仪器甲中盛放的物质是_____ ,可以观察到的现象是_____ 。
(4)图 2 仪器具有多种用途,小亮同学利用它制氧气并验证氧气性质:图2装置内发生的反应方程式____ 。实验过程中观察到的现象为_____ 。
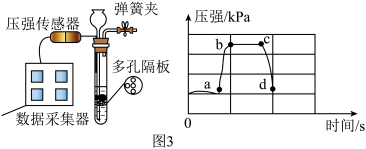
(5)兴趣小组在实验室制取二氧化碳气体的发生装置中连接上压强传感器,测得实验过程中试管内气体压强变化情况如图3,由此可知,石灰石与盐酸脱离接触的是 (填选项)。
(6)以CO2为碳源,与H2经催化可转化为高附加值的有机物,此方法具有重要的战略意义。中国化学家使用特殊的催化剂实现了CO2和H2转化为A或B等有机物和水,反应原理如图4所示:请回答下列问题:
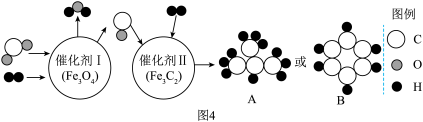
①A的化学式是_____ 。
②根据催化剂的特性可知,催化剂在该反应前后的质量和_____ 不变。
③理论上讲,当原料气中碳、氢元素质量比为_____ ,最终产物是B。

(1)装置①中添加液体的仪器名称
A. 过氧化氢溶液和二氧化锰混合制取氧气 B. 锌与稀硫酸反应制取氢气
(2)利用①、②装置中制得的气体不纯,小明同学认为杂质可能为水蒸气,这是科学探究中的 (填字母)。
| A.提出问题 | B.做出假设 | C.进行实验 | D.获得结论 |
(4)图 2 仪器具有多种用途,小亮同学利用它制氧气并验证氧气性质:图2装置内发生的反应方程式
(5)兴趣小组在实验室制取二氧化碳气体的发生装置中连接上压强传感器,测得实验过程中试管内气体压强变化情况如图3,由此可知,石灰石与盐酸脱离接触的是 (填选项)。
| A.ab 段 | B.bc 段 | C.cd 段 |

(6)以CO2为碳源,与H2经催化可转化为高附加值的有机物,此方法具有重要的战略意义。中国化学家使用特殊的催化剂实现了CO2和H2转化为A或B等有机物和水,反应原理如图4所示:请回答下列问题:

①A的化学式是
②根据催化剂的特性可知,催化剂在该反应前后的质量和
③理论上讲,当原料气中碳、氢元素质量比为
您最近一年使用:0次
【推荐1】下图是实验室制备气体的部分装置
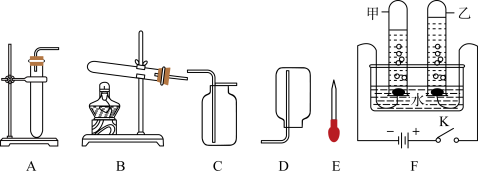
(1)用过氧化氢溶液制备一瓶氧气用于性质实验:
①该方法制得O2的化学方程式是___________ 。
②可选用_____ 和________ (填序号)装置组合。首先检查装置的气密性,方法是:把导管口放入水中,然后__________ ,观察到有气泡冒出,说明装置气密性良好。
(2)氢气被认为是理想的清洁、高能燃料
①实验室用锌与稀硫酸制取氢气并验证其可燃性,可选用_______ (填序号)与E装置组合,在E导管口点燃。实验过程是:组装仪器→检查装置气密性→装入药品制备氢气→________ →点燃。
②电解水也可制得H2。装置如图F,_________ 管中产生的是氢气
③氢气的生产方法是制约其作为清洁能源广泛使用的原因之一,科学家根据生产方法提出“绿色”氢气和“有污染”的氢气的概念,下列方法可获得“绿色”氢气的是_________ 。
A.用矿石生产锌和硫酸,再相互反应
B.在催化剂作用下,利用太阳能光解水
C.利用煤燃烧发电,再电解水
D.利用风能、水力发电,再电解水
(3)实验室常用加热醋酸钠和碱石灰的固体混合物来制取甲烷(CH4)气体,甲烷是一种无色无味、密度比空气小、极难溶于水的气体。制甲烷时,气体的发生装置是______ ,气体的收集装置可选用________ 。
(4)麦芽糖的化学式是C12H22O11,则每个麦芽糖分子中氢、氧原子的最简个数比为____ ,麦芽糖中碳、氢、氧三种元素的质量比为_______ (填最简整数比)。
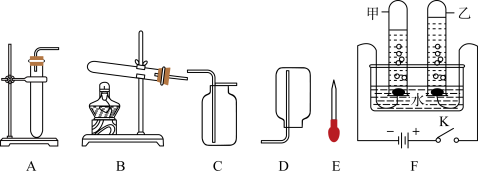
(1)用过氧化氢溶液制备一瓶氧气用于性质实验:
①该方法制得O2的化学方程式是
②可选用
(2)氢气被认为是理想的清洁、高能燃料
①实验室用锌与稀硫酸制取氢气并验证其可燃性,可选用
②电解水也可制得H2。装置如图F,
③氢气的生产方法是制约其作为清洁能源广泛使用的原因之一,科学家根据生产方法提出“绿色”氢气和“有污染”的氢气的概念,下列方法可获得“绿色”氢气的是
A.用矿石生产锌和硫酸,再相互反应
B.在催化剂作用下,利用太阳能光解水
C.利用煤燃烧发电,再电解水
D.利用风能、水力发电,再电解水
(3)实验室常用加热醋酸钠和碱石灰的固体混合物来制取甲烷(CH4)气体,甲烷是一种无色无味、密度比空气小、极难溶于水的气体。制甲烷时,气体的发生装置是
(4)麦芽糖的化学式是C12H22O11,则每个麦芽糖分子中氢、氧原子的最简个数比为
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】学好化学知识,助力个人防护,预防新冠病毒感染。
(1)出门要戴好口罩。制作口罩用的无纺布面料主要是聚丙烯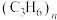 ,聚丙烯中碳、氢元素质量比为
,聚丙烯中碳、氢元素质量比为______ (填写最简整数比)。
(2)预防期间,常用“84”消毒液和75%的酒精进行消毒。“84”消毒液的主要成分是次氯酸钠( )和氯化钠(
)和氯化钠( ),两种物质中氯元素的化合价依次是
),两种物质中氯元素的化合价依次是______ 、______ 。酒精的学名为乙醇,其化学式是 ,酒精分子中碳、氢两种原子的个数比为
,酒精分子中碳、氢两种原子的个数比为______ (填写最简整数比)
(3)为了增强体质,我们需要进行体育锻炼。锻炼后常出现肌肉酸痛,这是由于部分葡萄糖( )无氧代谢产生乳酸(
)无氧代谢产生乳酸(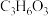 )造成的,休息后即可缓解。
)造成的,休息后即可缓解。
①乳酸的化学式量为______ ;
②乳酸中碳元素的质量分数为______ ;
③多少克乳酸中含有7.2g碳元素?______ (写出计算过程)
(1)出门要戴好口罩。制作口罩用的无纺布面料主要是聚丙烯
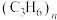 ,聚丙烯中碳、氢元素质量比为
,聚丙烯中碳、氢元素质量比为(2)预防期间,常用“84”消毒液和75%的酒精进行消毒。“84”消毒液的主要成分是次氯酸钠(
 )和氯化钠(
)和氯化钠( ),两种物质中氯元素的化合价依次是
),两种物质中氯元素的化合价依次是 ,酒精分子中碳、氢两种原子的个数比为
,酒精分子中碳、氢两种原子的个数比为(3)为了增强体质,我们需要进行体育锻炼。锻炼后常出现肌肉酸痛,这是由于部分葡萄糖(
 )无氧代谢产生乳酸(
)无氧代谢产生乳酸(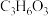 )造成的,休息后即可缓解。
)造成的,休息后即可缓解。①乳酸的化学式量为
②乳酸中碳元素的质量分数为
③多少克乳酸中含有7.2g碳元素?
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】“二十四节气”是我国古代农耕文化的产物,农耕生产与节气息息相关。
(1)“立春”:万物复苏,春暖花开。乙酸苯甲酯(C9H10O2)是一种具有茉莉花香的物质,其中氢、氧元素的质量比是___________ (填最简整数比)。
(2)“清明”:清明有霜梅雨少。正常雨水略显酸性,原因是___________ (用方程式表示)。pH<5.6的雨水容易导致土壤酸化,常用___________ 改良酸性土壤。
(3)“谷雨”:谷雨麦挑旗,立夏麦头齐。为促进小麦生长,应追加肥料。
①下列肥料属于复合肥料的是___________ (填字母)。
A CO(NH2)2 B.Ca3(PO4)2 C.NH4NO3 D.KNO3
②草木灰是一种钾肥,主要成分是K2CO3,一般不与铵态氮肥混合使用。据此推测,K2CO3溶液中含有的阴离子是___________ (填离子符号)。
(4)“秋风”:一粒好种,万担好粮。农业上常用质量分数为16%的NaCl溶液来选种。现有100g质量分数为26%的NaCl溶液,加___________ g水即可配成质量分数为16%的NaCl溶液。
(5)“小雪”:小雪雪满天,来年必丰年。农作物的丰收离不开化肥的加持,常用的化肥“碳铵”受热易分解产生NH3.某小组同学根据NH3还原CuO的反应,设计测定Cu相对原子质量Ar(Cu)的实验。
【反思评价】
①从图中选择并组装一套合理、简单的装置,连接顺序为:制氨气发生装置→C→A___________ (填“B→C”或“C→B”);___________ (用含a、b的代数式表示)。
③在本实验中,使测定结果 Ar(Cu)偏大的是___________ (填字母)。
A.CuO未完全起反应 B.CuO中混有不反应的杂质 C.NH3通入A装置前未用C装置干燥
(1)“立春”:万物复苏,春暖花开。乙酸苯甲酯(C9H10O2)是一种具有茉莉花香的物质,其中氢、氧元素的质量比是
(2)“清明”:清明有霜梅雨少。正常雨水略显酸性,原因是
(3)“谷雨”:谷雨麦挑旗,立夏麦头齐。为促进小麦生长,应追加肥料。
①下列肥料属于复合肥料的是
A CO(NH2)2 B.Ca3(PO4)2 C.NH4NO3 D.KNO3
②草木灰是一种钾肥,主要成分是K2CO3,一般不与铵态氮肥混合使用。据此推测,K2CO3溶液中含有的阴离子是
(4)“秋风”:一粒好种,万担好粮。农业上常用质量分数为16%的NaCl溶液来选种。现有100g质量分数为26%的NaCl溶液,加
(5)“小雪”:小雪雪满天,来年必丰年。农作物的丰收离不开化肥的加持,常用的化肥“碳铵”受热易分解产生NH3.某小组同学根据NH3还原CuO的反应,设计测定Cu相对原子质量Ar(Cu)的实验。

【反思评价】
①从图中选择并组装一套合理、简单的装置,连接顺序为:制氨气发生装置→C→A

③在本实验中,使测定结果 Ar(Cu)偏大的是
A.CuO未完全起反应 B.CuO中混有不反应的杂质 C.NH3通入A装置前未用C装置干燥
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐1】金属材料发展突飞猛进,其对人类生产、生活和社会发展有着极其重要作用。人类制得并利用金属历史悠久,研究金属发展过程为:存在形式→冶炼方法→性质应用。
【存在形式】
(1)金属化合物在自然界中以矿物的形式存在。现有①铝土矿②磁铁矿③黄铜矿三种矿石,其中可用来冶炼金属铜的是__________ 。
【冶炼方法】
(2)电解熔融氯化镁可得到镁和氯气的化学方程式为____________ 。
(3)《淮南万毕术》中有“曾青得铁则化为铜”的记载,其化学方程式为_________ ,基本反应类型是__________ 。
(4)下图为工业高炉炼铁剂而图和实验室模拟工业炼铁的部分仪器与装置。
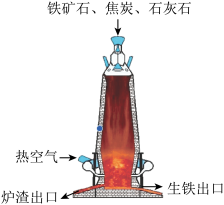
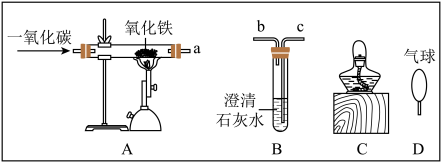
①工业炼铁时所需原料有____________ 。
②模拟炼铁时,A装置a口需要与B装置的(填字母)___________ 口相连接,模拟炼铁的化学反应方程式为___________ 。
③实验产生的尾气不能直接排放,你选择的处理装置是_________ 。
④若用含氧化铁240t的赤铁矿石为原料进行炼铁,理论上可得到含杂质4%的生铁质量为__________ 。
【性质用途】
(5)用铁制锅铲需要加上木柄或塑料柄,这是因为铁具有___________ 。
(6)在常温下,铝能“自我保护”的原因是_____________ 。
【存在形式】
(1)金属化合物在自然界中以矿物的形式存在。现有①铝土矿②磁铁矿③黄铜矿三种矿石,其中可用来冶炼金属铜的是
【冶炼方法】
(2)电解熔融氯化镁可得到镁和氯气的化学方程式为
(3)《淮南万毕术》中有“曾青得铁则化为铜”的记载,其化学方程式为
(4)下图为工业高炉炼铁剂而图和实验室模拟工业炼铁的部分仪器与装置。


①工业炼铁时所需原料有
②模拟炼铁时,A装置a口需要与B装置的(填字母)
③实验产生的尾气不能直接排放,你选择的处理装置是
④若用含氧化铁240t的赤铁矿石为原料进行炼铁,理论上可得到含杂质4%的生铁质量为
【性质用途】
(5)用铁制锅铲需要加上木柄或塑料柄,这是因为铁具有
(6)在常温下,铝能“自我保护”的原因是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】铁及其化合物在生产生活中发挥着重要作用。
一、铁的有关知识
(1)明代科学著作《天工开物》记载了中国劳动人民的科技成绩。
①“或用木炭,扇炉风箱,土(铁矿石)化成铁”描述了古代炼铁的方法。用化学方程式表示一氧化碳还原赤铁矿(主要成分为Fe2O3)的原理______ 。
②记载的“炒钢法”的生产如图所示。
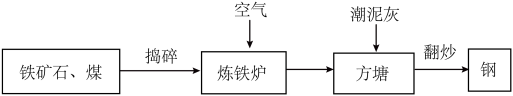
Ⅰ.铁矿石和煤在加入炼铁炉时需“捣碎",这样做的目的是______ 。
Ⅱ.不断翻炒液态坐铁,是为了______ (填“降低”或“升高")碳元素含最以制钢。
Ⅲ.对生铁炼钢的描述有:“凡钢铁炼法,火力到时生铁先化”。说明生铁的熔点比钢______ (填“高”或“低”)。
(2)铁器表面通过化学方法可形成致密的保护膜Fe3O4,故宫博物院对某出土铁器保护的过程如下。
①检测锈蚀产物
说明铁器在含有O2、______ 和盐等环境中容易被腐蚀。
②化学修复出土铁器可通过脱氯、还原,形成保护层来实现,原理如下:

脱氯发生反应的化学方程式为______ 。
二、Fe3O4的制备
Fe3O4是合成氨催化剂的主要成分,以下两种方法制备Fe3O4
方法一:

方法二:

(3)方法一发生反应的化学方程式为______ , 方法二中A的化学式为______ ,操作1和操作2相同,均为______ 。
(4)与方法二相比,方法一的不足之处是______ (答1点即可)。
(5)氢氧化氧铁(FeOOH)中铁元素是+3价,Fe3O4可表示为FeO∙Fe2O3,当A溶液①与A溶液②的质量之比为______ ,铁元素全部转化到中Fe3O4。
三、Fe3O4的失效与再生
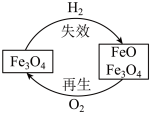
(6)合成氨催化过程中因部分Fe3O4与H2反应使催化剂“失效”。在一定温度下可用O2将其“再生”,原理如图所示。“再生”过程中铁元素的质量分数______ (选填“变大”、 “不变”或“变小”)。
(7)通入O2加热,将64.8gFeO进行再生。固体质量与温度变化的关系如图所示。
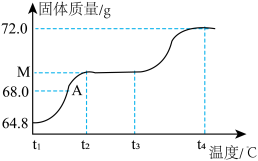
已知:T1°C~T2℃时,FeO转化为Fe3O4,T3℃~T4℃时,Fe3O4转化为Fe2O3。
①M=______ g。
②A点固体中生成的Fe3O4的质量为______ g。(请写出计算过程)
一、铁的有关知识
(1)明代科学著作《天工开物》记载了中国劳动人民的科技成绩。
①“或用木炭,扇炉风箱,土(铁矿石)化成铁”描述了古代炼铁的方法。用化学方程式表示一氧化碳还原赤铁矿(主要成分为Fe2O3)的原理
②记载的“炒钢法”的生产如图所示。

Ⅰ.铁矿石和煤在加入炼铁炉时需“捣碎",这样做的目的是
Ⅱ.不断翻炒液态坐铁,是为了
Ⅲ.对生铁炼钢的描述有:“凡钢铁炼法,火力到时生铁先化”。说明生铁的熔点比钢
(2)铁器表面通过化学方法可形成致密的保护膜Fe3O4,故宫博物院对某出土铁器保护的过程如下。
①检测锈蚀产物
| 主要成分 | |||
| Fe3O4 | Fe2O3∙H2O | FeOOH | FeOCl |
②化学修复出土铁器可通过脱氯、还原,形成保护层来实现,原理如下:

脱氯发生反应的化学方程式为
二、Fe3O4的制备
Fe3O4是合成氨催化剂的主要成分,以下两种方法制备Fe3O4
方法一:

方法二:

(3)方法一发生反应的化学方程式为
(4)与方法二相比,方法一的不足之处是
(5)氢氧化氧铁(FeOOH)中铁元素是+3价,Fe3O4可表示为FeO∙Fe2O3,当A溶液①与A溶液②的质量之比为
三、Fe3O4的失效与再生

(6)合成氨催化过程中因部分Fe3O4与H2反应使催化剂“失效”。在一定温度下可用O2将其“再生”,原理如图所示。“再生”过程中铁元素的质量分数
(7)通入O2加热,将64.8gFeO进行再生。固体质量与温度变化的关系如图所示。

已知:T1°C~T2℃时,FeO转化为Fe3O4,T3℃~T4℃时,Fe3O4转化为Fe2O3。
①M=
②A点固体中生成的Fe3O4的质量为
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】金属铁及其合金是世界上年产量最高、应用最广泛的金属材料,也是我们初中重点学习的金属单质。
(1)金属的化学性质主要是由金属的活动性决定的。
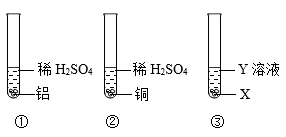
用如图①②所示实验证明铝的活动性比铜强,观察到的现象是______ ,反应的化学方程式为______ ;用图中③实验可以直接证明铝比铜活泼,则X和Y溶液分别是______ ;
(2)某同学用如图装置,进行还原氧化铁的实验(图中夹持已略去),检查装置气密性,加入药品,在装置中充满二氧化碳后进行实验。
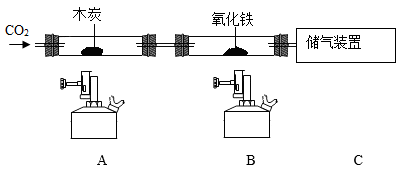
①缓缓通入CO2,点燃A处酒精喷灯,加热一段时间,硬质玻璃管中发生反应的化学方程式为______ 。
②点燃B处酒精喷灯,加热一段时间后B处玻璃管内观察到的实验现象是______ ,硬质玻璃管中发生反应的化学方程式为______ 。
③请解释储气装置C中收集到的气体及这些气体有剩余的原因是______ 。
④该实验说明______ 具有还原性
(3)工业上利用赤铁矿炼铁的过程如图所示:
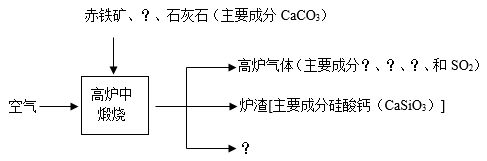
炼铁原料的选择:图中缺少的炼铁原料是______ ,我们一般选择赤铁矿(主要成分Fe2O3)而不用黄铁矿(主要成分FeS2)来炼铁,原因是______ ;高炉炼铁的产物:将高炉气体的主要成分补充完整______ ,高炉炼铁的产物还有______ ;
(4)为了探究钢铁锈蚀的条件,取4枚洁净无锈的铁钉,分别放入4支试管中如图所示:
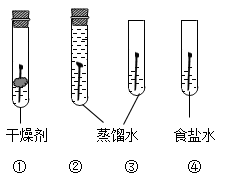
为了证明铁生锈需要同时接触水和氧气,我们必须进行的实验是______ (填序号,下同);若要证明其他条件相同时,有氯化钠存在会加速铁的锈蚀, 需要进行的实验是______ ;
(5)保护金属资源人人有责,我们保护金属资源的有效途径主要是:
①合理开采,寻找替代品;②防止金属锈蚀;③______ 等。
(1)金属的化学性质主要是由金属的活动性决定的。

用如图①②所示实验证明铝的活动性比铜强,观察到的现象是
(2)某同学用如图装置,进行还原氧化铁的实验(图中夹持已略去),检查装置气密性,加入药品,在装置中充满二氧化碳后进行实验。

①缓缓通入CO2,点燃A处酒精喷灯,加热一段时间,硬质玻璃管中发生反应的化学方程式为
②点燃B处酒精喷灯,加热一段时间后B处玻璃管内观察到的实验现象是
③请解释储气装置C中收集到的气体及这些气体有剩余的原因是
④该实验说明
(3)工业上利用赤铁矿炼铁的过程如图所示:

炼铁原料的选择:图中缺少的炼铁原料是
(4)为了探究钢铁锈蚀的条件,取4枚洁净无锈的铁钉,分别放入4支试管中如图所示:

为了证明铁生锈需要同时接触水和氧气,我们必须进行的实验是
(5)保护金属资源人人有责,我们保护金属资源的有效途径主要是:
①合理开采,寻找替代品;②防止金属锈蚀;③
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐1】钢铁在生产生活中有广泛应用。
I.实验室模拟炼铁
某化学兴趣小组用一氧化碳与氧化铁样品(含少量杂质)的反应来探究炼铁的原理,装置如图所示。请回答有关问题:
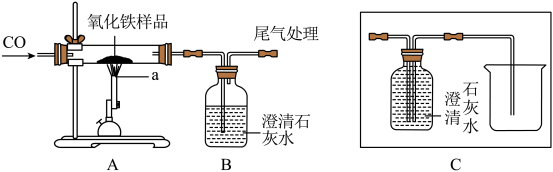
(1)A中仪器a的名称为:____ ,A装置中反应的方程式为____ 。
(2)CO气体除作为反应物外,还能起到的作用是:
①实验开始时,排尽装置中的空气,防止加热时发生爆炸;
②______ ;③将A装置中的CO2送入B装置的溶液中。
(3)若将B装置改成C虚线方框内装置,则C还起到的作用是______ 。
(4)若反应过程中装置A固体质量的变化情况如图所示,则所取氧化铁样品中Fe2O3的质量分数为多少?(写出计算过程)

Ⅱ.工业炼铁方式
(5)一种工业炼铁方法如图所示。
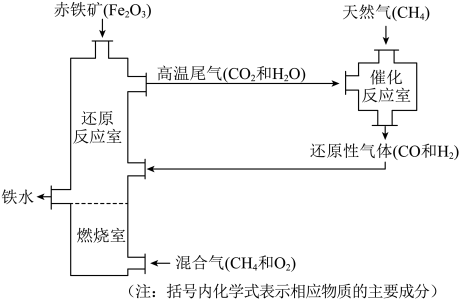
①催化反应室中,CH4与CO2或H2O在高温下均能发生反应,产物相同。写出其中一个反应的化学方程式:____ 。
②流程中CH4除产生还原性气体外,还有的作用是_____ 。
I.实验室模拟炼铁
某化学兴趣小组用一氧化碳与氧化铁样品(含少量杂质)的反应来探究炼铁的原理,装置如图所示。请回答有关问题:

(1)A中仪器a的名称为:
(2)CO气体除作为反应物外,还能起到的作用是:
①实验开始时,排尽装置中的空气,防止加热时发生爆炸;
②
(3)若将B装置改成C虚线方框内装置,则C还起到的作用是
(4)若反应过程中装置A固体质量的变化情况如图所示,则所取氧化铁样品中Fe2O3的质量分数为多少?(写出计算过程)

Ⅱ.工业炼铁方式
(5)一种工业炼铁方法如图所示。

①催化反应室中,CH4与CO2或H2O在高温下均能发生反应,产物相同。写出其中一个反应的化学方程式:
②流程中CH4除产生还原性气体外,还有的作用是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】金属在生产和生活中具有广泛的应用.
(1)地壳中含量最高的金属元素是________ (写元素符号,下同);人体中含量最高的金属元素是________ .
(2)铁制品容易锈蚀,用稀盐酸除铁锈的化学方程式为________ .
(3)铁矿石冶炼成铁是一个复杂的过程.把铁矿石、焦炭和石灰石一起加入高炉,在高温下,利用其中反应生成的______ 把铁从铁矿石中还原出来.
(4)炼钢过程中,检验员提取5g钢样,在足量的氧气中充分燃烧,将生成的气体用足量的澄清石灰水充分吸收,得到0.25g白色沉淀.求:
①该钢样燃烧时生成二氧化碳的质量________ ;
②该钢样中碳的质量分数________ .(写出计算过程)
(1)地壳中含量最高的金属元素是
(2)铁制品容易锈蚀,用稀盐酸除铁锈的化学方程式为
(3)铁矿石冶炼成铁是一个复杂的过程.把铁矿石、焦炭和石灰石一起加入高炉,在高温下,利用其中反应生成的
(4)炼钢过程中,检验员提取5g钢样,在足量的氧气中充分燃烧,将生成的气体用足量的澄清石灰水充分吸收,得到0.25g白色沉淀.求:
①该钢样燃烧时生成二氧化碳的质量
②该钢样中碳的质量分数
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,它们的转化关系如图所示.请回答:
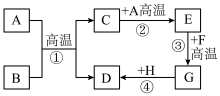
(1)物质B的化学式为_________ ;F的化学式为__________ ;
(2)写出下列反应方程式
反应①的化学方程式为_______ ;
反应②的化学方程式为_______ ;
(3)反应①属于______ 反应(填反应基本类型),反应①、③的反应基本类型是否相同?_____ .
为了防止食品腐败,在许多食品包装盒中都有一包黑色粉末.这种粉末是一种除氧剂。该粉末没有失效时呈黑色,失效后带有红棕色。为了确定该粉末的成分,小明做出了以下的【猜想】
猜想1:该粉末是木炭粉
猜想2:该粉末是铁粉
猜想3:该粉末是木炭粉和铁粉的混合物
小明取没有失效的该粉末,分别用不同的方法进行如下实验,填写表中空格.
【交流与反思】
(1)根据失效后的颜色判断,该粉末失效的原因是_____ ,变质后得到的红棕色粉末的主要成分是_____ (填物质的化学式).
(2)采用什么实验方法可以使失效的粉末“再生”?(用化学方程式表示)______ 。

(1)物质B的化学式为
(2)写出下列反应方程式
反应①的化学方程式为
反应②的化学方程式为
(3)反应①属于
为了防止食品腐败,在许多食品包装盒中都有一包黑色粉末.这种粉末是一种除氧剂。该粉末没有失效时呈黑色,失效后带有红棕色。为了确定该粉末的成分,小明做出了以下的【猜想】
猜想1:该粉末是木炭粉
猜想2:该粉末是铁粉
猜想3:该粉末是木炭粉和铁粉的混合物
小明取没有失效的该粉末,分别用不同的方法进行如下实验,填写表中空格.
| 试验操作 | 试验现象 | 猜想是否成立 | |
| 实验1 | 加入足量的硫酸铜溶液 | 猜想1:不成立 | |
| 实验2 | 加入足量的稀盐酸 | 猜想2:成立 | |
| 实验3 | 用磁铁吸引 | 粉末被全部吸引 | 猜想3: |
(1)根据失效后的颜色判断,该粉末失效的原因是
(2)采用什么实验方法可以使失效的粉末“再生”?(用化学方程式表示)
您最近一年使用:0次



