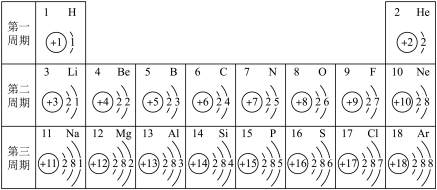
我们周围的物质世界是由各种元素组成的,为了便于研究元素的性质和用途,寻求它们之间的内在规律,科学家根据元素的结构和性质,将它们科学有序地排列成元素周期表的形式。下表是元素周期表中的一部分,表中的元素是人体生命活动的常量元素。

(1)氮元素的核电荷数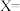
_____ 。
(2)与钠元素化学性质相似的元素为_____ (填元素符号)。
(3)氧、氯、硫、磷在化学反应中一般易_____ 电子,达到相对稳定结构。
(4)氦气常用来给气球充气,主要原因除了密度小,还因为它的化学性质比较_____ 。
(5)分析上表可发现,每一横行元素从左向右排列所遵循的一条规律是_____ 。
①质子数增加 ②原子电子数增加 ③金属性越强 ④电子层数相同 ⑤相对原子质量越大 ⑥相对原子质量越小

(1)氮元素的核电荷数
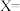
(2)与钠元素化学性质相似的元素为
(3)氧、氯、硫、磷在化学反应中一般易
(4)氦气常用来给气球充气,主要原因除了密度小,还因为它的化学性质比较
(5)分析上表可发现,每一横行元素从左向右排列所遵循的一条规律是
①质子数增加 ②原子电子数增加 ③金属性越强 ④电子层数相同 ⑤相对原子质量越大 ⑥相对原子质量越小
18-19八年级下·浙江·期末 查看更多[1]
(已下线)【初中科学2174 】【初二下】
更新时间:2019-12-30 10:38:19
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】(1)历史上,道尔顿认为,原子是一个个简单的、不可分割的实心球体。现在你认为该观点___________ (选填“正确”或“错误”)。
(2)现代化学上,镁元素的原子结构示意图为: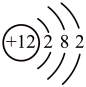 可知在化学反应中,镁原子易
可知在化学反应中,镁原子易_______ (选填“得到”或“失去”)电子形成镁离子,其离子符号表示为:____ 。
(2)现代化学上,镁元素的原子结构示意图为:
 可知在化学反应中,镁原子易
可知在化学反应中,镁原子易
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐2】如图中A、B、C、D是四种粒子的结构示意图,E是银元素在周期表中的信息。
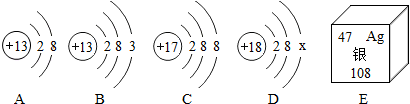
请回答下列问题:
(1)图中A、B、C、D四种粒子共表示_____ 种元素,
(2)D中x_____ 。
(3)E中银元素原子的质子数为_____ ,一个银原子质量是一个碳12原子质量的_____ 倍。

请回答下列问题:
(1)图中A、B、C、D四种粒子共表示
(2)D中x
(3)E中银元素原子的质子数为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】下表是元素周期表的一部分,请回答有关问题。

(1)图2表示如表中______ (填表中序号)的原子结构示意图;得电子后形成的离子符号为______ ;
(2)③处元素组成的单质在①处元素组成的单质中燃烧的符号表达式为______ ;
(3)②处形成的离子结构示意图是______ ;
(4)写出一条第三周期元素原子的核外电子排布规律______ ;
(5)与氧离子核外电子数相同的原子是_____ (填名称),1个甲烷分子(CH4)中共有______ 个质子。
(6)已知原子或离子的电子层数越少,半径越小;若电子层数相同,则核电荷数越小,半径越大。则F– 、Na+、S2–的离子半径由小到大的顺序为______ 。

(1)图2表示如表中
(2)③处元素组成的单质在①处元素组成的单质中燃烧的符号表达式为
(3)②处形成的离子结构示意图是
(4)写出一条第三周期元素原子的核外电子排布规律
(5)与氧离子核外电子数相同的原子是
(6)已知原子或离子的电子层数越少,半径越小;若电子层数相同,则核电荷数越小,半径越大。则F– 、Na+、S2–的离子半径由小到大的顺序为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】回答问题
(1)如图是七种原子的结构示意图,其中属于金属原子的是___________ (填字母),其原子的结构特点为___________ ,在化学反应中容易失去电子,形成___________ 离子。
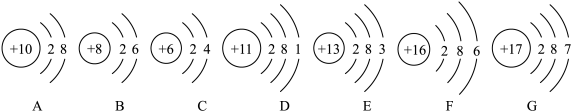
(2)写出B、C两种原子形成的化合物CB2的名称_______ 。
(1)如图是七种原子的结构示意图,其中属于金属原子的是

(2)写出B、C两种原子形成的化合物CB2的名称
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】核电荷数为1~18的元素的原子结构示意图等信息如下,请回答下列问题:

(1)中国科学院等单位联合发布了115号元素,中文名为“镆”。该元素属于______ 元素(填“金属”或“非金属”),此元素原子的核电荷数为______ 。
(2)已知硫原子的中子数为16,则硫原子的相对原子质量为______ ,写出13号元素和16号元素形成化合物的化学式______ ,该物质的名称为______ 。
(3)最外层电子数是决定元素化学性质的重要依据,下列各组具有相似化学性质的元素是______(填字母)
(4)某粒子的结构示意图如图,当x﹣y=8时,该粒子的符号为______ 。


(1)中国科学院等单位联合发布了115号元素,中文名为“镆”。该元素属于
(2)已知硫原子的中子数为16,则硫原子的相对原子质量为
(3)最外层电子数是决定元素化学性质的重要依据,下列各组具有相似化学性质的元素是______(填字母)
| A.Na、Cl | B.O、S | C.F、Cl | D.Cl、Ar |

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】元素周期表是学习和研究化学的重要工具。下图是元素周期表的一部分,我们对它进行研究。

(1)某一个氯原子的中子数为18,则其相对原子质量为___________ 。
(2)第7号元素位于第___________ 周期,属于___________ (填“金属”或“非金属”)盐酸,它在化学反应中容易___________ (填“得”或“失”)电子。
(3)科学家宣布,现已人工合成第120号元素,则此元素的核电荷数为___________ 。
(4)该图中与锂元素(Li)化学性质相似的元素名称为___________ 。
(5)元素周期表中不同种元素的本质区别是___________ 。
(6)市场上有“含氟牙膏”等商品,这里的“氟”指的是___________ (填“分子”“原子”或“元素”)

(1)某一个氯原子的中子数为18,则其相对原子质量为
(2)第7号元素位于第
(3)科学家宣布,现已人工合成第120号元素,则此元素的核电荷数为
(4)该图中与锂元素(Li)化学性质相似的元素名称为
(5)元素周期表中不同种元素的本质区别是
(6)市场上有“含氟牙膏”等商品,这里的“氟”指的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是元素周期表的部分内容,请认真分析并回答后面的问题:
请根据相关信息与知识回答:
(1)1869年,_____ (填序号)发现了元素周期律并编制了元素周期表。
A 拉瓦锡 B 张青莲 C 门捷列夫 D 道尔顿和阿伏加德罗
(2)请从上表中查出地壳中含量最多的金属元素的相对原子质量为_____ 。
(3)表中不同种元素最本质的区别是_____ (填序号)。
A 相对原子质量不同 B 质子数不同 C 中子数不同
(4)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如:_____ (填字母序号)。
A 从左到右,各元素原子的电子层数相同
B 从左到右,各元素原子的最外层电子数依次增加
C 从左到右,各元素原子的最外层电子数相同
IA | 0 | |||||||
1 | 1 H 氢 1.008 | 2 He 氦 4.003 | ||||||
IIA | IIIA | IVA | VA | VIA | VIIA | |||
2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
3 | 11 NA 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(1)1869年,
A 拉瓦锡 B 张青莲 C 门捷列夫 D 道尔顿和阿伏加德罗
(2)请从上表中查出地壳中含量最多的金属元素的相对原子质量为
(3)表中不同种元素最本质的区别是
A 相对原子质量不同 B 质子数不同 C 中子数不同
(4)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,如:
A 从左到右,各元素原子的电子层数相同
B 从左到右,各元素原子的最外层电子数依次增加
C 从左到右,各元素原子的最外层电子数相同
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)图 1 是元素周期表的部分内容,图 2 是这三种元素的原子结构示意图。

①SeO2 的相对分子质量为____________ 。
②图 2 中硫原子的结构示意图是__________ ,元素种类不同的原因是________ 。
③画出 O2﹣的结构示意图是______ 。
(2)近年来,我国科研人员在“甲烷二氧化碳重整和 Ni 基催化剂”的研究方面取得突破。如图 3 是甲烷与二氧化碳反应的微观示意图。

①在框内补充 C 的微观模型图____________ 。
②该反应利用两种温室气体,兼具环保和经济价值:反应难点之一是破坏甲烷分子、二氧化碳分子的稳定结构,分为_____________ (填微粒名称)并重新组合。
③写出该反应的化学方程式_________________ 。
(1)图 1 是元素周期表的部分内容,图 2 是这三种元素的原子结构示意图。

①SeO2 的相对分子质量为
②图 2 中硫原子的结构示意图是
③画出 O2﹣的结构示意图是
(2)近年来,我国科研人员在“甲烷二氧化碳重整和 Ni 基催化剂”的研究方面取得突破。如图 3 是甲烷与二氧化碳反应的微观示意图。

①在框内补充 C 的微观模型图
②该反应利用两种温室气体,兼具环保和经济价值:反应难点之一是破坏甲烷分子、二氧化碳分子的稳定结构,分为
③写出该反应的化学方程式
您最近一年使用:0次
【推荐2】(一)化学用语是我们学习化学的重要工具,结合下图中的信息回答问题。

(1)图1 是硅元素在元素周期表中的信息, 下列说法中错误的是( )
A.硅原子的相对原子质量为28.09g B.硅原子的质子数为14
C.硅元素为非金属元素 D.硅原子核外电子数为14
(2)图2中A、B、C分别为镁、氖、氯三种元素相关粒子的结构示意图,其中与 化学性质相似的原子是
化学性质相似的原子是_________ (填字母),与图3所示粒子属于同一种元素的离子是_______ (填离子符号),粒子________ (填字母)对应的元素在元素周期表中位于第三周期。
(3)A、C形成的化合物的化学式为____________ 。
(二)化学的学科特征是在分子、原子水平上研究物质的变化。下图为过氧化氢分解的微观示意图,请根据图示回答问题。

(1)反应后“X”所表示的粒子模型是_____________ 。
A. B.
B. C.
C. D.
D.
(2)写出上图所表示的化学反应的化学方程式:________ 。

(1)图1 是硅元素在元素周期表中的信息, 下列说法中错误的是
A.硅原子的相对原子质量为28.09g B.硅原子的质子数为14
C.硅元素为非金属元素 D.硅原子核外电子数为14
(2)图2中A、B、C分别为镁、氖、氯三种元素相关粒子的结构示意图,其中与
 化学性质相似的原子是
化学性质相似的原子是(3)A、C形成的化合物的化学式为
(二)化学的学科特征是在分子、原子水平上研究物质的变化。下图为过氧化氢分解的微观示意图,请根据图示回答问题。

(1)反应后“X”所表示的粒子模型是
A.
 B.
B. C.
C. D.
D.
(2)写出上图所表示的化学反应的化学方程式:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】元素周期表是学习和研究化学的重要工具,它的内容十分丰富,下表是依据元素周期表画出的1~18号元素的原子结构示意图。

(1)核电荷数为11的元素名称是__________ ,核电荷数为9的元素属于__________ (填“金属”或“非金属”)元素。
(2)对1~18号元素的原子结构示意图进行分析,可以发现许多规律,如第一周期元素的原子核外只有1个电子层。请再总结出其他规律,并写出其中一条:__________ 。
(3)在元素周期表中,同一周期(横行)中的元素,除0族元素(稀有气体元素)外,从左到右原子序数逐渐增大,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强。则:原子半径:碳________ (填“>”“=”或“<”,下同)氧:原子得电子能力:氧______ 氟。

(1)核电荷数为11的元素名称是
(2)对1~18号元素的原子结构示意图进行分析,可以发现许多规律,如第一周期元素的原子核外只有1个电子层。请再总结出其他规律,并写出其中一条:
(3)在元素周期表中,同一周期(横行)中的元素,除0族元素(稀有气体元素)外,从左到右原子序数逐渐增大,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强。则:原子半径:碳
您最近一年使用:0次