马强和几位同学在实验室用下列装置制取几种气体:
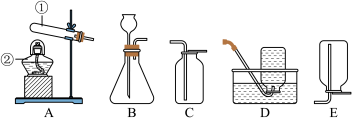
(1)写出图中标有①,②的仪器名称:①____ ②_____
(2)马强若用加热高锰酸钾制取并收集氧气,他应选择图中的A和___ 或_____ (填装置的序号)进行组装。写出反应文字表达式是________
(3)陈超利用过氧化氢溶液制取和收集氧气应选择的装置为___ 和____ (填装置的序号)进行组装。其中二氧化锰起______ 作用,写出反应文字表达式是______
(4)实验中在装药品前的一步操作是______ ,在给药品加热时,应先______
(5)实验室里,常用氯化铵晶体跟氢氧化钙粉末混合加热制取氨气,它是一种无色的,有刺激性气味的,密度比空气小,而溶于水且能跟水反应生成氨水的气体,制取氨气过程中还有氯化钙和水生成,实验室制取氨气的发生装置为______ (填装置的序号)其理由是_____ 。收集氨气可用____ (填装置的序号)理由是_______
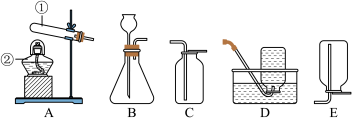
(1)写出图中标有①,②的仪器名称:①
(2)马强若用加热高锰酸钾制取并收集氧气,他应选择图中的A和
(3)陈超利用过氧化氢溶液制取和收集氧气应选择的装置为
(4)实验中在装药品前的一步操作是
(5)实验室里,常用氯化铵晶体跟氢氧化钙粉末混合加热制取氨气,它是一种无色的,有刺激性气味的,密度比空气小,而溶于水且能跟水反应生成氨水的气体,制取氨气过程中还有氯化钙和水生成,实验室制取氨气的发生装置为
更新时间:2020-01-15 20:37:45
|
相似题推荐
实验题
|
适中
(0.65)
解题方法
【推荐1】在用氯酸钾和二氧化锰的混合物制取氧气实验后,为了进一步探究二氧化锰的用量对氯酸钾分解速度的影响,小明用如图装置,以及实验室提供的实验所需药品和器材进行实验。老师对实验的建议:①每组实验氯酸钾用量可取4克,二氧化锰质量不宜超过2克。②实验应设计4 组。

(1)结合老师建议,补充完整实验步骤①之后的其它步骤。
①检查装置的气密性;________ ________ ________ ________
(2)实验结束后,小明回收了二氧化锰。如果要证明二氧化锰是氯酸钾分解的催化剂,还需验证二氧化锰的__________ 保持不变。

(1)结合老师建议,补充完整实验步骤①之后的其它步骤。
①检查装置的气密性;
(2)实验结束后,小明回收了二氧化锰。如果要证明二氧化锰是氯酸钾分解的催化剂,还需验证二氧化锰的
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】实验室可选用下列装置制取气体:
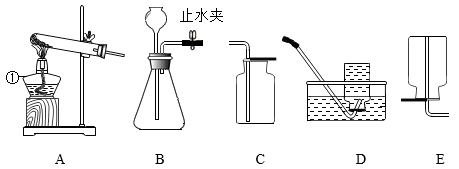
(1)写出图中标有①的仪器名称:①_____ 。
(2)用双氧水和二氧化锰制取O2,选择的发生和收集装置的组合是_____ (写出一种组合,填序号)。
(3)探究用过氧化氢制取氧气的适宜催化剂。实验方案如下:
Ⅰ、用MnO2、CuO、Fe2O3、Cr2O3(氧化铬)四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用,
Ⅱ、取30粒含MnO2的海藻酸钠微球,采用如图2所示装置进行实验。请写出该反应的符号表达式_____ ,二氧化锰的作用是_____ ,改用其他三种微球,分别重复上述实验,得到锥形瓶内压强随时间变化的曲线图3。
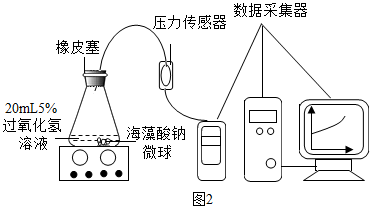

①每次实验时,海藻酸钠微球数应相同的原因_____ 。
②用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是_____ 。
③从实验曲线看,催化效果较好、反应温和的催化剂是_____ 。

(1)写出图中标有①的仪器名称:①
(2)用双氧水和二氧化锰制取O2,选择的发生和收集装置的组合是
(3)探究用过氧化氢制取氧气的适宜催化剂。实验方案如下:
Ⅰ、用MnO2、CuO、Fe2O3、Cr2O3(氧化铬)四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用,
Ⅱ、取30粒含MnO2的海藻酸钠微球,采用如图2所示装置进行实验。请写出该反应的符号表达式


①每次实验时,海藻酸钠微球数应相同的原因
②用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是
③从实验曲线看,催化效果较好、反应温和的催化剂是
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】小林同学在体育课上腿部擦伤,医务室的大夫在她伤口上涂了医用过氧化氢溶液, 小林看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解 就加快了呢?

I、小林准备用如图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化 氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧 气。
II、小林查阅了相关资料,并进行了探究实验
【查阅资料】
①过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以 催化过氧化氢分解。
②温度对化学反应的快慢有影响,人体正常体温是 37℃。
【提出猜想】
猜想1: 过氧化氢分解加快是因为体温比瓶中的温度高。猜想2: 过氧化氢分解加快是因为伤口中有过氧化氢酶。
【进行实验】
(1)实验①得出的结论是_______ 。
(2)实验②中第一次收集到的氧气体积为_______ mL。
(3)实验②中横线部分应进行的操作是_______
(4)为探究影响过氧化氢分解速率的因素,还可以作为判断依据的是 。
【实验反思】小林反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的 结论可能存在不足。因此又补充进行了几组实验,量筒中2分钟收集到的气体体积数据记录如下表所示。
(5)通过这些数据,你能得出的新结论是_______ 。

I、小林准备用如图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化 氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧 气。
II、小林查阅了相关资料,并进行了探究实验
【查阅资料】
①过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以 催化过氧化氢分解。
②温度对化学反应的快慢有影响,人体正常体温是 37℃。
【提出猜想】
猜想1: 过氧化氢分解加快是因为体温比瓶中的温度高。猜想2: 过氧化氢分解加快是因为伤口中有过氧化氢酶。
【进行实验】
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 分两次进行实验,均注入5mL过氧化氢溶液第一次在常温下进行 第二次将试管浸在 37℃的温水中 | 量筒中2分钟收集到的气体体积均为5mL | |
| ② | 分两次进行实验第一次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5mL 过氧化氢溶液第二次_______ | 第一次,量筒中2分钟收集到的气体体积为_______mL第二次,量筒中2分钟收集到的气体体积为5mL | 过氧化氢分解加快 是因为过氧化氢酶的作用 |
(1)实验①得出的结论是
(2)实验②中第一次收集到的氧气体积为
(3)实验②中横线部分应进行的操作是
(4)为探究影响过氧化氢分解速率的因素,还可以作为判断依据的是 。
| A.产生气泡的快慢 |
| B.测定收集等体积气体所需时间 |
| C.分别测定不同时间所产生的气体体积 |
【实验反思】小林反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的 结论可能存在不足。因此又补充进行了几组实验,量筒中2分钟收集到的气体体积数据记录如下表所示。
| 加入过氧化氢酶 | 不加过氧化氢酶 | |||||
| 反应温度/ ℃ | 25 | 37 | 42 | 25 | 37 | 42 |
| 收集到气体体积/ mL | 39 | 56 | 34 | 5 | 5 | 5 |
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的。结合下列实验装置图回答问题:
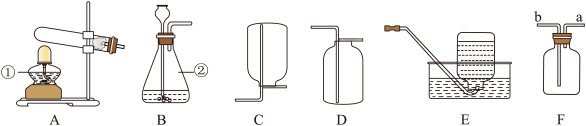
(1)写出标号仪器的名称:①____________ ;②____________ 。
(2)实验室若用高锰酸钾制取氧气,选择的发生装置是____________ (填字母序号),试管口放一团棉花的作用是____________ ,写出反应的文字表达式____________ ;用高锰酸钾制取氧气的实验步骤有:①给试管加热 ②连接仪器,检查装置的气密性 ③将试管固定在铁架台上 ④向试管中装入高锰酸钾。并在试管口放一团棉花 ⑤收集气体 ⑥熄灭酒精灯 ⑦将导管移出水面正确的顺序为____________ 。(用序号表示)
(3)若用E装置收集氧气,当看到___________________ 时开始收集,收集好气体后将集气瓶从水槽中取出后____________ (填“正放”或“倒放”)在实验桌上。
(4)若用D装置收集氧气,验满的方法是___________________ 。
(5)若用F装置用排空气法收集氧气,氧气从____________ (填“a”或“b”)端通入。

(1)写出标号仪器的名称:①
(2)实验室若用高锰酸钾制取氧气,选择的发生装置是
(3)若用E装置收集氧气,当看到
(4)若用D装置收集氧气,验满的方法是
(5)若用F装置用排空气法收集氧气,氧气从
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】现有下图所示的实验装置,请回答问题:

(1)实验室用高锰酸钾制取氧气所选择的发生装置是_____ (填序号,下同),该反应的文字表达式____ ,收集氧气可选择C装置,其原因是______ ;
(2)实验室可用双氧水制取氧气该反应的文字表达式为______ ;实验室可用氯酸钾制取氧气该反应的文字表达式为______ 。
(3)用排水法收集氧气,应待气泡_______ 时才开始收集。
(4)做木炭在氧气中燃烧的实验时,为了使木炭在氧气中充分燃烧,应将红热的木炭_____ 伸入集气瓶中。
(5)甲烷(CH4)是一种无色、无味的气体,密度比空气小且极难溶于水,是天然气的主要成分。实验室制取甲烷气体常用无水醋酸钠(固体)和碱石灰(固体)加热制得。则实验室制取甲烷可选用的发生装置是______ ,选用的收集装置是________ 、_________ 。
(6)如图有多种功能,如收集、洗涤、贮存气体等。回答下列问题:
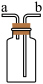
①气体从a端进入集气,该气体必须具有的性质是_________ 。
②若装置中预先盛满水,将水排出贮气,气体从_________ 端进入。

(1)实验室用高锰酸钾制取氧气所选择的发生装置是
(2)实验室可用双氧水制取氧气该反应的文字表达式为
(3)用排水法收集氧气,应待气泡
(4)做木炭在氧气中燃烧的实验时,为了使木炭在氧气中充分燃烧,应将红热的木炭
(5)甲烷(CH4)是一种无色、无味的气体,密度比空气小且极难溶于水,是天然气的主要成分。实验室制取甲烷气体常用无水醋酸钠(固体)和碱石灰(固体)加热制得。则实验室制取甲烷可选用的发生装置是
(6)如图有多种功能,如收集、洗涤、贮存气体等。回答下列问题:

①气体从a端进入集气,该气体必须具有的性质是
②若装置中预先盛满水,将水排出贮气,气体从
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】实验室部分装置如图所示,请回答下列问题。

(1)若用KMnO4制取O2,应选用发生装置________ (填编号),应选用收集装置_____ 或
_____ (填编号),反应的化学方程式是___________ 。
(2)若用100g含杂质5%的石灰石和盐酸制取CO2(假设杂质不与盐酸反应,石灰石的体积约为34cm3),应选用发生装置_____ (填编号),反应的化学方程式是______________ ,其中CaCO3与CO2的质量比为_________ ,反应后最多能生成______ gCO2(结果取整数)。
(3)在实验室制取二氧化碳的研究中,进行了如下实验:
①若要研究盐酸的浓、稀对反应的影响,可选择实验甲与______ 对照(选填实验编号)。
②除盐酸的浓稀外,上述实验研究的另一个影响反应的因素是_____________________ 。

(1)若用KMnO4制取O2,应选用发生装置
(2)若用100g含杂质5%的石灰石和盐酸制取CO2(假设杂质不与盐酸反应,石灰石的体积约为34cm3),应选用发生装置
(3)在实验室制取二氧化碳的研究中,进行了如下实验:
| 实验编号 药品 | 甲 | 乙 | 丙 | 丁 |
| m g石灰石 | 块状 | 块状 | 粉末状 | 粉末状 |
| w g盐酸 | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
②除盐酸的浓稀外,上述实验研究的另一个影响反应的因素是
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】氧气的制取是初中化学的重要内容,根据如图所示的装置回答问题:
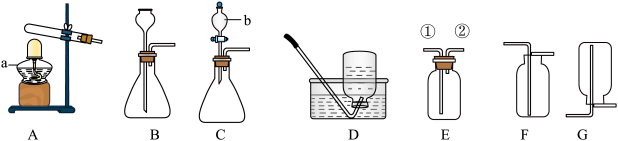
(1)仪器a常用______ (填“内焰”“外焰”或“焰心”)加热,图中b仪器的名称是______ ;
(2)A、B、C装置均可作为实验室制取氧气的发生装置,与B相比,选用C装置的优点是______ 。
(3)实验室以过氧化氢溶液、二氧化锰为原料制取氧气。连接装置C、D,微热C,若D中产生气泡、且恢复常温后玻璃管内水面______ 水槽的水面,就证明装置气密性良好。该反应的文字表达式为______ 。
(4)若用装置E收集氧气,气体从______ (填①或②)端进入;
(5)实验室制取O2一般有六个步骤:①检查装置的气密性;②按要求装配好仪器;③向b中注入过氧化氢试液;④向锥形瓶中放入固体粉末二氧化锰;⑤用带火星的木条靠近集气瓶瓶口验满;⑥收集气体。则正确的操作顺序是______ (填数字序号)。

(1)仪器a常用
(2)A、B、C装置均可作为实验室制取氧气的发生装置,与B相比,选用C装置的优点是
(3)实验室以过氧化氢溶液、二氧化锰为原料制取氧气。连接装置C、D,微热C,若D中产生气泡、且恢复常温后玻璃管内水面
(4)若用装置E收集氧气,气体从
(5)实验室制取O2一般有六个步骤:①检查装置的气密性;②按要求装配好仪器;③向b中注入过氧化氢试液;④向锥形瓶中放入固体粉末二氧化锰;⑤用带火星的木条靠近集气瓶瓶口验满;⑥收集气体。则正确的操作顺序是
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】依据下列实验室制取气体的发生和收集装置,回答问题。

(1)仪器①的名称是______ 。
(2)实验室用高锰酸钾制取氧气的文字表达式为______ ,发生装置选择______ (填字母)。
(3)氧气可选用E装置进行收集,其原因是______ 。
(4)用F装置探究氧气的性质,观察到集气瓶中硫剧烈燃烧,发出______ 火焰。

(1)仪器①的名称是
(2)实验室用高锰酸钾制取氧气的文字表达式为
(3)氧气可选用E装置进行收集,其原因是
(4)用F装置探究氧气的性质,观察到集气瓶中硫剧烈燃烧,发出
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】实验室制取气体常用到下列装置,据图回答下列问题:
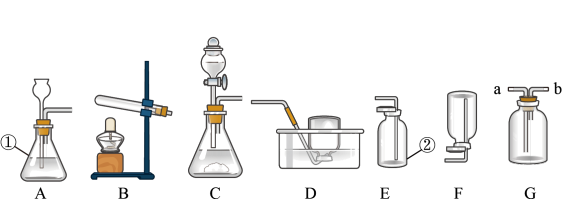
(1)图中仪器①的名称是______ 。
(2)在实验室选用氯酸钾和二氧化锰来制取并收集较纯净的氧气,应选择的制取装置是______ (填序号)。若用图G装置在瓶中装满水来也可以收集氧气,此时气体应从______ (填“a”或“b”)端通入。
(3)若用过氧化氢溶液和二氧化锰制取氧气,可以选择装置A或C,其中C装置的优点是______ 。
(4)某同学在加热氯酸钾制氧气时,发现产生氧气的速率很慢,经检查装置气密性良好,氯酸钾也没有变质,你认为可能的原因是______ 。

(1)图中仪器①的名称是
(2)在实验室选用氯酸钾和二氧化锰来制取并收集较纯净的氧气,应选择的制取装置是
(3)若用过氧化氢溶液和二氧化锰制取氧气,可以选择装置A或C,其中C装置的优点是
(4)某同学在加热氯酸钾制氧气时,发现产生氧气的速率很慢,经检查装置气密性良好,氯酸钾也没有变质,你认为可能的原因是
您最近半年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】氧气是人类不可离开的物质。根据下列装置图回答问题。
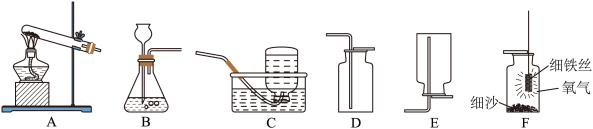
(1)实验室用氯酸钾制氧气的化学方程式为______ ,其发生装置可选用(填字每序号,下同):______ ,用C装置收集氧气前,将集气瓶内空气完全排尽的方法是______ 。
(2)某同学欲按图F所示方法做细铁丝燃烧的实验,收集所需氧气最好选用的装置是______ ;做硫燃烧实验,收集所需氧气最好选用的装置是______ 。由此可见,选择气体的收集方法主要应考虑气体的性质,此外往往还要考虑______ 。

(1)实验室用氯酸钾制氧气的化学方程式为
(2)某同学欲按图F所示方法做细铁丝燃烧的实验,收集所需氧气最好选用的装置是
您最近半年使用:0次
实验题
|
适中
(0.65)
名校
【推荐2】氨气是一种无色、有强烈的刺激气味的气体。课后为了继续探究氨气的性质,同学们先收集一试管的氨气,然后塞上带有胶头滴管的橡胶塞,再将胶头滴管的水挤入试管,最后在水中取下胶头,观察到试管内出现了红色喷泉。

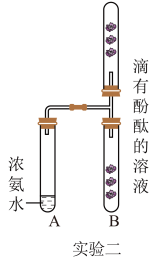
(1)实验一,④中试管看到红色喷泉,说明此时试管内压强________ (“变大”或“变小”或“不变”),由实验一还可推断出氨气的物理性质有_______ 、______ 。
(2)课堂上老师按“实验二”的装置对分子运动进行探究,实验过程中,_______ (填“B”或“C”)试管中滴有酚酞的滤纸条最先全部变红。


(1)实验一,④中试管看到红色喷泉,说明此时试管内压强
(2)课堂上老师按“实验二”的装置对分子运动进行探究,实验过程中,
您最近半年使用:0次
【推荐3】为了制取CO2气体并验证其性质,小周同学设计并进行了图1所示的实验,请根据要求回答有关问题。

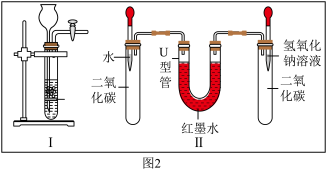
(1)仪器①的名称是_____ ,实验室制取并收集二氧化碳气体应选用的装置组合是____ (填图1中装置字母的代号);反应的化学方程式是______ ;
(2)小陆同学是位善于动脑筋的学生,他将小周中的装置B进行了改进(如图2中的 I),这样改进后,装置的主要优点是______ ;
(3)小陆同学用其改进的装置收集了两试管的CO2气体,用来验证CO2与氢氧化钠溶液反应,她设计的实验装置如图2中的II,请回答:
①同时滴入等体积的水和氢氧化钠溶液后,观察到现象是______ ;
②写出二氧化碳与氢氧化钠反应的化学方程式______ 。


(1)仪器①的名称是
(2)小陆同学是位善于动脑筋的学生,他将小周中的装置B进行了改进(如图2中的 I),这样改进后,装置的主要优点是
(3)小陆同学用其改进的装置收集了两试管的CO2气体,用来验证CO2与氢氧化钠溶液反应,她设计的实验装置如图2中的II,请回答:
①同时滴入等体积的水和氢氧化钠溶液后,观察到现象是
②写出二氧化碳与氢氧化钠反应的化学方程式
您最近半年使用:0次



