请回忆“粗盐提纯”的活动与探究并回答下列问题:

(1)为了除去粗盐中可溶性杂质氯化镁(泥沙已除去),可进行如下操作:
①加水溶解②加过量的_____ 溶液③过滤④加入适量的盐酸,顺序不能交换的原因是_____ 。
(2)蒸发滤液的过程中,下列操作正确的是_____ 。
A 把浑浊的液体倒入蒸发皿内加热
B 开始析出晶体后用玻璃棒搅拌
C 蒸发皿中出现较多固体时停止加热
D 待蒸发皿中液体蒸干后停止加热

(1)为了除去粗盐中可溶性杂质氯化镁(泥沙已除去),可进行如下操作:
①加水溶解②加过量的
(2)蒸发滤液的过程中,下列操作正确的是
A 把浑浊的液体倒入蒸发皿内加热
B 开始析出晶体后用玻璃棒搅拌
C 蒸发皿中出现较多固体时停止加热
D 待蒸发皿中液体蒸干后停止加热
2019·北京·模拟预测 查看更多[1]
更新时间:2020/02/13 09:27:41
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】二氧化碳“捕集”技术实现了二氧化碳的捕捉、封存和资源化利用,是实现“碳中和”的重要途径之一、图为“氨法”捕集二氧化碳流程图。请回答相关问题:
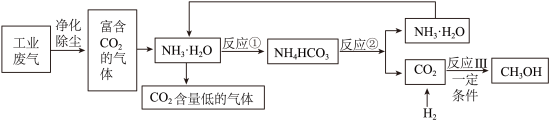
(1)反应①需控制在一定温度范围内进行,原因是___________ 。
(2)反应③除生成CH3OH外,还生成一种相对分子质量最小的氧化物,写出该反应的化学方程式___________ 。
(3)③上述流程中,可循环利用的物质是___________ 。
(4)④对“氨法”捕集二氧化碳技术认识正确的是___________。(填字母序号,可多选)

(1)反应①需控制在一定温度范围内进行,原因是
(2)反应③除生成CH3OH外,还生成一种相对分子质量最小的氧化物,写出该反应的化学方程式
(3)③上述流程中,可循环利用的物质是
(4)④对“氨法”捕集二氧化碳技术认识正确的是___________。(填字母序号,可多选)
| A.有利于缓解温室效应 | B.有利于变废为宝 | C.流程繁琐,无推广价值 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】平板电视显示屏生产过程中产生的废玻璃粉末主要成分为SiO2、Fe2O3、CeO2.回收利用这种粉末制得氢氧化铈【Ce(OH)4】和硫酸亚铁的主要流程如下:
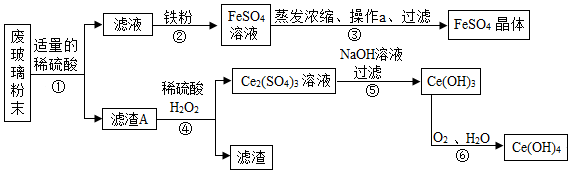
(1)过程①加稀硫酸时,发生反应的化学方程式为___________ ;过程②观察到铁粉溶解,溶液变为___________ 色。过程③中操作a的名称为___________ ;过程④中___________ 被溶解,___________ 成为滤渣。
(3)过程⑤发生的是复分解反应,化学方程式为___________ 。
(4)在过程①~⑥中,___________ (填过程序号)两个过程发生的是化合反应。

(1)过程①加稀硫酸时,发生反应的化学方程式为
(3)过程⑤发生的是复分解反应,化学方程式为
(4)在过程①~⑥中,
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E、F是初中化学常见的6种物质,如图是这些物质间的相互反应及转化关系。其中A、C均为氧化物,B俗称纯碱,F是大理石的主要成分。图中“一”表示两端的物质能发生反应,“→”表示一种物质可转化为另一种物质(部分反应物、生成物及反应条件已略去)。请根据上述条件进行推断并完成下列问题。

(1)写出C的一种用途______________ 。
(2) B→A的反应属于基本反应类型中的______________ 反应。
(3)写出D的化学式______________ 。
(4)写出E→F的反应方程式______________ 。

(1)写出C的一种用途
(2) B→A的反应属于基本反应类型中的
(3)写出D的化学式
(4)写出E→F的反应方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】制盐在我国有着悠久的历史。某盐湖水样品含有 、
、 及少量
及少量 和
和 ,某小组从中获取
,某小组从中获取 和
和 的主要过程如下:
的主要过程如下:
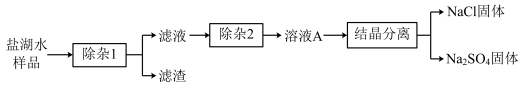
回答下列问题:(除杂限选试剂: 、
、 、
、 、
、
(1)“除杂1”应依次加入的试剂是__________ ;“除杂2”应加入的试剂是__________ 。
(2)写出“除杂2”过程中发生中和反应的化学方程式:__________ 。
 、
、 及少量
及少量 和
和 ,某小组从中获取
,某小组从中获取 和
和 的主要过程如下:
的主要过程如下:
回答下列问题:(除杂限选试剂:
 、
、 、
、 、
、
(1)“除杂1”应依次加入的试剂是
(2)写出“除杂2”过程中发生中和反应的化学方程式:
您最近一年使用:0次
【推荐2】已知某粗盐样品中含有泥沙和Na2SO4、MgCl2、CaCl2等杂质。实验室提纯氯化钠的流程如下:

(1)第①步操作时蒸馏水的最佳使用量约为______ (已知20℃时NaCl的溶解度为36g)。
增加蒸馏水的用量虽然能加快粗盐的溶解,但会引起的不良后果是______ 。实验时若加入的氯化钠没有达到饱和,得精盐产率 __________ (填不变、偏大、偏小)
(2)第②步操作时,两次用到玻璃棒,其作用分别是________ 、 ______________ 。
(3)第⑤步操作加入试剂的顺序是_______
(4)第③⑧步操作a的名称是 ______ ,此步操作中,如果不使用玻璃棒,常常会使产率 ______ (填不变、偏大、偏小)。
(5)在第⑦步操作中,向滤液中滴加足量盐酸的目的是(用化学反应方程式表示)______ 。

(1)第①步操作时蒸馏水的最佳使用量约为
增加蒸馏水的用量虽然能加快粗盐的溶解,但会引起的不良后果是
(2)第②步操作时,两次用到玻璃棒,其作用分别是
(3)第⑤步操作加入试剂的顺序是
| A.过量的氢氧化钠、过量的氯化钡、过量的碳酸钠 |
| B.过量的氯化钡、过量的氢氧化钠、过量的碳酸钠 |
| C.过量的碳酸钠、过量的氯化钡、过量的氢氧化钠 |
| D.过量的氯化钡、过量的碳酸钠、过量的氢氧化钠 |
(5)在第⑦步操作中,向滤液中滴加足量盐酸的目的是(用化学反应方程式表示)
您最近一年使用:0次
【推荐3】为充分开发利用海洋资源,全面促进海洋经济持续健康发展,烟台市近日出台《2014年烟台市海洋经济发展意见》。请围绕“海洋”这个话题回答以下问题:
(1)从海水中提取出的粗盐中除了NaCl外,还含有Ca2+、Mg2+、SO42-及泥沙等杂质,为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。下列操作顺序中最合适的是 。
(2)海水提取出粗盐后的母液中,还含有较多的氯化镁,用氯化镁可制得金属镁。
①工业上从母液中提取氯化镁的过程如下图:反应1的基本反应类型是 ;物质X是 (填名称)。
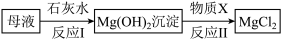
②海水制镁过程中对于如何富集镁离子,甲、乙、丙三位同学各自提出自己的设想:
甲:直接往海水中加入石灰乳
乙:高温加热蒸发海水后,加入石灰乳
丙:向晒盐后的卤水中,加入石灰乳
通过分析比较,你认为 的设想最为经济合理(选填“甲”、“乙”或“丙”).
(3)我国化学家侯德榜在氨碱法的基础上创立的“侯氏制碱法”,是向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出可用作肥料的NH4Cl。NH4Cl和NaCl的溶解度曲线如图所示。
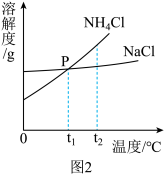
①写出一条P点表示的意义 。
②将t2℃时NH4Cl饱和溶液的温度降到t1℃,溶液中NH4Cl的质量分数会 (填“变大”“变小”“不变”之一)。
③当NH4Cl固体中含有少量NaCl时,可采用 (填“降温结晶”或“蒸发结晶”)的方法提纯NH4Cl。
(1)从海水中提取出的粗盐中除了NaCl外,还含有Ca2+、Mg2+、SO42-及泥沙等杂质,为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。下列操作顺序中最合适的是 。
| A.②④⑤①③ | B.⑤④②③① |
| C.⑤②④③① | D.②⑤④①③ |
①工业上从母液中提取氯化镁的过程如下图:反应1的基本反应类型是 ;物质X是 (填名称)。
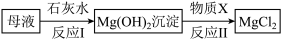
②海水制镁过程中对于如何富集镁离子,甲、乙、丙三位同学各自提出自己的设想:
甲:直接往海水中加入石灰乳
乙:高温加热蒸发海水后,加入石灰乳
丙:向晒盐后的卤水中,加入石灰乳
通过分析比较,你认为 的设想最为经济合理(选填“甲”、“乙”或“丙”).
(3)我国化学家侯德榜在氨碱法的基础上创立的“侯氏制碱法”,是向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出可用作肥料的NH4Cl。NH4Cl和NaCl的溶解度曲线如图所示。

①写出一条P点表示的意义 。
②将t2℃时NH4Cl饱和溶液的温度降到t1℃,溶液中NH4Cl的质量分数会 (填“变大”“变小”“不变”之一)。
③当NH4Cl固体中含有少量NaCl时,可采用 (填“降温结晶”或“蒸发结晶”)的方法提纯NH4Cl。
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】早在战国时期,《周礼●考工记》就记载了我国劳动人民制取KOH以漂洗丝帛的工艺。大意是:先将干燥的木头烧成灰(含K2CO3),用其灰汁浸泡丝帛,再加入石灰即可。如图为模拟该法制取KOH的工艺流程。请回答有关问题。_______ 。
(2)“制浆”中发生反应的化学方程式是_______ 。
(3)“反应池”中发生主要反应的基本反应类型是________ 。
(4)“燃烧窑”中产生的热量可供煅烧和操作_______ (填“①”、“②”或“③”)利用。
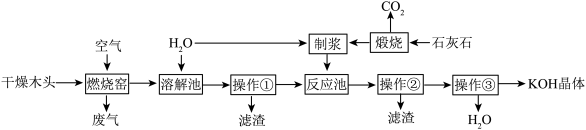
(2)“制浆”中发生反应的化学方程式是
(3)“反应池”中发生主要反应的基本反应类型是
(4)“燃烧窑”中产生的热量可供煅烧和操作
您最近一年使用:0次
【推荐2】为除去白糖中泥沙,可通过溶解、过滤、蒸发等过程。
(1)从物质分类分析,糖水属于_________ (填“纯净物”或“混合物”);从物质变化角度分析,白糖溶于水属于_________ 变化;
(2)溶解、过滤、蒸发得到白糖的过程中,用到的玻璃仪器有烧杯、玻璃棒、酒精灯和_____________ ;
(1)从物质分类分析,糖水属于
(2)溶解、过滤、蒸发得到白糖的过程中,用到的玻璃仪器有烧杯、玻璃棒、酒精灯和
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】我国将从2023年7月1日起禁止销售未达“国六B”标准的燃油车,碳酸锂(Li2CO3)是制备新能源汽车电池的重要原料。如图是一种模拟提纯碳酸锂的工艺,根据要求回答问题。
Ⅰ.锂辉矿主要成分为Li2CO3,含泥沙等杂质;
Ⅱ.Li2CO3 (化学性质与Na2CO3类似)为无色晶体,微溶于水,在冷水中的溶解度比热水中大。
(1)X是一种酸,其溶质化学式为________ ,加入该酸溶液过量的原因主要是_______ 。
(2)写出检验Y气体的化学方程式:___________ ,①②需要分离固体、液体,该操作中玻璃棒的作用是___________ 。
(3)②中发生中和反应的化学方程式为___________ 。
(4)有以下三种温度的饱和Na2CO3溶液,③中你选择的是___________(填字母序号)。
(5)将滤液2蒸发,当有___________ (填现象)时,停止加热,可得到其他化工产品。
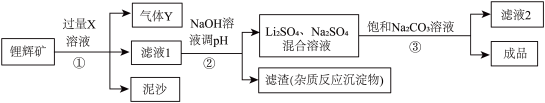
Ⅰ.锂辉矿主要成分为Li2CO3,含泥沙等杂质;
Ⅱ.Li2CO3 (化学性质与Na2CO3类似)为无色晶体,微溶于水,在冷水中的溶解度比热水中大。
(1)X是一种酸,其溶质化学式为
(2)写出检验Y气体的化学方程式:
(3)②中发生中和反应的化学方程式为
(4)有以下三种温度的饱和Na2CO3溶液,③中你选择的是___________(填字母序号)。
| A.0℃ | B.25℃ | C.80℃ |
(5)将滤液2蒸发,当有
您最近一年使用:0次



