A、B、C三种物质的溶解度曲线如图所示,请回答下列问题:

(1)N点对应的是物质A的____ (填“ 饱和”或“不饱和”)溶液。
(2)加热C的饱和溶液,出现浑浊现象,其原因是____________ 。
(3)t1°C时,将A、B、C各8g分别加入盛有50g水的烧杯中,充分溶解,测得三种溶液中溶质的质量分数分别为w(A)、w(B)、w(C),则三者之间的大小关系是____________ 。

(1)N点对应的是物质A的
(2)加热C的饱和溶液,出现浑浊现象,其原因是
(3)t1°C时,将A、B、C各8g分别加入盛有50g水的烧杯中,充分溶解,测得三种溶液中溶质的质量分数分别为w(A)、w(B)、w(C),则三者之间的大小关系是
2019·河南信阳·二模 查看更多[1]
更新时间:2020-03-19 11:06:37
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】A、B、C 三种固体物质的溶解度曲线如图所示,请回答下列问题:

①P点表示 t1℃时,____ 物质的溶解度相等;
②t1℃时,15 g B 物质投入50 g 水中,充分溶解,所得溶液为__________ 溶液(填“饱和”或“不饱和”);
③室温下,将盛有A的饱和溶液的试管放入盛水的烧杯中,再向烧杯内的水中加入一定量的NH4NO3固体并搅拌,试管内可以观察到的现象是__________ ;
④将 A、B、C 三种物质的饱和溶液从 t2 ℃降温到 t1 ℃时,所得溶液中溶质质量分数的大小关系正确的是__________ (填序号)。
a.A>B>C b. B>A>C c. B>A=C

①P点表示 t1℃时,
②t1℃时,15 g B 物质投入50 g 水中,充分溶解,所得溶液为
③室温下,将盛有A的饱和溶液的试管放入盛水的烧杯中,再向烧杯内的水中加入一定量的NH4NO3固体并搅拌,试管内可以观察到的现象是
④将 A、B、C 三种物质的饱和溶液从 t2 ℃降温到 t1 ℃时,所得溶液中溶质质量分数的大小关系正确的是
a.A>B>C b. B>A>C c. B>A=C
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】碳酸钾广泛应用于玻璃、纺织印染和肥皂生产等领域,制取碳酸钾的工艺流程示意图如下:

根据以上图表信息,回答下列问题:
(1)生成碳酸钾的化学方程式为_______ 。
(2)上述流程中可循环使用的物质是_______ 。
(3)得到K2CO3晶浆的结晶方法是_______ 。
(4)上述流程中洗涤K2CO3晶体应选用_______ (填序号)。
①NH4C1溶液 ②热水 ③饱和K2CO3溶液

| 温度/°C | 0 | 10 | 20 | 30 | 40 | 60 | 80 |
| K2CO3的溶解度/g | 107.0 | 109.0 | 111.0 | 114.0 | 117.0 | 126.0 | 139.0 |
(1)生成碳酸钾的化学方程式为
(2)上述流程中可循环使用的物质是
(3)得到K2CO3晶浆的结晶方法是
(4)上述流程中洗涤K2CO3晶体应选用
①NH4C1溶液 ②热水 ③饱和K2CO3溶液
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】KNO3和NaCl在不同温度时的溶解度如下表所示。请回答下列问题:

(1)依据上表数据,绘制出KNO3和NaCl的溶解度曲线如图所示,图中能表示KNO3溶解度曲线的是______ (填“A”或“B”);
(2)由表中数据分析可知, KNO3和NaCl在某一温度时具有相同的溶解度,则温度的取值范围是______ ;
(3)某兴趣小组做了以下实验:

上述实验过程中得到的溶液一定属于不饱和溶液的是______ (填数字序号);
(4)硝酸钾中含有少量氯化钠时,可通过______ (填“蒸发结晶”或“降温结晶”)的方法提纯。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | |

(1)依据上表数据,绘制出KNO3和NaCl的溶解度曲线如图所示,图中能表示KNO3溶解度曲线的是
(2)由表中数据分析可知, KNO3和NaCl在某一温度时具有相同的溶解度,则温度的取值范围是
(3)某兴趣小组做了以下实验:

上述实验过程中得到的溶液一定属于不饱和溶液的是
(4)硝酸钾中含有少量氯化钠时,可通过
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】(1)用NaCl配制100mL0.9%医用的生理盐水(密度约为1g/ mL),需要NaCl的质量为 ___________ g。
(2)由下图可知,t1℃时,硝酸钾溶解度____ 氯化钠的溶解度(填“>”, “<”或“=”)。

(3)从氯化钠和硝酸钾饱和溶液中提取硝酸钾,应采用下列方法中的______ (填写编号)。
a.冷却结晶 b.蒸发溶剂 c.过滤
(4)将t1℃时氯化钠和硝酸钾饱和溶液升温至t3℃时,溶质质量分数氯化钠______ 硝酸钾(填“>”,“<”或“=”)。
(2)由下图可知,t1℃时,硝酸钾溶解度

(3)从氯化钠和硝酸钾饱和溶液中提取硝酸钾,应采用下列方法中的
a.冷却结晶 b.蒸发溶剂 c.过滤
(4)将t1℃时氯化钠和硝酸钾饱和溶液升温至t3℃时,溶质质量分数氯化钠
您最近一年使用:0次
【推荐2】下表是三种物质在不同温度下的溶解度。
(1)20℃时,溶解度最大的物质是_______ 。
(2)饱和的氯化钠溶液转化为不饱和溶液,最好采用的方法是_______ 。
(3)分析上表可知,提纯含少量氯化钠的硝酸钾晶体可用的方法是_______ (填“降温结晶”或“蒸发结晶”)。
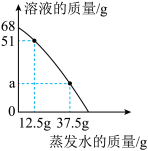
(4)下图为20℃饱和NaC1溶液的质量随蒸发水的质量变化关系图。则a点溶液中溶质质量为___ g。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | |
(2)饱和的氯化钠溶液转化为不饱和溶液,最好采用的方法是
(3)分析上表可知,提纯含少量氯化钠的硝酸钾晶体可用的方法是
(4)下图为20℃饱和NaC1溶液的质量随蒸发水的质量变化关系图。则a点溶液中溶质质量为

您最近一年使用:0次
【推荐3】下表是硝酸钾和氯化钠在不同温度时的溶解度,请回答:
(1)若将上表数据在坐标系中绘制成NaCl和KNO3的溶解度曲线,两条曲线的交点对应的温度范围是______ ;
(2)结合两种物质的溶解度分析,下列说法错误的是______ ;
A.硝酸钾属于易溶物质,氯化钠属于微溶物质
B.两物质中,硝酸钾的溶解度受温度影响较大
C.40℃两物质的饱和溶液中,溶质质量分数较大的是硝酸钾饱和溶液
D.NaCl饱和溶液与不饱和溶液间相互转化时,通常不考虑改变温度来实现
(3)硝酸钾溶液中含有少量的氯化钠,提纯硝酸钾通常采用______ 的方法。
(4)利用20℃时两物质溶解度的差异,可以区分两种白色固体,请写出具体的实验操作和现象______ 。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 /g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(2)结合两种物质的溶解度分析,下列说法错误的是
A.硝酸钾属于易溶物质,氯化钠属于微溶物质
B.两物质中,硝酸钾的溶解度受温度影响较大
C.40℃两物质的饱和溶液中,溶质质量分数较大的是硝酸钾饱和溶液
D.NaCl饱和溶液与不饱和溶液间相互转化时,通常不考虑改变温度来实现
(3)硝酸钾溶液中含有少量的氯化钠,提纯硝酸钾通常采用
(4)利用20℃时两物质溶解度的差异,可以区分两种白色固体,请写出具体的实验操作和现象
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】硝酸钾和氯化钾两种物质的溶解度曲线见图 1。回答下列问题:

(1)交点 P的含义:_______________ ;
(2)60℃时,分别将等质量的 KNO3 和 KCl 两种物质的饱和溶液温度降至 t℃,析出晶体的质量关系为: KNO3____________ KCl(填写“>”“=”或“<”);
(3)如图 2 所示,20℃时,将一定质量的 KNO3固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解。则加入的物质可以是 (填写字母选项)。
①冰块 ②生石灰固体 ③硝酸铵固体 ④干冰 ⑤浓硫酸 ⑥氢氧化钠固体

(1)交点 P的含义:
(2)60℃时,分别将等质量的 KNO3 和 KCl 两种物质的饱和溶液温度降至 t℃,析出晶体的质量关系为: KNO3
(3)如图 2 所示,20℃时,将一定质量的 KNO3固体放入盛水的试管中,发现有少量固体未溶解,向烧杯的水中加入某物质后,试管内固体能完全溶解。则加入的物质可以是 (填写字母选项)。
①冰块 ②生石灰固体 ③硝酸铵固体 ④干冰 ⑤浓硫酸 ⑥氢氧化钠固体
| A.①③④ | B.②⑤⑥ | C.①③⑤ | D.②④⑥ |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】小明同学取一定量的氢氧化钙,加入2ml水并滴加酚酞试液后,分为甲乙两等份。
(1)在试管甲中加入1ml水后振荡,有固体剩余,加热后固体______ (填“消失”或“不消失”)。
(2)在试管乙中加入 1ml 盐酸后振荡,固体消失、红色溶液变为无色,发生反应的化学方程式为_________ 。
(1)在试管甲中加入1ml水后振荡,有固体剩余,加热后固体
(2)在试管乙中加入 1ml 盐酸后振荡,固体消失、红色溶液变为无色,发生反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】如图1是两种固体A、B的溶解度曲线。

(1)在20℃时,将固体A、B各30g 分别加入100g水中,充分溶解后,所得溶液的质量较大的是____ (填“A”或“B”)溶液。
(2)若A中混有少量B,提纯B的方法是______ 。
(3)40℃时,将一定质量的A、B溶液分别进行恒温蒸发,析出晶体的质量与蒸发水的质量关系如图2所示,则40℃时A的溶解度为_______ 。蒸发过程中,溶质质量分数始终保持不变的是_____ (填“A”或“B”)溶液。


(1)在20℃时,将固体A、B各30g 分别加入100g水中,充分溶解后,所得溶液的质量较大的是
(2)若A中混有少量B,提纯B的方法是
(3)40℃时,将一定质量的A、B溶液分别进行恒温蒸发,析出晶体的质量与蒸发水的质量关系如图2所示,则40℃时A的溶解度为

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】化学科学的发展促进了人类社会文明的进步,化学已经渗透到人们生活的各个方面。
(1)①公共卫生:消毒与清洁对公共场所和家庭是至关重要的。洁厕灵、84消毒液是生活中常见的两种清洁、消毒用品,二者若混用会产生一种有毒的气体X,反应的化学方程式为NaClO+2HCl=NaCl+H2O+X↑,则X的化学式为______ 。
②材料研制:2023年2月19日,我国科学家绘出首张蛛丝形成机制分子细胞图谱,为人工合成蛛丝提供了关键理论基础。蛛丝由甘氨酸(C2H5NO2)、丙氨酸(C3H7NO2)等物质组成,具有良好的机械性能和仿生应用潜力,广泛应用于生物医学、高强度复合材料等领域。甘氨酸分子中碳原子与氢原子的个数之比为______ (填最简整数比),丙氨酸中质量分数最小的元素是______ 。
③航天科技:2023年1月14日,中国探月航天太空兔正式命名为“兔星星”和“To star”,体现了传统文化与航天科技的融合。“玉兔号”月球车是中国首辆月球车,月球车上的太阳能电池板主要材料为硅。工业上可利用氢气和四氯化硅(SiCl4)在高温条件下反应制取高纯硅,同时生成了一种有刺激性气味的气体,该反应的化学方程式为______ ,反应后硅元素的化合价______ (填“升高”“降低”“不变”之一)。

(2)我国化学家侯德榜创立了侯氏制碱法,开创了世界制碱工业的新纪元。该技术中生成Na2CO3的同时得到副产品NH4Cl。Na2CO3和NH4Cl的溶解度曲线如图所示。

①在t2℃时,Na2CO3的溶解度______ NH4Cl溶解度(填“大于”“小于”“等于”之一)。
②在t1℃时,向盛有50g水的烧杯中加入15g Na2CO3,充分溶解,得到该温度时Na2CO3的______ (填“饱和”或“不饱和”)溶液。若使烧杯内物质缓慢升温至t2℃(不考虑水分蒸发),在t2℃时,所得溶液中溶质与溶剂的质量之比为______ (填最简整数比)。
③t1℃时,将不同质量的Na2CO3饱和溶液与NH4Cl饱和溶液同时升温至t2℃,此时,Na2CO3溶液的溶质质量分数______ NH4Cl溶液的溶质质量分数(填“大于”“小于”“等于”之一)。
(1)①公共卫生:消毒与清洁对公共场所和家庭是至关重要的。洁厕灵、84消毒液是生活中常见的两种清洁、消毒用品,二者若混用会产生一种有毒的气体X,反应的化学方程式为NaClO+2HCl=NaCl+H2O+X↑,则X的化学式为
②材料研制:2023年2月19日,我国科学家绘出首张蛛丝形成机制分子细胞图谱,为人工合成蛛丝提供了关键理论基础。蛛丝由甘氨酸(C2H5NO2)、丙氨酸(C3H7NO2)等物质组成,具有良好的机械性能和仿生应用潜力,广泛应用于生物医学、高强度复合材料等领域。甘氨酸分子中碳原子与氢原子的个数之比为
③航天科技:2023年1月14日,中国探月航天太空兔正式命名为“兔星星”和“To star”,体现了传统文化与航天科技的融合。“玉兔号”月球车是中国首辆月球车,月球车上的太阳能电池板主要材料为硅。工业上可利用氢气和四氯化硅(SiCl4)在高温条件下反应制取高纯硅,同时生成了一种有刺激性气味的气体,该反应的化学方程式为

(2)我国化学家侯德榜创立了侯氏制碱法,开创了世界制碱工业的新纪元。该技术中生成Na2CO3的同时得到副产品NH4Cl。Na2CO3和NH4Cl的溶解度曲线如图所示。

①在t2℃时,Na2CO3的溶解度
②在t1℃时,向盛有50g水的烧杯中加入15g Na2CO3,充分溶解,得到该温度时Na2CO3的
③t1℃时,将不同质量的Na2CO3饱和溶液与NH4Cl饱和溶液同时升温至t2℃,此时,Na2CO3溶液的溶质质量分数
您最近一年使用:0次





