为了除去氯化钠样品中的碳酸钠杂质,兴趣小组最初设计了如下的方案并进行实验.
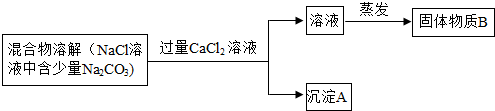
(1)写出沉淀A的化学式______ .
(2)加入CaCl2溶液后,分离除去沉淀A的实验操作方法是______ .
(3)同学在实验过程中,又发现了新的问题:此方案很容易引入新的杂质,请写出固体物质B的成分______ (用化学式表示).
(4)同学继续探究后又提出新的方案:将混合物溶解,若滴加盐酸至不再产生气体为止,则既能除去Na2CO3杂质,又能有效地防止新杂质的引入.写出有关反应的化学方程式:______ .

(1)写出沉淀A的化学式
(2)加入CaCl2溶液后,分离除去沉淀A的实验操作方法是
(3)同学在实验过程中,又发现了新的问题:此方案很容易引入新的杂质,请写出固体物质B的成分
(4)同学继续探究后又提出新的方案:将混合物溶解,若滴加盐酸至不再产生气体为止,则既能除去Na2CO3杂质,又能有效地防止新杂质的引入.写出有关反应的化学方程式:
更新时间:2019-10-24 19:54:52
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】将化学物质进行合理分类是研究物质及其变化的常用方法。
(1)以下物质的分类对于预测其化学性质没有帮助的是_____ (填标号)。
A 二氧化硫属于非金属氧化物
B 锌属于“氢前金属”
C 氢氧化锰属于白色固体
D 硫酸亚铁属于硫酸盐
(2)碳酸锂(Li2CO3)广泛应用于陶瓷和医药等领域,是一种微溶于水的白色固体。结合所学知识预测,Li2CO3能与_______ (填物质类别)反应,验证预测的实验操作与预期现象是:取Li2CO3固体于试管中,__________ 。
(3)依据各类物质之间的反应规律,设计两种制备Li2CO3的方案(要求依据两种不同的反应规律)。完成下表:
(1)以下物质的分类对于预测其化学性质没有帮助的是
A 二氧化硫属于非金属氧化物
B 锌属于“氢前金属”
C 氢氧化锰属于白色固体
D 硫酸亚铁属于硫酸盐
(2)碳酸锂(Li2CO3)广泛应用于陶瓷和医药等领域,是一种微溶于水的白色固体。结合所学知识预测,Li2CO3能与
(3)依据各类物质之间的反应规律,设计两种制备Li2CO3的方案(要求依据两种不同的反应规律)。完成下表:
| 方案 | 原料1 | 原料2 | 预期反应的化学方程式 | 依据的反应规律 |
| ① | Li2SO4溶液 | 两种盐反应生成两种新盐,生成物中有沉淀。 | ||
| ② |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】小梅同学学习了单质、氧化物、酸、碱、盐的性质后,发现许多不同类别的物质反应时能生产盐,于是她构建了如图所示的知识网络图.借助网络图回答:
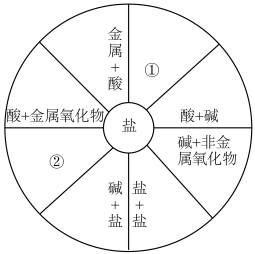
(1)写出用酸和碱生产硫酸铜的化学方程式:_____ .
(2)参照网络图,则图中①②可以是_____ 和_____ (要求不能与图中已有信息重复).

(1)写出用酸和碱生产硫酸铜的化学方程式:
(2)参照网络图,则图中①②可以是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】酸、碱、盐是我们身边重要的化合物,在生活和生产中具有广泛的应用。
(1)两种抗胃酸药剂的主要成分及建议每次剂量见表:
①根据表格写出用盐治疗胃酸过多的化学方程式___ 。
②服用Mg(OH)2的药效比服用NaHCO3“强”的原因是___ 。
(2)下列各组物质能在同一个反应中生成的是 (填字母)。
(3)叠氮酸(HN3)常温下是一种无色液体,其水溶液具有酸性,可与NaOH溶液反应得到叠氮化钠(NaN3),某些汽车安全气囊中装有叠氮化钠。请回答下列问题
①叠氮酸的水溶液中的阴离子是___ (填化学符号)。
②叠氮酸与NaOH溶液的反应的化学方程式是___ 。
(1)两种抗胃酸药剂的主要成分及建议每次剂量见表:
| 主要成分 | 氢氧化镁 | 碳酸氢钠 |
| 建议每次剂量/g | 0.5 | 0.3 |
②服用Mg(OH)2的药效比服用NaHCO3“强”的原因是
(2)下列各组物质能在同一个反应中生成的是 (填字母)。
| A.HCl、AgNO3 | B.Fe(OH)2、NaCl | C.ZnSO4、KNO3 | D.Fe2(SO4)3、H2 |
①叠氮酸的水溶液中的阴离子是
②叠氮酸与NaOH溶液的反应的化学方程式是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】科学探测发现月球贮存有一定数量的冰尘混合物、甲烷(CH4)和钛铁矿(主要成分FeTiO3)资源。人类有望利用月球上的水资源,并通过电解获取氢气为火箭提供燃料,获取的氧气可逐渐形成可供呼吸的大气层,用来满足植物和人类所需。下图是根据科学家设想的有关人类利用月球资源的流程图。
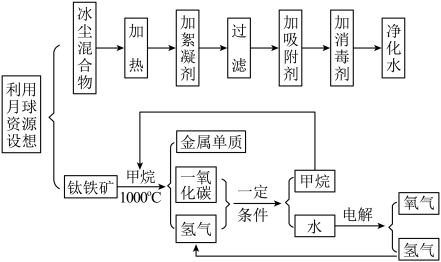
(1)得到净化水的过程中,可做吸附剂的物质有______ (填一种物质名称)。
(2)在过滤时所用的玻璃仪器有漏斗、玻璃棒和______ 。
(3)该流程图中可循环利用的物质是______ (填化学式)。
(4)根据流程图的信息,写出 CO 和H2反应的化学方程式______ 。
(5)水在通电分解过程中电能转化为______ 能。

(1)得到净化水的过程中,可做吸附剂的物质有
(2)在过滤时所用的玻璃仪器有漏斗、玻璃棒和
(3)该流程图中可循环利用的物质是
(4)根据流程图的信息,写出 CO 和H2反应的化学方程式
(5)水在通电分解过程中电能转化为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】实验室废液中含有硝酸银、硝酸铜,实验小组利用稀硫酸和铁粉分离回收银和铜,设计如下,流程图处理:
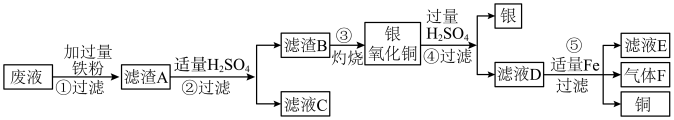
(1)先再废液中加入过量的铁粉,过量的目的是_____ (填序号)。
Ⅰ.加快反应速度 Ⅱ.铁的金属活动性较强 Ⅲ.使反应充分进行
(2)滤渣B的成分__________ ,滤液D中溶质的成分有_________ (填化学式)。
(3)写出步骤反应④的化学方程式__________ 。
(4)写出步骤⑤中生成铜的化学方程式__________ 。
(5)如果在过滤操作中发现滤液浑浊,在仪器洁净、滤纸未破损的前提下,你认为滤液的浑浊的原因可能是_________ 。

(1)先再废液中加入过量的铁粉,过量的目的是
Ⅰ.加快反应速度 Ⅱ.铁的金属活动性较强 Ⅲ.使反应充分进行
(2)滤渣B的成分
(3)写出步骤反应④的化学方程式
(4)写出步骤⑤中生成铜的化学方程式
(5)如果在过滤操作中发现滤液浑浊,在仪器洁净、滤纸未破损的前提下,你认为滤液的浑浊的原因可能是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】MnO2是一种重要的无机功能材料,粗MnO2(含有较多的MnO和MnCO3)的提纯是工业生产的重要环节。查阅资料可知,MnO可以与稀酸反应,但是MnO2不行,学习小组在实验室中模拟工业上粗MnO2转化为纯MnO2的工艺流程。
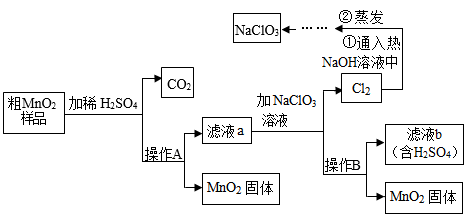
请回答下列问题:
(1)操作A的名称是________ 。
(2)NaClO3中氯元素的化合价为________ 价。
(3)加入稀H2SO4发生的化学方程式为_______ 任写一个)
(4)所得滤液a的溶质有_______ 。
(5)上述流程中可以循环利用的物质有_______ 任写一个) 。

请回答下列问题:
(1)操作A的名称是
(2)NaClO3中氯元素的化合价为
(3)加入稀H2SO4发生的化学方程式为
(4)所得滤液a的溶质有
(5)上述流程中可以循环利用的物质有
您最近一年使用:0次



