酸、碱、盐溶解性表是学习化学的重要工具。下表列出了部分酸、碱、盐在20°C时的溶解性。
请利用此表完成下列任务:
(1)NaNO3的溶解性_____ ;
(2)根据如表写化学式:一种不溶于水的碱_____ ;
(3)判断:氯化钠溶液与硝酸钙溶液能否发生反应及其理由是_____ ;
(4)写出铝与表中的一种盐反应的化学方程式:_____ 。
| OH- | NO3- | Cl- | CO32- | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 不 |
| Cu2+ | 不 | 溶 | 溶 | — |
(1)NaNO3的溶解性
(2)根据如表写化学式:一种不溶于水的碱
(3)判断:氯化钠溶液与硝酸钙溶液能否发生反应及其理由是
(4)写出铝与表中的一种盐反应的化学方程式:
更新时间:2020/03/26 19:40:03
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】我国化学家侯德榜所创立的侯氏联合制碱波,既提高了原料利用率,又“变废为宝”,降低了生产成本,促进了世界制碱技术的发展。侯氏联合制碱法的部分工艺流程如图1。图2为NH4Cl、NaCl、NaHCO3三种物质的溶解度曲线。回答下列问题:
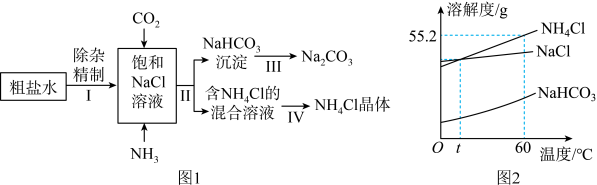
(1)粗盐水中主要含有Na2SO4、MgCl2、CaCl2 三种可溶性杂质,工业上常用加入稍过量的____________ (填化学式,下同)溶液、NaOH溶液、______ 溶液及适量的盐酸等除杂、精制。
(2)Ⅱ中发生反应的化学方程式为______ 。
(3)碳酸氢钠晶体首先从溶液中析出的原因是______ 。
(4)从含氯化铵的混合溶液中得到氯化铵晶体的操作为:蒸发浓缩、______ 过滤、洗涤、干燥。
(5)实验过程中先通入足量氨气,再缓慢通入二氧化碳。先通氨气后通二氧化碳的主要原因是______ 。
(6)将60℃时氯化铵和氯化钠的饱和溶液各100g分别蒸发掉10g水,然后降温至t℃,过滤,得到溶液甲和溶液乙,下列说法正确的是______(填字母)。

(1)粗盐水中主要含有Na2SO4、MgCl2、CaCl2 三种可溶性杂质,工业上常用加入稍过量的
(2)Ⅱ中发生反应的化学方程式为
(3)碳酸氢钠晶体首先从溶液中析出的原因是
(4)从含氯化铵的混合溶液中得到氯化铵晶体的操作为:蒸发浓缩、
(5)实验过程中先通入足量氨气,再缓慢通入二氧化碳。先通氨气后通二氧化碳的主要原因是
(6)将60℃时氯化铵和氯化钠的饱和溶液各100g分别蒸发掉10g水,然后降温至t℃,过滤,得到溶液甲和溶液乙,下列说法正确的是______(填字母)。
| A.甲和乙都是饱和溶液 | B.溶剂的质量:甲<乙 |
| C.溶液的质量:甲>乙 | D.溶质的质量分数:甲=乙 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】物质的结构决定物质的性质,根据物质的结构可以预测物质的化学性质,并推测物质之间的相互转化。
(1)根据上表信息,结合所学化学知识,推断氯化锶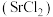 能与
能与_____________________ (填物质的化学式)反应。
(2)已知金属锶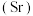 的活动性强于镁。请设计三种制备氯化锶的方案(要求含锶原料分别属于不同的物质类别)。完成下表:
的活动性强于镁。请设计三种制备氯化锶的方案(要求含锶原料分别属于不同的物质类别)。完成下表:
| 锶的化合物 | 氯化锶 | 硫酸锶 | 碳酸锶 | 氢氧化锶 |
| 溶解性 | 易溶于水 | 微溶于水 | 难溶于水 | 可溶于水 |
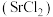 能与
能与(2)已知金属锶
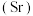 的活动性强于镁。请设计三种制备氯化锶的方案(要求含锶原料分别属于不同的物质类别)。完成下表:
的活动性强于镁。请设计三种制备氯化锶的方案(要求含锶原料分别属于不同的物质类别)。完成下表:| 方案 | 依据的反应规律 | 试剂 | 制备反应方程式 |
| ① | 活泼金属与酸反应,生成盐和氢气 | | |
| ② | 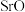 、 、 | ||
| ③ |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】催化剂在化学工业中有着非常重要的作用。五氧化二钒(V2O5)是一种工业催化剂,如图是制取V2O5的工艺流程图(假设每步都恰好完全反应)。请回答:

(1)实验室进行操作a时,用到的玻璃仪器有玻璃棒、烧杯和______ ,其中玻璃棒的作用为______ 。
(2)反应①能发生的条件是______ 。
(3)反应①后获得的沉淀需进行多次洗涤,检验沉淀是否洗净可向最后一次洗涤液样品中加入AgNO3溶液,若未洗净,该过程中发生反应的化学方程式为______ 。
(4)已知物质X为一种有刺激性气味的气体,则反应②的化学方程式为______ ,该反应的基本反应类型是______ 。

(1)实验室进行操作a时,用到的玻璃仪器有玻璃棒、烧杯和
(2)反应①能发生的条件是
(3)反应①后获得的沉淀需进行多次洗涤,检验沉淀是否洗净可向最后一次洗涤液样品中加入AgNO3溶液,若未洗净,该过程中发生反应的化学方程式为
(4)已知物质X为一种有刺激性气味的气体,则反应②的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】向一定质量的CuSO4和MgSO4的混合溶液中,加入一定质量的铝粉和锌粉的混合物,充分反应后过滤,所得滤液的质量等于原混合溶液的质量。
(1)写出一个上述过程中能发生反应的化学方程式_______ 。
(2)所得滤液中一定含有哪些溶质_______ 。(写化学式)
(3)向滤渣上滴加盐酸_______ (填“一定有”“可能有”或“一定没有”)气泡产生。
(1)写出一个上述过程中能发生反应的化学方程式
(2)所得滤液中一定含有哪些溶质
(3)向滤渣上滴加盐酸
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】2022年北京冬奥会计划从废旧电子设备中回收金、银、铜来制作奖牌,现已收集到30kg黄金、4. 1t白银和2. 7t铜。
(1)下列性质中,与金、银、铜可用于制作奖牌无关的是_____ (填字母序号)。
A 有金属光泽
B 导电性好
C 化学性质较稳定
(2)用稀盐酸浸泡可将废旧电子设备中的铝、铁等金属除去,过滤可得到金、银、铜。请写出一个与之相关的化学反应的化学方程式:_____ 。
(3)我国早在西汉时期就有“湿法炼铜”的记载,在《淮南万毕术》一书中就写道“曾青得铁则化为铜”。请你写出与之相关的一个反应的化学方程式:_____ ,其基本反应类型是_____ 。
(4)常温下铝是一种活泼金属,但铝却有较强的抗腐蚀性,其原因是_____ 。
(1)下列性质中,与金、银、铜可用于制作奖牌无关的是
A 有金属光泽
B 导电性好
C 化学性质较稳定
(2)用稀盐酸浸泡可将废旧电子设备中的铝、铁等金属除去,过滤可得到金、银、铜。请写出一个与之相关的化学反应的化学方程式:
(3)我国早在西汉时期就有“湿法炼铜”的记载,在《淮南万毕术》一书中就写道“曾青得铁则化为铜”。请你写出与之相关的一个反应的化学方程式:
(4)常温下铝是一种活泼金属,但铝却有较强的抗腐蚀性,其原因是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】A~J表示初中化学的常见物质,图所示是它们之间的转化关系(部分反应物、生成物和反应条件已略去),已知:A和C、F和H的组成元素相同;E可用作冰箱除味剂;G和J均为红色固体。请回答下列问题:
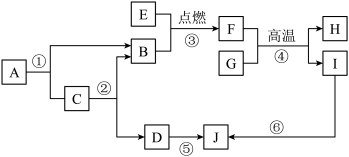
(1)物质E的化学式为______ 。
(2)反应①的化学方程式为______ 。
(3)根据反应⑥可判断I和J金属活动性由强到弱的顺序为______ ,该反应的一个化学方程式为______ 。
(4)反应②所属的基本反应类型为______ 。
(5)反应⑤的一种用途是______ 。

(1)物质E的化学式为
(2)反应①的化学方程式为
(3)根据反应⑥可判断I和J金属活动性由强到弱的顺序为
(4)反应②所属的基本反应类型为
(5)反应⑤的一种用途是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】实验室有溶液样品M,可能含有NH4NO3、NaCl、BaCl2、MgCl2、Na2SO4五种物质中的一种或几种。为确定样品M的成分,设计并完成了如下图所示的实验。
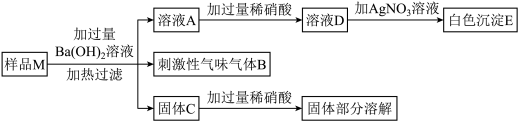
(1)气体B为_______ (填化学式)。
(2)由固体C加入硝酸后部分溶解,可推断固体中一定含有_______ (填化学式)。
(3)原样品M_______ (填“可能有”、“一定有”、“没有”)NaCl。
(4)原样品M溶液一定含有的阳离子_______ 。

(1)气体B为
(2)由固体C加入硝酸后部分溶解,可推断固体中一定含有
(3)原样品M
(4)原样品M溶液一定含有的阳离子
您最近一年使用:0次
【推荐2】分类、类比、推理是学习化学常用的方法。
(1)很多化学实验的设计目的是探究物质的性质,在探究性质实验过程中也会发生物质的变化。
根据实验探究的性质及实验过程中物质发生的变化,应将实验A和_______ (填字母)分为一类,依据是_______ 。
A.二氧化碳的溶解性实验
B.试验酸、碱、盐溶液的导电性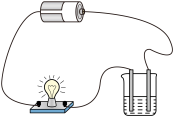
C.比较合金和纯金属的硬度
D.铁丝在氧气中燃烧实验
(2)从九年级教材中的“部分酸碱盐溶解性表”看到碳酸铝一栏是“一”,解释为“表示那种物质不存在或遇到水分解了”,实际上碳酸铝遇水就会分解(也叫水解),碳酸铝水解的化学方程式为:Al2(CO3) 3+3H2O=2A1(OH)3↓+3CO2↑。 碳酸铜和碳酸铝类似,碳酸铜在水中也会水解,请写出CuCl2和Na2CO3在溶液中反应的化学方程式_______ 。已知磷酸盐和碳酸盐的溶解性规律一致, 请回答Ca3(PO4)2的溶解性_______ (填“可溶”或“难溶”)。
(1)很多化学实验的设计目的是探究物质的性质,在探究性质实验过程中也会发生物质的变化。
根据实验探究的性质及实验过程中物质发生的变化,应将实验A和
A.二氧化碳的溶解性实验

B.试验酸、碱、盐溶液的导电性

C.比较合金和纯金属的硬度

D.铁丝在氧气中燃烧实验

(2)从九年级教材中的“部分酸碱盐溶解性表”看到碳酸铝一栏是“一”,解释为“表示那种物质不存在或遇到水分解了”,实际上碳酸铝遇水就会分解(也叫水解),碳酸铝水解的化学方程式为:Al2(CO3) 3+3H2O=2A1(OH)3↓+3CO2↑。 碳酸铜和碳酸铝类似,碳酸铜在水中也会水解,请写出CuCl2和Na2CO3在溶液中反应的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
解题方法
【推荐3】某工厂在粗盐的提纯过程中产生了大量的“盐泥”[主要成分为 、
、 和NaCl]。利用“盐泥”制备硫酸镁晶体的工艺流程如下图所示。
和NaCl]。利用“盐泥”制备硫酸镁晶体的工艺流程如下图所示。
(1)20℃时,NaCl的溶解度为________ g。
(2)“反应器”中反应的化学方程式为________ 。
(3)“过滤器1”产生的“滤渣”为________ 。
(4)“结晶槽”中获得硫酸镁晶体的方法是________ 结晶。
(5)从结晶槽中获得的硫酸镁晶体表面附着有杂质,需用试剂洗去。为避免晶体损失,最适宜的洗涤试剂是________ 。
 、
、 和NaCl]。利用“盐泥”制备硫酸镁晶体的工艺流程如下图所示。
和NaCl]。利用“盐泥”制备硫酸镁晶体的工艺流程如下图所示。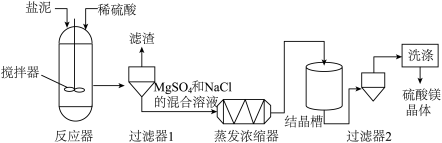
温度/℃ | 0 | 20 | 40 | 60 | 80 |
NaCl溶解度/g | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| 22.0 | 33.7 | 44.5 | 54.6 | 55.8 |
(1)20℃时,NaCl的溶解度为
(2)“反应器”中反应的化学方程式为
(3)“过滤器1”产生的“滤渣”为
(4)“结晶槽”中获得硫酸镁晶体的方法是
(5)从结晶槽中获得的硫酸镁晶体表面附着有杂质,需用试剂洗去。为避免晶体损失,最适宜的洗涤试剂是
您最近一年使用:0次

 溶解度/g
溶解度/g

