已知草酸(H2C2O4)固体与浓硫酸共热发生化学反应:H2C2O4 CO2↑+CO↑+H2O。某化学兴趣小组同学设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁。请根据题目要求回答问题:
CO2↑+CO↑+H2O。某化学兴趣小组同学设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁。请根据题目要求回答问题:
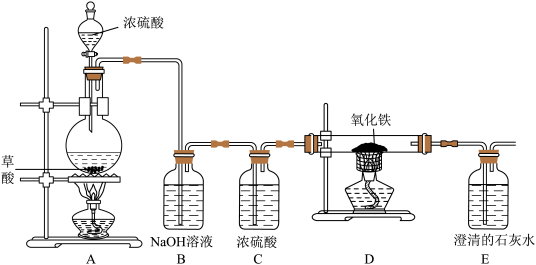
(1)实验开始时,应先点燃_____ 处的酒精灯(填装置序号)。
(2)装置B中的NaOH溶液的作用是_____ ,B、C装置的顺序不能颠倒的原因是_____ 。
(3)从环保角度考虑,上述实验的不足之处是_____ 。反应后玻璃管内固体粉末由红色全部变成黑色,小马同学认为该黑色固体全部是铁,但小军同学提出了质疑,于是小组内的同学们提出查阅资料,寻求真理。
【查阅资料】
①一氧化碳还原Fe2O3的固体产物的成分与反应的温度、时间有关,产物可能是Fe3O4、FeO、Fe;
②几种物质的性质,如下表所示:
③已知反应 :Fe3O4+8HCl=FeCl2+2FeCl3+4H2O, FeCl3溶液呈棕黄色。
【实验探究】
(4)该小组同学将反应后的黑色固体研细后,用磁铁吸引,发现黑色粉末全部被吸引,则该黑色粉末中不可能含有_____ (填化学式)。
(5)黑色固体的成分是什么?
猜想Ⅰ:全部为Fe; 猜想Ⅱ:全部为Fe3O4; 猜想Ⅲ:_____ (填化学式)。
实验:将黑色粉末加入到足量的稀硫酸中,固体全部溶解,观察现象:①有无色气泡产生,证明该固体中一定有_____ (填化学式);②溶液呈棕黄色。
(6)由上述实验现象,得出猜想_____ 正确。
 CO2↑+CO↑+H2O。某化学兴趣小组同学设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁。请根据题目要求回答问题:
CO2↑+CO↑+H2O。某化学兴趣小组同学设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁。请根据题目要求回答问题:
(1)实验开始时,应先点燃
(2)装置B中的NaOH溶液的作用是
(3)从环保角度考虑,上述实验的不足之处是
【查阅资料】
①一氧化碳还原Fe2O3的固体产物的成分与反应的温度、时间有关,产物可能是Fe3O4、FeO、Fe;
②几种物质的性质,如下表所示:
| 物质化学式 | Fe | Fe2O3 | FeO | Fe3O4 |
| 物质的颜色 | 黑色 | 红色 | 黑色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
③已知反应 :Fe3O4+8HCl=FeCl2+2FeCl3+4H2O, FeCl3溶液呈棕黄色。
【实验探究】
(4)该小组同学将反应后的黑色固体研细后,用磁铁吸引,发现黑色粉末全部被吸引,则该黑色粉末中不可能含有
(5)黑色固体的成分是什么?
猜想Ⅰ:全部为Fe; 猜想Ⅱ:全部为Fe3O4; 猜想Ⅲ:
实验:将黑色粉末加入到足量的稀硫酸中,固体全部溶解,观察现象:①有无色气泡产生,证明该固体中一定有
(6)由上述实验现象,得出猜想
更新时间:2020-03-26 19:40:03
|
相似题推荐
科学探究题
|
较难
(0.4)
解题方法
【推荐1】金属及其化合物在生产生活中有广泛的应用。
(一)金属的应用和防护
(1)飞机的燃料是航空煤油,它主要是由____ 炼制的(填“石油”或“煤”)。
(2)铁生锈需要同时接触O2和____ ,请提出生活中铁制品防锈的一种方法____ 。
(3)特种钢中的Mn可以由MnO2和Al粉混合在高温下通过置换反应制得,该化学方程式为____ 。
(4)Mg(OH)2受热分解生成MgO,Mg(OH)2用作阻燃剂,其原理是____ (填字母)。
A 分解吸热,降低环境温度 B MgO覆盖燃烧物,隔绝氧气
(二)制备还原性铁粉
实验室利用废铁屑(含少量Fe2O3)为原料制备还原性铁粉的流程如下:
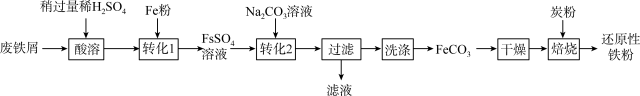
(1)Fe粉可使“酸溶”产生的Fe2(SO4)3转化为FeSO4,该反应的化学方程式为____ 。
(2)检验FeCO3已洗净的方法:取最后一次洗涤后的滤液,先加入一定量稀盐酸,除去CO32-,再滴加____ 溶液,无明显现象。
(3)“干燥”发生转化:FeCO3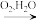 FeOOH+CO2,该转化的化学方程式为
FeOOH+CO2,该转化的化学方程式为____ 。
(4)“焙烧”前,应将炭粉与“干燥”所得固体均匀混合,目的是____ 。
(三)测定还原性铁粉的组成
还原性铁粉中含有少量FexCy,小组同学在老师的指导下进行以下实验。
资料:① Fe,FexCy在加热时与O2反应能生成Fe2O3和CO2。
②FexCy不与酸反应。
实验1:取30.48g样品,加入足量稀H2SO4,充分反应后生成1.00gH2。
实验2:另取30.48g样品,按下图进行实验。
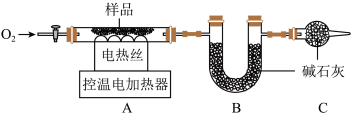
表:装置A和B的质量变化
实验后A中固体全部变为红棕色,装置A、B的质量变化如上表。
(1)装配好装置后,实验前先要____ 。
(2)装置C的作用是____ 。
(3)FexCy中,x:y=____ 。表中m的值是____ g。
【实验反思】:若用空气(除去CO2)的替代O2进行实验,测得x:y的值偏大,可能的原因是____ 。
(一)金属的应用和防护
(1)飞机的燃料是航空煤油,它主要是由
(2)铁生锈需要同时接触O2和
(3)特种钢中的Mn可以由MnO2和Al粉混合在高温下通过置换反应制得,该化学方程式为
(4)Mg(OH)2受热分解生成MgO,Mg(OH)2用作阻燃剂,其原理是
A 分解吸热,降低环境温度 B MgO覆盖燃烧物,隔绝氧气
(二)制备还原性铁粉
实验室利用废铁屑(含少量Fe2O3)为原料制备还原性铁粉的流程如下:

(1)Fe粉可使“酸溶”产生的Fe2(SO4)3转化为FeSO4,该反应的化学方程式为
(2)检验FeCO3已洗净的方法:取最后一次洗涤后的滤液,先加入一定量稀盐酸,除去CO32-,再滴加
(3)“干燥”发生转化:FeCO3
 FeOOH+CO2,该转化的化学方程式为
FeOOH+CO2,该转化的化学方程式为(4)“焙烧”前,应将炭粉与“干燥”所得固体均匀混合,目的是
(三)测定还原性铁粉的组成
还原性铁粉中含有少量FexCy,小组同学在老师的指导下进行以下实验。
资料:① Fe,FexCy在加热时与O2反应能生成Fe2O3和CO2。
②FexCy不与酸反应。
实验1:取30.48g样品,加入足量稀H2SO4,充分反应后生成1.00gH2。
实验2:另取30.48g样品,按下图进行实验。

表:装置A和B的质量变化
| 装置 | A | B |
| 反应前 | 400.00g | 400.00g |
| 反应后 | mg | 400.88g |
实验后A中固体全部变为红棕色,装置A、B的质量变化如上表。
(1)装配好装置后,实验前先要
(2)装置C的作用是
(3)FexCy中,x:y=
【实验反思】:若用空气(除去CO2)的替代O2进行实验,测得x:y的值偏大,可能的原因是
您最近一年使用:0次
【推荐2】在学习了酸的化学性质之后,某实验小组选用稀盐酸做了如下图所示实验。

请回答下列问题:
(1)A烧杯中,铜不与稀盐酸发生反应的原因是________ 。
(2)能产生气泡的是_______ (填字母序号)。
(3)写出C烧杯中反应的实验现象:_________ 。
(4)D烧杯中,溶液由红色变为_______ 色,说明盐酸与氢氧化钠发生了反应。
同学们进一步对D烧杯中反应后的溶液进行探究,对其溶质的成分(除酚酞外)做出如下猜想。
【作出猜想】
猜想一:只含有一种溶质:
猜想二:含有两种溶质。
为了验证上述猜想
【设计方案】
请完成下列表格。
小组同学选用稀硫酸代替稀盐酸重复实验,证明了硫酸与盐酸具有相似的化学性质。酸有一些相似的化学性质,是因为在不同的酸溶液中都含有相同的氢离子。
【发散思维】
某同学利用一黑色粉末(含氧化铜、铁粉,碳粉中的一种或多种)和未知溶质质量分数的稀硫酸做如下探究,将ag黑色粉末加入盛有100g该稀硫酸的烧杯中,充分反应后,称得烧杯内物质质量为(99.8+a)g,该稀硫酸的溶质质量分数不低于______ (填百分数)。

请回答下列问题:
(1)A烧杯中,铜不与稀盐酸发生反应的原因是
(2)能产生气泡的是
(3)写出C烧杯中反应的实验现象:
(4)D烧杯中,溶液由红色变为
同学们进一步对D烧杯中反应后的溶液进行探究,对其溶质的成分(除酚酞外)做出如下猜想。
【作出猜想】
猜想一:只含有一种溶质:
猜想二:含有两种溶质。
为了验证上述猜想
【设计方案】
请完成下列表格。
| 实验操作 | 测定结果 | 得出结论 |
| 用玻璃棒蘸取D烧杯中反应后的溶液,滴在pH试纸上,与标准比色卡比较 | pH<7 | 猜想 |
【发散思维】
某同学利用一黑色粉末(含氧化铜、铁粉,碳粉中的一种或多种)和未知溶质质量分数的稀硫酸做如下探究,将ag黑色粉末加入盛有100g该稀硫酸的烧杯中,充分反应后,称得烧杯内物质质量为(99.8+a)g,该稀硫酸的溶质质量分数不低于
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐3】为探究等质量的锌与过量的盐酸反应速率大小的影响因素,某实验小组设计了以下方案。记录产生气体体积V与反应时间t的数据,根据有关数据绘制得到图1。
【方案设计】
(1)锌与稀盐酸反应的化学方程式是_______________ 。

(2)若通过第1组和第3组实验可以验证温度对金属与酸反应速率的影响,则x的数值应为______ ;若曲线c、d分别表示第3组实验和第1组实验,则温度与反应速率的关系是____________ 。
(3)能验证金属与酸反应速率与盐酸浓度关系的组别是_________ 。
(4)第2组实验对应的曲线是________ 。
【深入探究】图甲是利用数字化仪器的实验装置图、图乙是测得的室温下三种金属片分别与的盐酸反应产生氢气的量。 产生氢气的量用气体压强表示,在等温条件下,产生氢气体积与装置内气压成正比
产生氢气的量用气体压强表示,在等温条件下,产生氢气体积与装置内气压成正比 。
。
(1)实验中消耗质量最多的金属是________ ;
(2)根据图乙,你能得出的结论是____________ 。
【拓展提升】图3是室温下足量的镁片与的盐酸反应装置内气压与时间的关系曲线,结果测得的实际值与通过计算得到的理论值如图所示,请你分析造成以上结果可能的原因(回答两点)。
(1)__________________ ;(2)_____________ 。
【方案设计】
(1)锌与稀盐酸反应的化学方程式是
| 组别 | 盐酸的浓度(%) | 温度(℃) |
| 1 | x | 20 |
| 2 | 10 | 30 |
| 3 | 5 | 30 |
| 4 | 10 | 50 |

(2)若通过第1组和第3组实验可以验证温度对金属与酸反应速率的影响,则x的数值应为
(3)能验证金属与酸反应速率与盐酸浓度关系的组别是
(4)第2组实验对应的曲线是
【深入探究】图甲是利用数字化仪器的实验装置图、图乙是测得的室温下三种金属片分别与的盐酸反应产生氢气的量。
 产生氢气的量用气体压强表示,在等温条件下,产生氢气体积与装置内气压成正比
产生氢气的量用气体压强表示,在等温条件下,产生氢气体积与装置内气压成正比 。
。(1)实验中消耗质量最多的金属是
(2)根据图乙,你能得出的结论是
【拓展提升】图3是室温下足量的镁片与的盐酸反应装置内气压与时间的关系曲线,结果测得的实际值与通过计算得到的理论值如图所示,请你分析造成以上结果可能的原因(回答两点)。
(1)
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】老师给了同学们一包红色粉末,该粉末可能是铜粉和氧化铁(Fe2O3)粉末中的一种或两种。同学们对该粉末进行了定性与定量研究。
(1)定性实验:
写出“红色粉末全部消失”发生反应的化学方程式__________ 。
(2)定量实验:
取该粉末 4g 放入硬质玻璃管中,先通 CO,然后再用酒精喷灯加热一段时间,停止加热继续通入 CO 至装置冷却。实验装置如图:
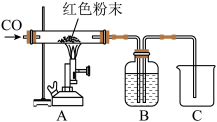
①实验时,先通 CO 再加热的目的是__________ 。
②若该粉末全部是氧化铁,在硬质玻璃管中观察到的实验现象是__________ 。发生的化学反应方程式是__________ 。B 装置是用于吸收二氧化碳并收集 CO,其中盛放的试剂最好是__________ 。
A. NaOH 溶液 B .稀盐酸 C. 水
如果该实验没有装置 B、C,实验造成的危害是__________ 。
(1)定性实验:
| 实验方案 | 实验现象 | 实验结论 |
| 取少量红色粉末放入试管中,滴加足量的稀盐酸振荡 | 红色粉末全部消失,溶液呈棕黄色 | 粉末为 Fe2O3 |
| 粉末 Cu |
(2)定量实验:
取该粉末 4g 放入硬质玻璃管中,先通 CO,然后再用酒精喷灯加热一段时间,停止加热继续通入 CO 至装置冷却。实验装置如图:

①实验时,先通 CO 再加热的目的是
②若该粉末全部是氧化铁,在硬质玻璃管中观察到的实验现象是
A. NaOH 溶液 B .稀盐酸 C. 水
如果该实验没有装置 B、C,实验造成的危害是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】为了解甲酸的分解产物,实验小组进行了以下探究:
[查阅资料]①甲酸(HCOOH)的熔点为8.6℃,能分解生成两种物质;
②氧化铁为红棕色粉末,铁粉为黑色。
[提出猜想]实验小组对甲酸的分解产物提出了猜想:
猜想1.H2和CO2:猜想2.CO和H2O。
[设计实验]20℃时,甲酸的状态为_____ :从图(一)装置中选择合适的装置_____ (填序号)对甲酸进行加热。为了加快分解速率,实验小组加入了催化剂,反应后将分解产物通入图(二)装置进行实验。
 [实验预测]若猜想1成立,则D中的实验现象应为
[实验预测]若猜想1成立,则D中的实验现象应为_____ 。
[进行实验]实验中观察到C处瓶内出现的现象为_____ ,F处玻璃管中出现红棕色粉末变成黑色且G处瓶内无明显现象,则甲酸分解的化学方程式为_____ 。
[交流拓展]资料表明,不同条件下,甲酸的分解产物不同,猜想1和猜想2均能成立。据此小新对甲酸的分解产物又提出新猜想:猜想3.H2O和CO2;猜想4.CO和H2。经讨论认为无须进行实验就能确定猜想3和猜想4都错误,理由是_____ 。
[查阅资料]①甲酸(HCOOH)的熔点为8.6℃,能分解生成两种物质;
②氧化铁为红棕色粉末,铁粉为黑色。
[提出猜想]实验小组对甲酸的分解产物提出了猜想:
猜想1.H2和CO2:猜想2.CO和H2O。
[设计实验]20℃时,甲酸的状态为
 [实验预测]若猜想1成立,则D中的实验现象应为
[实验预测]若猜想1成立,则D中的实验现象应为[进行实验]实验中观察到C处瓶内出现的现象为
[交流拓展]资料表明,不同条件下,甲酸的分解产物不同,猜想1和猜想2均能成立。据此小新对甲酸的分解产物又提出新猜想:猜想3.H2O和CO2;猜想4.CO和H2。经讨论认为无须进行实验就能确定猜想3和猜想4都错误,理由是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】早在春秋战国时期,我国就开始生产和使用铁器。工业炼铁把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
一氧化碳还原氧化铁的化学方程式为:___________ 。其中,石灰石起的作用是 _____________ 。
(一)甲组同学在学习炼铁的相关内容时,对炼铁时还原剂的选择进行了如下探究。
【提出问题】
单质碳也具有还原性,碳还原氧化铁的化学方程式为___________ 。为什么工业上不用焦炭作为还原剂直接还原铁矿石?
【猜想与假设】
焦炭和铁矿石都是固体,接触面积小,反应不易完全。
【进行实验】
①称取两份相同质量的氧化铁粉末。一份与足量的碳粉均匀混合放入图1装置A的试管中;另一份放入图1装置B的玻璃管中。
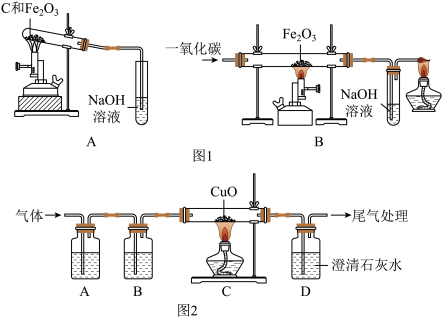
②图1装置A和B两组实验同时开始进行。在图1装置B的反应中,实验开始前应先________ (选填“通CO”或“加热”); 实验结束后应继续通入CO直至冷却至室温,其原因是 ____________ 。
【实验现象】
当图1装置B的玻璃管中固体完全由___________ 时(选填“红色变为黑色”或“黑色变为红色”),图1装置A的试管中仍有 _____________ 。
【解释与结论】
焦炭和铁矿石都是固体,接触面积小,反应确实不易完全,这可能是工业上不用焦炭作为还原剂直接还原铁矿石的一个原因。
【完善实验】
联想到单质碳的一些化学性质,甲同学认为在碳还原氧化铁的反应中可能还会有CO产生。为了证明碳还原氧化铁所得的气体中含有CO和CO2,将该气体通过图2的检验装置。图2A装置中的试剂是(写名称,下同)______________ ,图2B装置中的试剂是氢氧化钠溶液,用以吸收二氧化碳(2NaOH+CO2═Na2CO3+H2O );证明原混合气体中CO2存在的化学方程式 ________ ;证明原混合气体中CO存在的实验现象是 _______ ;经过检验,证实碳还原氧化铁所得的气体中确实含有CO和CO2。
(二)精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
【物质制备】
利用绿矾制备精还原铁粉的工艺流程如下:
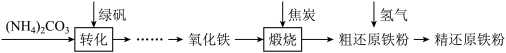
粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为
FexOy+yH2 xFe+yH2O,Fe3C+2H2
xFe+yH2O,Fe3C+2H2 3Fe+CH4。
3Fe+CH4。
【含量测定】
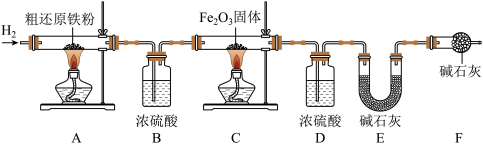
为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按图装置进行实验。
已知3CH4+4Fe2O3 3CO2+6H2O+8Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
3CO2+6H2O+8Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
(1)主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入纯净干燥的H2;
③点燃酒精灯,_______ (填“先点A处,后点C处”或“先点C处,后点A处”);
④分别熄灭A处、C处酒精灯;
⑤再缓缓通入少量H2;
⑥再次称量必要装置的质量
(2)步骤②的目的是_______ ,验证该步骤目的达到的实验方法是 _______ ;
(3)若缺少装置D,则所测氧元素的质量分数将_______ (填“偏大”,“偏小”或“不变”)。
(4)粗还原铁粉样品的质量为15.000g,装置B、E分别增重0.270g和0.330g,则计算样品出中碳、氧元素的质量分数分别是_______
一氧化碳还原氧化铁的化学方程式为:
(一)甲组同学在学习炼铁的相关内容时,对炼铁时还原剂的选择进行了如下探究。
【提出问题】
单质碳也具有还原性,碳还原氧化铁的化学方程式为
【猜想与假设】
焦炭和铁矿石都是固体,接触面积小,反应不易完全。
【进行实验】
①称取两份相同质量的氧化铁粉末。一份与足量的碳粉均匀混合放入图1装置A的试管中;另一份放入图1装置B的玻璃管中。

②图1装置A和B两组实验同时开始进行。在图1装置B的反应中,实验开始前应先
【实验现象】
当图1装置B的玻璃管中固体完全由
【解释与结论】
焦炭和铁矿石都是固体,接触面积小,反应确实不易完全,这可能是工业上不用焦炭作为还原剂直接还原铁矿石的一个原因。
【完善实验】
联想到单质碳的一些化学性质,甲同学认为在碳还原氧化铁的反应中可能还会有CO产生。为了证明碳还原氧化铁所得的气体中含有CO和CO2,将该气体通过图2的检验装置。图2A装置中的试剂是(写名称,下同)
(二)精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
【物质制备】
利用绿矾制备精还原铁粉的工艺流程如下:

粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为
FexOy+yH2
 xFe+yH2O,Fe3C+2H2
xFe+yH2O,Fe3C+2H2 3Fe+CH4。
3Fe+CH4。【含量测定】

为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按图装置进行实验。
已知3CH4+4Fe2O3
 3CO2+6H2O+8Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
3CO2+6H2O+8Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。(1)主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入纯净干燥的H2;
③点燃酒精灯,
④分别熄灭A处、C处酒精灯;
⑤再缓缓通入少量H2;
⑥再次称量必要装置的质量
(2)步骤②的目的是
(3)若缺少装置D,则所测氧元素的质量分数将
(4)粗还原铁粉样品的质量为15.000g,装置B、E分别增重0.270g和0.330g,则计算样品出中碳、氧元素的质量分数分别是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】一些城镇家庭用罐装的液化石油气作燃料,化学兴趣小组对液化石油气的燃烧产物进行探究,请你一同参与并回答下列问题。
[查阅资料]液化石油气的主要成分是丙烷、丁烷、丙烯、丁烯等,这些物质都由碳、氢两种元素组成。
实验一 探究液化石油气完全燃烧的产物
[实验验证](1)将干冷的小烧杯罩在液化石油气燃烧产生的火焰上,观察到烧杯内壁有水雾出现,证明有__________ ,(填化学式)生成。
(2)将干冷的小烧杯罩在液化石油气燃烧产生的火焰上,一段时间后将烧杯迅速倒转并注人澄清石灰水,观察到______________ ,证明有二氧化碳生成。
[交流讨论]生活中我们常常看到用液化石油气做饭后锅底有不少黑色物质,经分析,同学们一致认为该黑色物质是液化石油气不充分燃烧生成的炭黑。由此他们猜想液化石油气燃烧后还可能生成一氧化碳。
实验二 探究液化石油气不完全燃烧 是否会生成一氧化碳
[实验设计]同学们设计了以下实验装置进行验证。
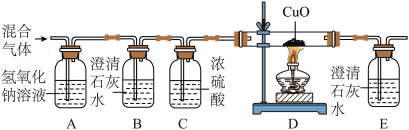
[实验分析](1)将液化石油气燃烧生成的气体依次通过如图所示装置,其中A装置的作用是_________________ 。
(2)观察到B中澄清石灰水不变浑浊,D中黑色粉末变红,E中澄清石灰水变浑浊,说明液化石油气燃烧有一氧化碳生成。写出装置D中发生反应的化学方程式_______________ 。
[反思评价]从环保角度看,该装置存在明显的缺陷,改进方法是_____________ 。
[拓展提高]含碳燃料不充分燃烧会生成一氧化碳等物质,,浪费资源且污染环境。为使其充分燃烧,应采取的措施是____________ (答一条即可)。
[查阅资料]液化石油气的主要成分是丙烷、丁烷、丙烯、丁烯等,这些物质都由碳、氢两种元素组成。
实验一 探究液化石油气完全燃烧的产物
[实验验证](1)将干冷的小烧杯罩在液化石油气燃烧产生的火焰上,观察到烧杯内壁有水雾出现,证明有
(2)将干冷的小烧杯罩在液化石油气燃烧产生的火焰上,一段时间后将烧杯迅速倒转并注人澄清石灰水,观察到
[交流讨论]生活中我们常常看到用液化石油气做饭后锅底有不少黑色物质,经分析,同学们一致认为该黑色物质是液化石油气不充分燃烧生成的炭黑。由此他们猜想液化石油气燃烧后还可能生成一氧化碳。
实验二 探究液化石油气不完全燃烧 是否会生成一氧化碳
[实验设计]同学们设计了以下实验装置进行验证。

[实验分析](1)将液化石油气燃烧生成的气体依次通过如图所示装置,其中A装置的作用是
(2)观察到B中澄清石灰水不变浑浊,D中黑色粉末变红,E中澄清石灰水变浑浊,说明液化石油气燃烧有一氧化碳生成。写出装置D中发生反应的化学方程式
[反思评价]从环保角度看,该装置存在明显的缺陷,改进方法是
[拓展提高]含碳燃料不充分燃烧会生成一氧化碳等物质,,浪费资源且污染环境。为使其充分燃烧,应采取的措施是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】我校兴趣小组进行木炭、一氧化碳与氧化铜反应的探究实验,回答相关问题。
实验一:如图实验进行碳还原氧化铜实验,

【查阅资料】
(1)氧化亚铜(Cu2O) 是红色固体,能与稀硫酸发生如下反应: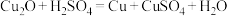 。
。
【提出问题】已知实验后试管中的红色固体含有单质铜,是否还含有氧化亚铜(Cu2O) 呢?
【实验验证】取试管中的红色固体少量于试管中,加入_________ 溶液,试管中出现__________ ,证明固体中确实含有Cu2O。
(2)从定量计算角度判断测定表格中的四个数据:①若只有CO2生成,理论上m4- m3______ m1-m2(选填“>”、“<”或“=”),A中发生反应的化学方程式是_____________ ,实际上生成的气体还有CO,分析产生CO的可能原因(写一个)__________________ 。
②实验结束时先拔掉A处试管口的橡皮塞,再停止对试管加热,其目的是________________ 。
实验二:同学们对另一份氧化铜样品中氧化铜的含量进行测定。他们称取了20g固体氧化铜样品,用图1所示的装置进行实验,至反应完全(杂质不参与反应,石灰水足量),测定的部分数据如图2所示:

(1)澄清石灰水的作用是________________ 。
(2)有同学认为图1装置不够完善,为了防止尾气对空气的污染,应该把图1装置中的盛有澄清石灰水的装置换成下列____________ 装置(填字母序号)。

(3)用补救后的装置进行此实验,加热前先通一会儿一氧化碳的目的是________________ 。
(4)图2中M点的含义是________________ 。
(5)该样品中氧化铜的质量分数为________________ 。
(6)本实验中其他条件不变,只把CO换为H2进行实验,所得氧化铜样品中氧化铜的质量分数为_________ (填“相同”或“不相同”)。
实验一:如图实验进行碳还原氧化铜实验,

【查阅资料】
(1)氧化亚铜(Cu2O) 是红色固体,能与稀硫酸发生如下反应:
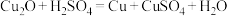 。
。【提出问题】已知实验后试管中的红色固体含有单质铜,是否还含有氧化亚铜(Cu2O) 呢?
【实验验证】取试管中的红色固体少量于试管中,加入
(2)从定量计算角度判断测定表格中的四个数据:①若只有CO2生成,理论上m4- m3
反应前的质量 | 反应后的质量 | |
装置A | m1 | m2 |
装置B | m3 | m4 |
实验二:同学们对另一份氧化铜样品中氧化铜的含量进行测定。他们称取了20g固体氧化铜样品,用图1所示的装置进行实验,至反应完全(杂质不参与反应,石灰水足量),测定的部分数据如图2所示:

(1)澄清石灰水的作用是
(2)有同学认为图1装置不够完善,为了防止尾气对空气的污染,应该把图1装置中的盛有澄清石灰水的装置换成下列

(3)用补救后的装置进行此实验,加热前先通一会儿一氧化碳的目的是
(4)图2中M点的含义是
(5)该样品中氧化铜的质量分数为
(6)本实验中其他条件不变,只把CO换为H2进行实验,所得氧化铜样品中氧化铜的质量分数为
您最近一年使用:0次
科学探究题
|
较难
(0.4)
真题
【推荐3】某CO气体中混有少量的CO2,为探究CO的性质,某同学在老师的指导下设计了以下实验装置,请填写下列空白.
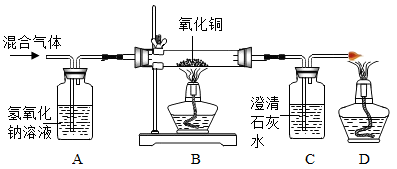
(1)A装置的作用是___________ .B处玻璃管内的现象是___________ .
(2)C处反应的化学方程式为___________ ;
(3)实验时,应___________ (选填“先”或“后”)点燃B处的酒精灯;
(4)某同学对B处玻璃管内剩余固体成分产生浓厚兴趣.
【提出问题】B处玻璃管内的剩余固体是什么?
【假设猜想】猜想①:剩余固体全部是铜 猜想②:剩余固体是铜和氧化铜的混合物
【实验设计】
【拓展延伸】
(Ⅰ)D处酒精灯的作用是___________ ;
(Ⅱ)根据B处的反应原理,CO可用于___________ .

(1)A装置的作用是
(2)C处反应的化学方程式为
(3)实验时,应
(4)某同学对B处玻璃管内剩余固体成分产生浓厚兴趣.
【提出问题】B处玻璃管内的剩余固体是什么?
【假设猜想】猜想①:剩余固体全部是铜 猜想②:剩余固体是铜和氧化铜的混合物
【实验设计】
| 实验步骤 | 实验中可能出现的现象 | 结论 |
| 取B处玻璃管内少量剩余固体于试管中加入 | 现象一:固体不溶解,溶液不变色 | 猜想① |
| 现象二: | 猜想②成立 |
【拓展延伸】
(Ⅰ)D处酒精灯的作用是
(Ⅱ)根据B处的反应原理,CO可用于
您最近一年使用:0次
【推荐1】兴趣小组同学在老师的带领下,探究影响过氧化氢分解速率的因素。
【提出问题】影响过氧化氢分解的因素有哪些?
【做出假设】假设1:催化剂的种类
假设2:过氧化氢溶液的浓度
假设3:温度
【实验探究】学生利用如图所示装置,以收集50mL的气体为标准,比较反应的快慢,实验方案如下表所示:
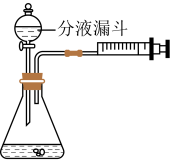
(1)写出实验3发生反应的文字表达式________ 。
(2)对比实验1和2,得出的结论是_______ 。
(3)通过对比实验1和3,得出二氧化锰的催化效果比氧化铜强的实验依据是_______ 。
(4)实验中,使用注射器的优点是______ 。
【拓展延伸】在实验3探究中,学生将注射器换成了压强传感器,测出了实验过程中装置压强与时间的关系图(如图2)。实验过程中,学生触摸锥形瓶外壁,有发烫的感觉,至反应结束后,发生装置的温度慢慢趋于常温。
(5)根据实验探究推知,过氧化氢分解的反应是_____ (填“吸热”或“放热”)反应;
(6)根据图2所示,我们分析发现:反应速率在不断发生改变。反应过程中从开始到结束影响反应速率的因素有______ (填2种)
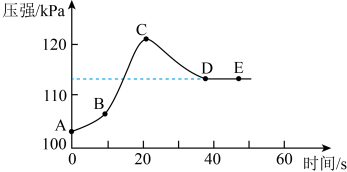
(7)图2中,CD段压强降低的主要原因是________ 。
【提出问题】影响过氧化氢分解的因素有哪些?
【做出假设】假设1:催化剂的种类
假设2:过氧化氢溶液的浓度
假设3:温度
【实验探究】学生利用如图所示装置,以收集50mL的气体为标准,比较反应的快慢,实验方案如下表所示:

| 序号12 | 温度/℃ | 过氧化氢溶液浓度 | 过氧化氢溶液体积/m | 1g催化剂 | 时间/S |
| 1 | 20 | 5% | 40 | 二氧化锰 | 37 |
| 2 | 20 | 10% | 40 | 二氧化锰 | 14 |
| 3 | 20 | 5% | 40 | 氧化铜 | b |
| 4 | 80 | 5% | 40 | 二氧化锰 | 29 |
(1)写出实验3发生反应的文字表达式
(2)对比实验1和2,得出的结论是
(3)通过对比实验1和3,得出二氧化锰的催化效果比氧化铜强的实验依据是
(4)实验中,使用注射器的优点是
【拓展延伸】在实验3探究中,学生将注射器换成了压强传感器,测出了实验过程中装置压强与时间的关系图(如图2)。实验过程中,学生触摸锥形瓶外壁,有发烫的感觉,至反应结束后,发生装置的温度慢慢趋于常温。
(5)根据实验探究推知,过氧化氢分解的反应是
(6)根据图2所示,我们分析发现:反应速率在不断发生改变。反应过程中从开始到结束影响反应速率的因素有

(7)图2中,CD段压强降低的主要原因是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐2】全世界每年因锈蚀造成浪费的金属高达产量的20%以上,但铁锈蚀原理却在日常生活中被广泛应用,例如暖宝宝、食品脱氧剂等。小组同学对暖宝宝发热产生兴趣,展开探究。
【资料信息】
成分:铁粉、蛭石(保温)、高分子吸水树脂(供水)、氯化钠、活性炭
内袋材料:微孔透气无纺布
注意事项:不使用时请勿拆开密封包装
【实验1】探究自制暖宝宝与市售暖宝宝的发热效果
(1)分别取2勺铁粉和活性炭,加入无纺布袋中(与市售暖宝宝所用无纺布相同),滴加少量氯化钠溶液,混合均匀制得暖宝宝。在相同环境下,利用温度传感器测定自制与市售暖宝宝温度随时间的变化,形成图像,如图所示。通过图像可知自制暖宝宝有两点不足分别是:______ ,______ 。

【猜想与假设】暖宝宝成分中氯化钠、活性炭可能加快铁锈蚀速率,使反应在短时间内放出大量的热。
【实验2】探究“暖宝宝”反应原理与铁的生锈本质是否一致
按图1(夹持仪器已略去)采用氧气、温度、湿度传感器收集数据,将拆除包装的暖宝宝倒入三颈烧瓶中密封装置,开始收集数据,观察曲线变化(如图2中图A、B、C)。
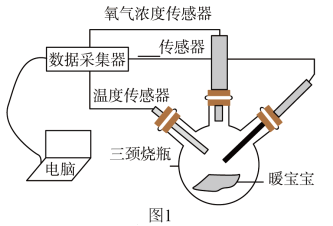
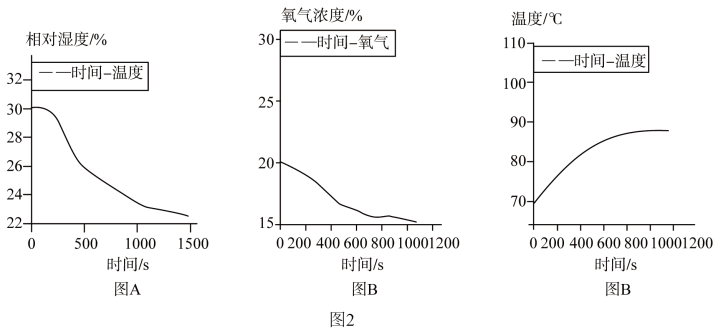
(2)从收集到的图像看暖宝宝发热是因为颗粒微小的铁粉与______ 发生反应,并______ 热量(填“吸收”或“放出”),这一反应与铁生锈原理一致。
【实验3】探究氯化钠、活性炭及两者共同存在对铁锈蚀速率的影响
设计完成如下4组实验(实验在密闭容器中进行),小组同学记录反应过程中温度的变化。
【解释与结论】
(3)对比实验Ⅰ和Ⅱ,可探究氯化钠对铁锈蚀速率的影响,表中m=______ 。
(4)为探究活性炭对铁锈蚀速率的影响,应选择的实验组合是______ (填编号)。
【实验4】测定市售暖宝宝中铁粉的含量
【实验设计】研究小组设计了如由图3所示的装置进行含量测定

【查阅资料】
①铁能与稀硫酸反应生成硫酸亚铁和氢气。②该实验条件下,氢气的密度约为ρg/L。
【实验步骤】
①连接好仪器,检查装置气密性;
②称取mg的样品于烧瓶中,并在分液漏斗中加入足量稀硫酸;
③反应前将液面调节到量气管的“0”刻度,并使两边液面相平;
④打开分液漏斗活塞,逐滴滴入稀硫酸,至不再产生气泡时,关闭活塞;
⑤……量气管读数为amL;
⑥用量筒测量圆底烧瓶内的剩余液体,读数为bmL。
请完成下列问题:
(5)检查装置气密性的方法是______ 。
(6)装置B中盛放的液体及其作用是______ 。
(7)步骤⑤中读数前的操作为______ 。
(8)根据实验数据计算该暖宝宝中铁粉的质量分数为______ (用含字母的式子表示)。
(9)若实验测得该暖宝宝中铁粉的质量分数比实际值偏低,可能原因是______(填字母)。
【资料信息】
成分:铁粉、蛭石(保温)、高分子吸水树脂(供水)、氯化钠、活性炭
内袋材料:微孔透气无纺布
注意事项:不使用时请勿拆开密封包装
【实验1】探究自制暖宝宝与市售暖宝宝的发热效果
(1)分别取2勺铁粉和活性炭,加入无纺布袋中(与市售暖宝宝所用无纺布相同),滴加少量氯化钠溶液,混合均匀制得暖宝宝。在相同环境下,利用温度传感器测定自制与市售暖宝宝温度随时间的变化,形成图像,如图所示。通过图像可知自制暖宝宝有两点不足分别是:

【猜想与假设】暖宝宝成分中氯化钠、活性炭可能加快铁锈蚀速率,使反应在短时间内放出大量的热。
【实验2】探究“暖宝宝”反应原理与铁的生锈本质是否一致
按图1(夹持仪器已略去)采用氧气、温度、湿度传感器收集数据,将拆除包装的暖宝宝倒入三颈烧瓶中密封装置,开始收集数据,观察曲线变化(如图2中图A、B、C)。


(2)从收集到的图像看暖宝宝发热是因为颗粒微小的铁粉与
【实验3】探究氯化钠、活性炭及两者共同存在对铁锈蚀速率的影响
设计完成如下4组实验(实验在密闭容器中进行),小组同学记录反应过程中温度的变化。
| 实验编号 | 铁粉/g | 水/mL | 活性炭/g | 氯化钠/g | 测得10min内温度 上升值/℃ |
| Ⅰ | 2 | 5 | 0 | 0 | 0.1 |
| Ⅱ | 2 | 5 | m | 0.1 | 3.1 |
| Ⅲ | 2 | 5 | 0.2 | 0 | 22.0 |
| Ⅳ | 2 | 5 | 0.2 | 0.1 | 56.3 |
(3)对比实验Ⅰ和Ⅱ,可探究氯化钠对铁锈蚀速率的影响,表中m=
(4)为探究活性炭对铁锈蚀速率的影响,应选择的实验组合是
【实验4】测定市售暖宝宝中铁粉的含量
【实验设计】研究小组设计了如由图3所示的装置进行含量测定

【查阅资料】
①铁能与稀硫酸反应生成硫酸亚铁和氢气。②该实验条件下,氢气的密度约为ρg/L。
【实验步骤】
①连接好仪器,检查装置气密性;
②称取mg的样品于烧瓶中,并在分液漏斗中加入足量稀硫酸;
③反应前将液面调节到量气管的“0”刻度,并使两边液面相平;
④打开分液漏斗活塞,逐滴滴入稀硫酸,至不再产生气泡时,关闭活塞;
⑤……量气管读数为amL;
⑥用量筒测量圆底烧瓶内的剩余液体,读数为bmL。
请完成下列问题:
(5)检查装置气密性的方法是
(6)装置B中盛放的液体及其作用是
(7)步骤⑤中读数前的操作为
(8)根据实验数据计算该暖宝宝中铁粉的质量分数为
(9)若实验测得该暖宝宝中铁粉的质量分数比实际值偏低,可能原因是______(填字母)。
| A.测定气体体积时未冷却至室温 |
| B.反应结束后圆底烧瓶中有H2残留 |
| C.测定气体体积时水准管的液面高于量气管的液面 |
| D.测量过程中有气体泄漏 |
您最近一年使用:0次
【推荐3】铁系脱氧剂在食品包装中广泛使用。某同学对铁系脱氧剂进行以下探究。
【查阅资料】
①铁系脱氧剂是以铁粉为主剂,还含有活性炭、氯化钠、氯化钙、硅藻土、碳酸钠晶体等功能扩展剂。
②硅藻土主要成分为二氧化硅,不能与稀酸反应。
探究一:探究铁系脱氧剂的脱氧原理
【进行实验】在盛有干燥空气的广口瓶中进行实验,用氧气浓度传感器测定相同时间内氧气含量的变化,记录如下:
(1)铁系脱氧剂脱氧的原理是铁粉与____________ 反应生成铁锈。
(2)欲得出“氯化钠能加快铁粉脱氧速率”,依据的实验是_____________ 。
探究二:探究铁系脱氧剂成分、铁粉活化程度对脱氧效果的影响
【进行实验】常温下,将5组不同配方的脱氧剂分别放入大小相同的5个锥形瓶中进行实验,实验方案如下表所示:
最终测得实验数据如下图所示
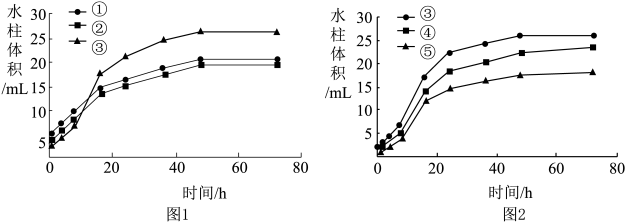
【解释与结论】
(3)实验过程中,均能观察到导管内水柱上升,其原因是_________ 。
(4)对比图1中的实验数据,可得出铁系脱氧剂最佳配方的实验是___________ 。
(5)设计实验③④⑤的目的是_________ 。
【反思与评价】
(6)欲证明铁系脱氧剂中含有碳酸盐,所需试剂是___________ 。
(7)检验铁系脱氧剂仍有效的实验方案是:将打开的脱氧剂置于滤纸上,并用磁铁吸引,取磁铁上的黑色粉末于试管中,加入_________ 。
【查阅资料】
①铁系脱氧剂是以铁粉为主剂,还含有活性炭、氯化钠、氯化钙、硅藻土、碳酸钠晶体等功能扩展剂。
②硅藻土主要成分为二氧化硅,不能与稀酸反应。
探究一:探究铁系脱氧剂的脱氧原理
【进行实验】在盛有干燥空气的广口瓶中进行实验,用氧气浓度传感器测定相同时间内氧气含量的变化,记录如下:
实验 | 序号 | 铁粉 | 碳粉 | 其他试剂 | 氧气含量 |
| ① | 5.0g | 0.1g | 无 | 21% |
② | 5.0g | 0.1g | 10滴水 | 15% | |
③ | 5.0g | 0.1g | 10滴水和1.0 g NaCl | 8% |
(2)欲得出“氯化钠能加快铁粉脱氧速率”,依据的实验是
探究二:探究铁系脱氧剂成分、铁粉活化程度对脱氧效果的影响
【进行实验】常温下,将5组不同配方的脱氧剂分别放入大小相同的5个锥形瓶中进行实验,实验方案如下表所示:
① | ② | ③ | ④ | ⑤ | 实验装置 | |
铁粉活化程度 | 新制 | 新制 | 新制 | 久制 | 还原 |
|
铁粉质量/g | 0.3 | 0.3 | 0.3 | 0.3 | 0.3 | |
活性炭质量/g | 0.1 | 0.1 | 0 | 0 | 0 | |
NaCl质量/g | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | |
CaCl2质量/g | 0 | 0.1 | 0 | 0 | 0 | |
碳酸钠晶体质量/g | 0 | 0 | 0.1 | 0.1 | 0.1 | |
硅藻土质量/g | 0.1 | 0 | 0.1 | 0.1 | 0.1 |

【解释与结论】
(3)实验过程中,均能观察到导管内水柱上升,其原因是
(4)对比图1中的实验数据,可得出铁系脱氧剂最佳配方的实验是
(5)设计实验③④⑤的目的是
【反思与评价】
(6)欲证明铁系脱氧剂中含有碳酸盐,所需试剂是
(7)检验铁系脱氧剂仍有效的实验方案是:将打开的脱氧剂置于滤纸上,并用磁铁吸引,取磁铁上的黑色粉末于试管中,加入
您最近一年使用:0次





