名校
1 . 现有五种物质A、B、C、D、E,其中C是碱,其余四种是盐,且B为钠盐,溶于水后电离可以产生下表中的离子:
为鉴别它们,分别完成以下实验。其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E。沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)写出下列物质的名称:X______ 。
(2)B溶于水后的电离方程式为______ 。
(3)按要求完成以下水溶液中的反应方程式:
①A溶液与B溶液反应的化学方程式:______ 。
②B溶液与E沉淀反应的化学方程式:______ 。
③写出B与C反应至溶液呈中性的离子方程式:______ 。
(4)D与E的混合物ag,加入足量盐酸,充分反应后生成标准状况时的气体bL,则D在混合物中的质量分数为______ 。(列出计算式即可)
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH-   |
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E。沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)写出下列物质的名称:X
(2)B溶于水后的电离方程式为
(3)按要求完成以下水溶液中的反应方程式:
①A溶液与B溶液反应的化学方程式:
②B溶液与E沉淀反应的化学方程式:
③写出B与C反应至溶液呈中性的离子方程式:
(4)D与E的混合物ag,加入足量盐酸,充分反应后生成标准状况时的气体bL,则D在混合物中的质量分数为
您最近半年使用:0次
解题方法
2 . 科学工作者研发了一种SUNCAT系统,借助该系统利用如图所示的原理可持续合成氨.下列说法正确的是
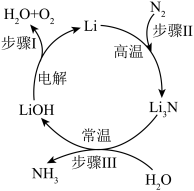
| A.步骤Ⅰ将化学能转化为电能电解 |
| B.步骤Ⅰ的基本反应类型属于置换反应 |
C.步骤Ⅱ的化学方程式是 |
| D.该系统工作过程中理论上步骤Ⅰ生成的水和步骤Ⅲ消耗的水的质量比为1:2 |
您最近半年使用:0次
解题方法
3 . 该小组为了探索CO还原Fe2O3与温度的关系,走访了某钢铁厂。工程师用SDTQ热分析仪对该反应进行研究,根据不同温度下所得固体的质量,推导对应的固体成分,结果如图。___________ ℃(填“400”“600”或“800”)。
(2)图中:x=___________ 。
(3)该小组查阅资料得知酒精灯加热温度为600℃左右,他们发现上述对黑色固体成分的检验结果与图像有矛盾,推测黑色固体在冷却过程中发生了以下反应:___  Fe3O4+
Fe3O4+___ (请将化学方程式补充完整)。
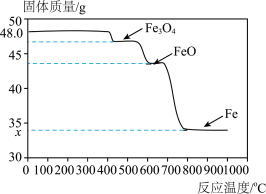
(2)图中:x=
(3)该小组查阅资料得知酒精灯加热温度为600℃左右,他们发现上述对黑色固体成分的检验结果与图像有矛盾,推测黑色固体在冷却过程中发生了以下反应:
 Fe3O4+
Fe3O4+
您最近半年使用:0次
4 . 图中A~I表示初中化学常见的物质。A是单质;G是氧化物,呈黑色,其中氧元素的质量分数为20%;D俗称纯碱;E是生物体中含量最多的物质;H常用于改良酸性土壤。图中“—”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;反应条件、部分反应物或生成物已略去。______ ,D______ 。
(2)写出A与G反应的化学方程式______ 。
(3)写出I→D反应的化学方程式______ 。
(4)E→H的基本反应类型是______ 。
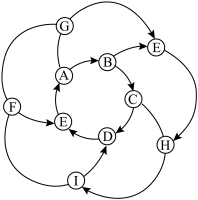
(2)写出A与G反应的化学方程式
(3)写出I→D反应的化学方程式
(4)E→H的基本反应类型是
您最近半年使用:0次
解题方法
5 . 宋朝王希孟的《千里江山图》历经千年,依旧色彩艳丽的关键在于使用了石青、石绿、赭石等传统颜料。某化学兴趣小组对石青和石绿的性质进行了以下探究。
查阅资料:石青的主要成分是2CuCO3•Cu(OH)2,石绿的主要成分是CuCO3•Cu(OH)2,都可称为碱式碳酸铜;碱式碳酸铜的化学式可表示为xCuCO3•yCu(OH)2,其中“•”表示合的意思,x、y为正整数;CuCO3、Cu(OH)2受热时会分解得到相应的氧化物。
I.探究石青和石绿的化学性质
(1)《本草纲目》载:铜得紫阳之气(二氧化碳、水蒸气、氧气)而生绿,绿久则成石,谓之石绿。请用化学方程式表示石绿的形成过程:_______ 。
(2)取少量石青粉末于试管中,充分加热后观察到试管中固体变黑,产生的气体通入到盛有澄清石灰水的烧杯中,溶液变浑浊。该黑色固体为_______ (填化学式)。
(3)取少量石绿粉末于试管中,加入足量稀硫酸,观察到固体溶解,产生气泡,溶液由无色变成蓝色。溶液中含有的盐类物质为_______ (填化学式)。
结论:碱式碳酸铜受热可分解,且可与酸反应。
II.测定某种碱式碳酸铜[为xCuCO3•yCu(OH)2]的组成。
利用如图所示装置进行实验(实验中每一步吸收都是完全的)。_______ ;②装入药品:③打开活塞K,鼓人空气;④一段时间后关闭活塞K,称量相关装置的质量;⑤点燃酒精灯,至装置B中无气泡产生;⑥打开活塞K,鼓入空气;⑦熄灭酒精灯;⑧一段时间后关闭活塞K,称量相关装置质量。
注:碱石灰主要成分为氢氧化钠和氧化钙固体,能吸收水和二氧化碳。
(5)C装置中U形管内碱石灰的作用是_______ 。
(6)若碱式碳酸铜已完全分解,实验后装置B增重4.5g,装置C增重4.4g,则该碱式碳酸铜的化学式可表示为_______ 。
III.感悟青绿
在古代,广义上青色可以代指绿色一蓝色一紫色一黑色,“青色”在文化意义上是一种虚指的颜色,常见的有玄青(氧化铜),曾青(硫酸铜),丹青(铜),青绿(碱式碳酸铜),这些颜色是中国文化的一个缩影。
(7)“曾青转化为丹青”的化学反应原理是_______ (用化学方程式表示)。
查阅资料:石青的主要成分是2CuCO3•Cu(OH)2,石绿的主要成分是CuCO3•Cu(OH)2,都可称为碱式碳酸铜;碱式碳酸铜的化学式可表示为xCuCO3•yCu(OH)2,其中“•”表示合的意思,x、y为正整数;CuCO3、Cu(OH)2受热时会分解得到相应的氧化物。
I.探究石青和石绿的化学性质
(1)《本草纲目》载:铜得紫阳之气(二氧化碳、水蒸气、氧气)而生绿,绿久则成石,谓之石绿。请用化学方程式表示石绿的形成过程:
(2)取少量石青粉末于试管中,充分加热后观察到试管中固体变黑,产生的气体通入到盛有澄清石灰水的烧杯中,溶液变浑浊。该黑色固体为
(3)取少量石绿粉末于试管中,加入足量稀硫酸,观察到固体溶解,产生气泡,溶液由无色变成蓝色。溶液中含有的盐类物质为
结论:碱式碳酸铜受热可分解,且可与酸反应。
II.测定某种碱式碳酸铜[为xCuCO3•yCu(OH)2]的组成。
利用如图所示装置进行实验(实验中每一步吸收都是完全的)。
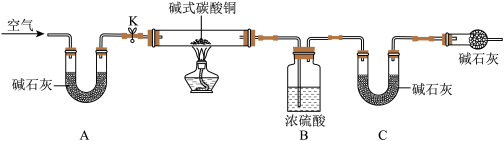
注:碱石灰主要成分为氢氧化钠和氧化钙固体,能吸收水和二氧化碳。
(5)C装置中U形管内碱石灰的作用是
(6)若碱式碳酸铜已完全分解,实验后装置B增重4.5g,装置C增重4.4g,则该碱式碳酸铜的化学式可表示为
III.感悟青绿
在古代,广义上青色可以代指绿色一蓝色一紫色一黑色,“青色”在文化意义上是一种虚指的颜色,常见的有玄青(氧化铜),曾青(硫酸铜),丹青(铜),青绿(碱式碳酸铜),这些颜色是中国文化的一个缩影。
(7)“曾青转化为丹青”的化学反应原理是
您最近半年使用:0次
6 . 在托盘天平的两边各放一只烧杯,调节天平至平衡,向两烧杯中分别注入等质量、等质量分数的稀硫酸(足量),向其中一只烧杯中投入2.2gCuO,发生反应的化学方程式为_______ ,要使天平保持平衡,向另一只烧杯中加入适量的镁,则加入镁的质量为______ g。
您最近半年使用:0次
解题方法
7 . 非整比化合物可用于制作新型功能材料,这类化合物中各类原子的相对数目不能用简单整数比表示,具有很大的科技价值。如Fe0.9O可应用于CO2的综合利用,对构建低碳环保社会有着重要意义,反应过程为:①CO2+Fe0.9O→Fe3O4+C,②3Fe3O4 10Fe0.9O+O2↑。下列说法
10Fe0.9O+O2↑。下列说法错误 的是
 10Fe0.9O+O2↑。下列说法
10Fe0.9O+O2↑。下列说法| A.该应用中Fe0.9O可循环利用 |
| B.①反应前后铁元素的化合价升高 |
| C.消耗44gCO2,理论上可生成16gO2 |
D.Fe0.9O中铁元素有+2、+3两种价态,则Fe0.9O可以表示为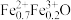 |
您最近半年使用:0次
8 . 天然气被称为 “清洁燃料”。生活中常用天然气作燃料,天然气中甲烷完全燃烧的化学方程式为______________ ;现有C3H6O和C2H4O2组成的混合物,经测定其中氧元素的质量分数为37%,则碳元素的质量分数为_______ 。
您最近半年使用:0次
解题方法
9 . 小组同学称取13.8gMgCO3•3H2O进行热重分析,并绘制出如图所示的热重曲线,下列说法正确的是
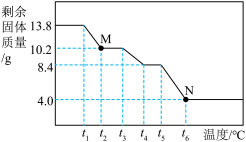
A.t1~t2℃时反应的化学方程式为:MgCO3•3H2O MgCO3+3H2O MgCO3+3H2O |
| B.t2℃时,固体物质的化学式为MgCO3•H2O |
| C.最终剩余的4.0g物质是MgCO3 |
| D.MgCO3•3H2O失去结晶水的过程属于物理变化 |
您最近半年使用:0次
2024·广东·模拟预测
10 . 非整比化合物如Fe0.9O、PbO1.9等,是新型的功能材料,具有很大的科技价值。利用Fe0.9O的某转换过程如图所示,下列说法不正确的是
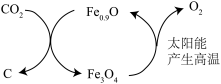
| A.该转换过程中Fe0.9O起催化作用 | B.Fe0.9O中+3价铁与+2价铁的原子个数比为7∶2 |
| C.Fe3O4的化学式可改写为FeO•Fe2O3 | D.该转换能转化利用CO2,助力碳中和 |
您最近半年使用:0次



