解题方法
1 . “二十四节气”是我国古代农耕文化的产物,农耕生产与节气息息相关。
(1)“立春”:万物复苏,春暖花开。乙酸苯甲酯(C9H10O2)是一种具有茉莉花香的物质,其中氢、氧元素的质量比是___________ (填最简整数比)。
(2)“清明”:清明有霜梅雨少。正常雨水略显酸性,原因是___________ (用方程式表示)。pH<5.6的雨水容易导致土壤酸化,常用___________ 改良酸性土壤。
(3)“谷雨”:谷雨麦挑旗,立夏麦头齐。为促进小麦生长,应追加肥料。
①下列肥料属于复合肥料的是___________ (填字母)。
A CO(NH2)2 B.Ca3(PO4)2 C.NH4NO3 D.KNO3
②草木灰是一种钾肥,主要成分是K2CO3,一般不与铵态氮肥混合使用。据此推测,K2CO3溶液中含有的阴离子是___________ (填离子符号)。
(4)“秋风”:一粒好种,万担好粮。农业上常用质量分数为16%的NaCl溶液来选种。现有100g质量分数为26%的NaCl溶液,加___________ g水即可配成质量分数为16%的NaCl溶液。
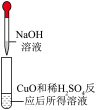
(5)“小雪”:小雪雪满天,来年必丰年。农作物的丰收离不开化肥的加持,常用的化肥“碳铵”受热易分解产生NH3.某小组同学根据NH3还原CuO的反应,设计测定Cu相对原子质量Ar(Cu)的实验。
【反思评价】
①从图中选择并组装一套合理、简单的装置,连接顺序为:制氨气发生装置→C→A___________ (填“B→C”或“C→B”);___________ (用含a、b的代数式表示)。
③在本实验中,使测定结果 Ar(Cu)偏大的是___________ (填字母)。
A.CuO未完全起反应 B.CuO中混有不反应的杂质 C.NH3通入A装置前未用C装置干燥
(1)“立春”:万物复苏,春暖花开。乙酸苯甲酯(C9H10O2)是一种具有茉莉花香的物质,其中氢、氧元素的质量比是
(2)“清明”:清明有霜梅雨少。正常雨水略显酸性,原因是
(3)“谷雨”:谷雨麦挑旗,立夏麦头齐。为促进小麦生长,应追加肥料。
①下列肥料属于复合肥料的是
A CO(NH2)2 B.Ca3(PO4)2 C.NH4NO3 D.KNO3
②草木灰是一种钾肥,主要成分是K2CO3,一般不与铵态氮肥混合使用。据此推测,K2CO3溶液中含有的阴离子是
(4)“秋风”:一粒好种,万担好粮。农业上常用质量分数为16%的NaCl溶液来选种。现有100g质量分数为26%的NaCl溶液,加
(5)“小雪”:小雪雪满天,来年必丰年。农作物的丰收离不开化肥的加持,常用的化肥“碳铵”受热易分解产生NH3.某小组同学根据NH3还原CuO的反应,设计测定Cu相对原子质量Ar(Cu)的实验。
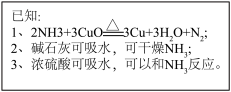
【反思评价】
①从图中选择并组装一套合理、简单的装置,连接顺序为:制氨气发生装置→C→A
③在本实验中,使测定结果 Ar(Cu)偏大的是
A.CuO未完全起反应 B.CuO中混有不反应的杂质 C.NH3通入A装置前未用C装置干燥
您最近一年使用:0次
解题方法
2 . 化学实验常有“出乎意料”的现象或结果,以下解释合理的是
| 实验 |
|
|
|
|
| 异常情况 | 产生氢气和氧气的体积比大于 | 测定结果偏大 | 开始时无蓝色沉淀出现 | 冷却后天平不平衡 |
| 选项 | A.氢气溶于水 | B.装置漏气 | C.稀硫酸过量 | D.红磷量不足 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-13更新
|
68次组卷
|
3卷引用:2024年陕西省汉中市初中学业水平考试化学全真模拟试卷(四)
解题方法
3 . 某学习小组用如图所示装置测定锌铜合金中锌、铜的质量分数。___________ ;
(2)实验操作步骤有:检查气密性,将药品和水装入各仪器中,连接好装置后,再进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥、称重;③待B中不再有气体产生恢复至室温,记录C的液面位置;④由A向B滴加足量试剂。
上述再进行的操作的顺序是___________ (填序号),记录C的液面位置时,除视线平视外,还应___________ ;
(3)B中发生反应的化学方程式为:___________ ;
(4)若实验用铜锌合金的质量为a g,与酸充分反应后,测得氢气体积为VL,为求出合金中锌、铜的质量分数,还缺少的一个数据是___________。
(5)若实验用锌铜合金的质量为a g,与酸充分反应后,B中剩余固体的质量为b g,则锌的质量分数为___________ ;
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得锌的质量分数将___________ (填“偏大”“偏小”或“不受影响”)。

(2)实验操作步骤有:检查气密性,将药品和水装入各仪器中,连接好装置后,再进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥、称重;③待B中不再有气体产生恢复至室温,记录C的液面位置;④由A向B滴加足量试剂。
上述再进行的操作的顺序是
(3)B中发生反应的化学方程式为:
(4)若实验用铜锌合金的质量为a g,与酸充分反应后,测得氢气体积为VL,为求出合金中锌、铜的质量分数,还缺少的一个数据是___________。
| A.反应前加入稀酸的体积 | B.反应前加入稀酸的质量分数 |
| C.实验前反应装置中空气的体积 | D.实验条件下氢气的密度 |
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得锌的质量分数将
您最近一年使用:0次
名校
4 . 实验是学习化学的重要手段,以下是初中阶段四个重要实验。_______ 。
(2)实验2,烧杯中盛放的物质是_______ (填“水”或“浓硫酸”)。
(3)实验3中发生的化学反应方程式为_______ 。
(4)实验4,配制100g溶质的质量分数为8.3%的碳酸钠溶液。称量碳酸钠固体质量时,发现托盘天平的指针偏向左盘应_______。
(5)经检测,实验4所配制溶液溶质的质量分数偏小,其原因可能是_______ (填序号)。
①称量时砝码端忘垫质量相同的纸片
②碳酸钠与砝码放反了(1g以下用游码)
③量取水时,俯视读数
④C操作中有固体洒出
⑤配好后装入试剂瓶中时有少量液体洒出

(2)实验2,烧杯中盛放的物质是
(3)实验3中发生的化学反应方程式为
(4)实验4,配制100g溶质的质量分数为8.3%的碳酸钠溶液。称量碳酸钠固体质量时,发现托盘天平的指针偏向左盘应_______。
| A.增加适量碳酸钠固体 | B.调节游码 |
| C.减少适量碳酸钠固体 | D.添加砝码 |
(5)经检测,实验4所配制溶液溶质的质量分数偏小,其原因可能是
①称量时砝码端忘垫质量相同的纸片
②碳酸钠与砝码放反了(1g以下用游码)
③量取水时,俯视读数
④C操作中有固体洒出
⑤配好后装入试剂瓶中时有少量液体洒出
您最近一年使用:0次
解题方法
5 . 某同学配制50 g6%的氯化钠溶液,整个操作过程如图所示,回答下列问题:

(1)经过计算,需称取氯化钠______ g
(2)配制溶液正确操作顺序为______ (填序号,下同),其中操作错误的是______ ;
(3)④中玻璃棒的作用是______ 。
(4)经检测,该同学配制的溶液溶质质量分数小,可能的原因是

(1)经过计算,需称取氯化钠
(2)配制溶液正确操作顺序为
(3)④中玻璃棒的作用是
(4)经检测,该同学配制的溶液溶质质量分数小,可能的原因是
| A.氯化钠固体不纯 |
| B.用生锈砝码称量 |
| C.装瓶时有少量溶液洒出 |
| D.溶解时烧杯内壁有水珠 |
您最近一年使用:0次
名校
解题方法
6 . 食盐(氯化钠)是生活必需品。提纯含少量泥沙的粗盐,经过以下操作流程:
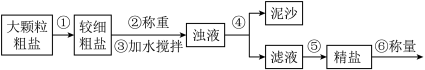
(1)整个流程中不需要用到的仪器是______(选填序号)。
(2)操作④中,所用玻璃仪器有_______ 、玻璃棒、烧杯。
(3)操作⑤中,当蒸发皿中出现较多固体时,应该_______(选填序号)。
(4)实验最后称量获得的精盐并计算精盐的产率(用所得精盐质量除以原粗盐质量),发现制得率较低,其可能原因是_______(选填序号)。

(1)整个流程中不需要用到的仪器是______(选填序号)。
| A.研钵 | B.量筒 | C.托盘天平 | D.药匙 |
(2)操作④中,所用玻璃仪器有
(3)操作⑤中,当蒸发皿中出现较多固体时,应该_______(选填序号)。
| A.移去酒精灯,停止搅拌 |
| B.移去酒精灯,用玻璃棒继续搅拌 |
| C.继续加热直至蒸干水分,再移去酒精灯 |
(4)实验最后称量获得的精盐并计算精盐的产率(用所得精盐质量除以原粗盐质量),发现制得率较低,其可能原因是_______(选填序号)。
| A.食盐没全溶解即过滤 | B.过滤时滤纸有破损 | C.蒸发时食盐飞溅剧烈 |
您最近一年使用:0次
解题方法
7 . 碳酸钠俗称纯碱或苏打,在生活,生产和实验研究中均有广泛应用。
【配制溶液】配制溶质质量分数分别为1%、2%和4%的Na2CO3溶液
(1)若配制50g溶质质量分数为4%的Na2CO3溶液,下列操作正确的是______________ (填字母)。
a.用托盘天平称取2gNa2CO3固体
b.选用50mL量筒量取所需体积的水
c.选用带玻璃塞的广口试剂瓶,将配好的溶液装瓶并贴标签
(2)分别测定25℃时,上述3种溶液的pH,记录数据如下:
分析①②③三组数据可得出的结论是______________ 。
【制备物质】用Na2CO3溶液和FeSO4溶液发生复分解反应制备FeCO3
【已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀】
(3)在烧杯中制备FeCO3沉淀时,应选用的加料方式是______________ (填字母)。
a.将FeSO4溶液与Na2CO3溶液同时加入到烧杯中
b.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的烧杯中
c.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的烧杯中
(4)潮湿的FeCO3固体置于空气中易变质,生成一种红褐色固体和能使澄清石灰水变浑浊的气体,写出该反应发化学方程式______________ 。
【标定浓度】标定待测盐酸的溶质质量分数
(5)将Na2CO3固体在270℃干燥至恒重,准确称取0.212g无水Na2CO3于锥形瓶中,加入50mL蒸馏水溶解,滴入待测盐酸,当两者恰好完全反应时,消耗盐酸的体积为20.00mL。
(该盐酸的密度近似等于1g.mL-1,反应中Na2CO3所含的碳元素全部转化为CO2)。
①列式计算待测盐酸的溶质质量分数(结果用百分数表示,保留两位小数)。________
②若上述测定过程中Na2CO3固体未经充分干燥,则测出盐酸的溶质质量分数将_________ (填“偏大”“偏小”或“无影响”)。
【配制溶液】配制溶质质量分数分别为1%、2%和4%的Na2CO3溶液
(1)若配制50g溶质质量分数为4%的Na2CO3溶液,下列操作正确的是
a.用托盘天平称取2gNa2CO3固体
b.选用50mL量筒量取所需体积的水
c.选用带玻璃塞的广口试剂瓶,将配好的溶液装瓶并贴标签
(2)分别测定25℃时,上述3种溶液的pH,记录数据如下:
| 实验编号 | ① | ② | ③ |
| 溶质质量分数 | 1% | 2% | 4% |
| 溶液pH值 | 11.62 | 11.76 | 11.90 |
【制备物质】用Na2CO3溶液和FeSO4溶液发生复分解反应制备FeCO3
【已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀】
(3)在烧杯中制备FeCO3沉淀时,应选用的加料方式是
a.将FeSO4溶液与Na2CO3溶液同时加入到烧杯中
b.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的烧杯中
c.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的烧杯中
(4)潮湿的FeCO3固体置于空气中易变质,生成一种红褐色固体和能使澄清石灰水变浑浊的气体,写出该反应发化学方程式
【标定浓度】标定待测盐酸的溶质质量分数
(5)将Na2CO3固体在270℃干燥至恒重,准确称取0.212g无水Na2CO3于锥形瓶中,加入50mL蒸馏水溶解,滴入待测盐酸,当两者恰好完全反应时,消耗盐酸的体积为20.00mL。
(该盐酸的密度近似等于1g.mL-1,反应中Na2CO3所含的碳元素全部转化为CO2)。
①列式计算待测盐酸的溶质质量分数(结果用百分数表示,保留两位小数)。
②若上述测定过程中Na2CO3固体未经充分干燥,则测出盐酸的溶质质量分数将
您最近一年使用:0次
解题方法
8 . 我国不少地方有端午吃“灰水粽”的习俗,所谓“灰水粽”是指用草木灰的浸出液(俗称“灰水”)浸泡糯米做成的粽子。已知草木灰中富含钾盐,主要成分是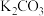 ,还有少量
,还有少量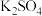 和
和 。
。
请回答:
(1)①碳酸钾中碳、氧元素的质量比_____________ (最简整数比)。
② 碳酸钾中钾元素质量为
碳酸钾中钾元素质量为_________________ 。
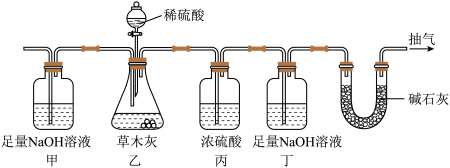
(2)为测定草木灰中碳酸钾的含量,现称取样品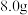 ,加入足量水溶解(其他杂质不溶于水)。向乙中加入足量的稀硫酸,反应结束后装置丁增重
,加入足量水溶解(其他杂质不溶于水)。向乙中加入足量的稀硫酸,反应结束后装置丁增重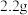 。写出装置乙中发生的化学方程式:
。写出装置乙中发生的化学方程式:______________ ,草木灰中碳酸钾的质量分数为_____________ (计算结果精确到 )。
)。
(3)若撤出装置甲,直接通入空气会导致实验结果_____________ (填“偏大”、“偏小”或“不变”)。
(4)为了检验草木灰的浸出液中存在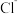 ,先往浸出液中加入足量的
,先往浸出液中加入足量的 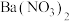 溶液后过滤,这样操作的目的是
溶液后过滤,这样操作的目的是_____________________ 。
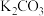 ,还有少量
,还有少量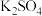 和
和 。
。请回答:

(1)①碳酸钾中碳、氧元素的质量比
②
 碳酸钾中钾元素质量为
碳酸钾中钾元素质量为(2)为测定草木灰中碳酸钾的含量,现称取样品
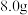 ,加入足量水溶解(其他杂质不溶于水)。向乙中加入足量的稀硫酸,反应结束后装置丁增重
,加入足量水溶解(其他杂质不溶于水)。向乙中加入足量的稀硫酸,反应结束后装置丁增重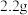 。写出装置乙中发生的化学方程式:
。写出装置乙中发生的化学方程式: )。
)。(3)若撤出装置甲,直接通入空气会导致实验结果
(4)为了检验草木灰的浸出液中存在
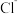 ,先往浸出液中加入足量的
,先往浸出液中加入足量的 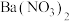 溶液后过滤,这样操作的目的是
溶液后过滤,这样操作的目的是
您最近一年使用:0次
解题方法
9 . 某同学为检验长时间露置在空气中的氢氧化钠变质程度并测定碳酸钠的质量分数,称取样品后加入如图装置,滴入足量稀盐酸至完全反应。以下分析正确的是
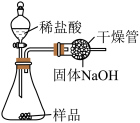
| A.加入足量稀盐酸后样品表面有气泡生成,说明样品完全变质 |
B.干燥管中固体 只吸收反应生成的二氧化碳 只吸收反应生成的二氧化碳 |
C.反应后向锥形瓶中滴入 溶液可验证样品中含有 溶液可验证样品中含有 |
| D.根据干燥管反应前后的质量差进行计算的结果一定比实际偏大 |
您最近一年使用:0次
2024-03-31更新
|
62次组卷
|
3卷引用:2024年陕西省宝鸡市凤翔区中考第一次质量检测化学试卷
解题方法
10 . 某品牌牙膏生产企业,购进一批牙膏摩擦剂(CaCO3和SiO2的混合物)。为了测定这种摩擦剂中CaCO3的质量分数,化学兴趣小组的同学取20g该牙膏摩擦剂和足量的稀盐酸,设计如图装置进行测定实验,记录数据如下表:
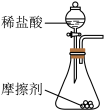
(1)计算该牙膏摩擦剂中碳酸钙的质量分数。(写出计算过程)
(2)此实验方案的设计导致计算结果偏小的原因是______ 。

| 反应前装置和药品总质量 | 充分反应后装置和药品总质量 |
| 370g | 363.4g |
(1)计算该牙膏摩擦剂中碳酸钙的质量分数。(写出计算过程)
(2)此实验方案的设计导致计算结果偏小的原因是
您最近一年使用:0次