解题方法
1 . “沉睡三千年,一醒惊天下”,三星堆大批珍贵文物的出土令世人叹为观止。_____ 材料(选填“合成”或“金属”)。铜锡合金的熔点和硬度随锡含量的变化如图3所示,图中表示熔点的曲线是_____ (选填“a”或“b”)。
(2)“青铜面具”布满锈斑,“黄金面具”仍金光闪闪,从物质性质角度分析原因是_____ 。青铜生锈产生铜绿【Cu2(OH)2CO3】可能与环境中的氧气、水和_____ 有关。
(3)古代劳动人民以孔雀石【主要成分为Cu2(OH)2CO3】为原料冶炼铜。化学探究小组称取25g孔雀石样品与足量的稀硫酸充分反应,产生了4.4g气体,发生反应的化学方程式为Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑(该孔雀石的其他成分不与酸反应)。请计算该孔雀石中Cu2(OH)2CO3的质量分数(写出计算过程)。

(2)“青铜面具”布满锈斑,“黄金面具”仍金光闪闪,从物质性质角度分析原因是
(3)古代劳动人民以孔雀石【主要成分为Cu2(OH)2CO3】为原料冶炼铜。化学探究小组称取25g孔雀石样品与足量的稀硫酸充分反应,产生了4.4g气体,发生反应的化学方程式为Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑(该孔雀石的其他成分不与酸反应)。请计算该孔雀石中Cu2(OH)2CO3的质量分数(写出计算过程)。
您最近一年使用:0次
名校
解题方法
2 . 2024年一季度,我国新能源汽车销售209万辆,同比增长31.8%,整车出口30.7万辆,同比增长23.8%,国产新能源汽车发展进入快车道。
(1)某品牌新能源汽车所用电池使用LFP(化学式:LiFePO4)作为正极材料,下列说法正确的是___________ 。
a.LFP属于有机化合物
b.LFP中锂元素为+1价,则铁元素为+2价
c.LFP中铁元素的质量分数最大
d.LFP由锂、铁、磷、氧四个元素组成
(2)新能源汽车为实现“轻量化”,部分外壳采用铝合金,请问不用纯铝的主要原因是什么?
(3)汽车制造离不开炼钢,用生铁炼钢在我国已有2500多年的历史。生铁和钢的最主要区别是什么?
(4)在实验室里,用下图装置进行模拟炼铁实验并检验气体产物(已知CO发生装置制得的CO气体中混有少量CO2和H2O)。___________ 。
②检验装置C中气体产物的实验现象为___________ 。
③装置A处发生反应的化学方程式为___________ ;实验结束后装置A溶液中氢氧化钠是否有剩余?请设计实验检验并简要写出实验步骤、现象和结论___________ 。
(5)某钢铁厂要冶炼含铁560t的生铁,请依据化学方程式计算,理论上需要含氧化铁80%的赤铁矿的质量是多少?
(1)某品牌新能源汽车所用电池使用LFP(化学式:LiFePO4)作为正极材料,下列说法正确的是
a.LFP属于有机化合物
b.LFP中锂元素为+1价,则铁元素为+2价
c.LFP中铁元素的质量分数最大
d.LFP由锂、铁、磷、氧四个元素组成
(2)新能源汽车为实现“轻量化”,部分外壳采用铝合金,请问不用纯铝的主要原因是什么?
(3)汽车制造离不开炼钢,用生铁炼钢在我国已有2500多年的历史。生铁和钢的最主要区别是什么?
(4)在实验室里,用下图装置进行模拟炼铁实验并检验气体产物(已知CO发生装置制得的CO气体中混有少量CO2和H2O)。
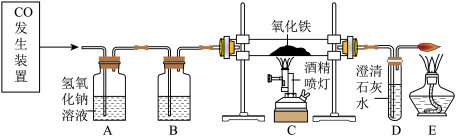
②检验装置C中气体产物的实验现象为
③装置A处发生反应的化学方程式为
(5)某钢铁厂要冶炼含铁560t的生铁,请依据化学方程式计算,理论上需要含氧化铁80%的赤铁矿的质量是多少?
您最近一年使用:0次
名校
解题方法
3 . 含氯消毒剂能杀灭病毒,常见的含氯消毒剂有漂白粉、“84”消毒液等。其中“84”消毒液的有效成分是次氯酸钠(NaClO),工业上制取“84”消毒液的化学方程式为: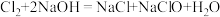 。
。
(1)关于制取“84”消毒液原料中的NaOH和另一副产品NaCl,下列说法正确的是_________ 。
a.NaCl配制成的生理盐水是混合物 b.氯化钠可用于消除积雪,做调味品
c.NaOH俗称烧碱、纯碱 d.氢氧化钠溶液可使紫色石蕊溶液变红
(2)次氯酸钠(NaClO)中,氯元素的化合价为________ 。
(3)生活中使用的“84”消毒液,次氯酸钠的浓度0.1%为最佳。小凡同学现在需要配制5000g浓度为0.1%的次氯酸钠溶液,需要10%的次氯酸钠溶液的质量为________ 。配制溶液时,需要用到的玻璃仪器有烧杯、量筒、________ 。
(4)配好溶液后,小凡在转移至细口瓶时,不慎洒出溶液,此时溶液的浓度________ (选填“变大”“变小”或“无影响”)
(5)将14.2g氯气通入足量的氢氧化钠溶液中(不考虑其他反应),根据化学方程式,计算出生成的次氯酸钠的质量。
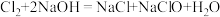 。
。(1)关于制取“84”消毒液原料中的NaOH和另一副产品NaCl,下列说法正确的是
a.NaCl配制成的生理盐水是混合物 b.氯化钠可用于消除积雪,做调味品
c.NaOH俗称烧碱、纯碱 d.氢氧化钠溶液可使紫色石蕊溶液变红
(2)次氯酸钠(NaClO)中,氯元素的化合价为
(3)生活中使用的“84”消毒液,次氯酸钠的浓度0.1%为最佳。小凡同学现在需要配制5000g浓度为0.1%的次氯酸钠溶液,需要10%的次氯酸钠溶液的质量为
(4)配好溶液后,小凡在转移至细口瓶时,不慎洒出溶液,此时溶液的浓度
(5)将14.2g氯气通入足量的氢氧化钠溶液中(不考虑其他反应),根据化学方程式,计算出生成的次氯酸钠的质量。
您最近一年使用:0次
2024·广东广州·模拟预测
解题方法
4 . 材料是人类赖以生存和发展的重要物质,目前铜依然是使用较多的金属材料。
(一)铜材料的有关知识
(1)①人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是______ 。
②纯铜又称紫铜,常见铜合金有黄铜、青铜等种类。家用电缆常用紫铜,以聚氯乙烯塑料或TPU橡胶包裹。
(2)以上叙述中不涉及到的材料是______(选填序号)。
(二)铜及其化合物的实验
(3)①将CuO粉溶于稀H2SO4,反应的化学方程式是______ 。
②向上述反应后的溶液中滴加NaOH溶液,生成浅绿色沉淀。
【查阅资料】
①NaOH与CuSO4反应会生成碱式硫酸铜【Cu4(OH)6SO4】,其不溶于水,呈浅绿色,能与酸反应:
②Cu(OH)2分解温度为80℃,Cu4(OH)6SO4分解温度为300℃。
(4)写出生成浅绿色沉淀反应的化学方程式______ 。
(5)将浅绿色固体加热至100℃,发现固体变______ 色,说明浅绿色固体中还含有Cu(OH)2。
(6)过滤、洗涤、低温干燥得到浅绿色固体,能证明固体已洗净的方法为______ 。
(三)浅绿色固体的热分解实验
兴趣小组称取此固体3.25g,在科研人员的指导下用如图装置进行热分解实验。
②浓硫酸不能吸收SO2,能吸收SO3。
(7)加热前后及过程中均通入N2,停止加热后继续通N2的目的是______ 。
(8)控制温度在不同的范围对A中样品加热。测得剩余固体质量随温度的变化如图所示。当加热到超过300℃时,装置C中的现象是______ 。______ 。
(10)浅绿色固体从室温开始加热至图中E点时装置B增重______ g。
(11)兴趣小组在E点时将N2换成CO继续通入到A中反应,一段时间后固体全变红且质量变为2g,此时用装有碱石灰的干燥管在E后面吸收CO2,理论上测得CO2的质量为______ 。
(一)铜材料的有关知识
(1)①人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是
②纯铜又称紫铜,常见铜合金有黄铜、青铜等种类。家用电缆常用紫铜,以聚氯乙烯塑料或TPU橡胶包裹。
(2)以上叙述中不涉及到的材料是______(选填序号)。
| A.金属材料 | B.无机非金属材料 | C.合成材料 |
(二)铜及其化合物的实验
(3)①将CuO粉溶于稀H2SO4,反应的化学方程式是
②向上述反应后的溶液中滴加NaOH溶液,生成浅绿色沉淀。
【查阅资料】
①NaOH与CuSO4反应会生成碱式硫酸铜【Cu4(OH)6SO4】,其不溶于水,呈浅绿色,能与酸反应:
②Cu(OH)2分解温度为80℃,Cu4(OH)6SO4分解温度为300℃。
(4)写出生成浅绿色沉淀反应的化学方程式
(5)将浅绿色固体加热至100℃,发现固体变
(6)过滤、洗涤、低温干燥得到浅绿色固体,能证明固体已洗净的方法为
(三)浅绿色固体的热分解实验
兴趣小组称取此固体3.25g,在科研人员的指导下用如图装置进行热分解实验。
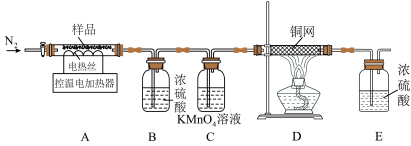
②浓硫酸不能吸收SO2,能吸收SO3。
(7)加热前后及过程中均通入N2,停止加热后继续通N2的目的是
(8)控制温度在不同的范围对A中样品加热。测得剩余固体质量随温度的变化如图所示。当加热到超过300℃时,装置C中的现象是
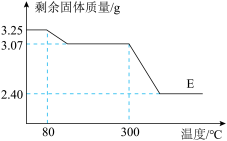
(10)浅绿色固体从室温开始加热至图中E点时装置B增重
(11)兴趣小组在E点时将N2换成CO继续通入到A中反应,一段时间后固体全变红且质量变为2g,此时用装有碱石灰的干燥管在E后面吸收CO2,理论上测得CO2的质量为
您最近一年使用:0次
5 . 黑龙江被誉为“国家大粮仓”粮食安全是“国之大者”。
(1)守住良田沃士,保障粮食安全。
①大豆富含蛋白质,磨成豆浆后加入盐卤(含MgCl2)能制成豆腐。下列说法正确的是_______ 。
A豆腐和年糕主要营养成分相同
B.氯化镁能使蛋白质失去生理活性
C.豆腐可在人体内转化为葡萄糖
D.豆腐烧焦后会产生烧焦羽毛气味
②常见农作物最适宜生长的土壤pH范围如下:
某农田改良后pH为6.8,该农田适合种植的农作物是_______ 。(填字母)
A.茶树 B.油菜 C.水稻 D.萝卜
(2)科技创新,开辟产粮新路径。
我国科学家利用CO2合成葡萄糖,该方案先通过电催化结合生物合成的方式,将CO2高效还原成醋酸,再利用微生物发酵获得葡萄糖,为人工和半人工合成“粮食”提供了新技术。_______ (用离子符号表示)。
②通电条件下,装置1中CO2分解成CO和常见气体单质X,X的化学式为_______ 。
③写出装置2中一氧化碳转化成醋酸的化学反应方程式_______ 。
④试计算理论上恰好合成葡萄糖所需CO2与H2O的质量比为_______ (填最简单整数比)。
(1)守住良田沃士,保障粮食安全。
①大豆富含蛋白质,磨成豆浆后加入盐卤(含MgCl2)能制成豆腐。下列说法正确的是
A豆腐和年糕主要营养成分相同
B.氯化镁能使蛋白质失去生理活性
C.豆腐可在人体内转化为葡萄糖
D.豆腐烧焦后会产生烧焦羽毛气味
②常见农作物最适宜生长的土壤pH范围如下:
| 农作物 | 茶树 | 油菜 | 水稻 | 萝卜 |
| pH | 5.0~5.5 | 5.8~6.7 | 6.0~7.0 | 7.0~7.5 |
A.茶树 B.油菜 C.水稻 D.萝卜
(2)科技创新,开辟产粮新路径。
我国科学家利用CO2合成葡萄糖,该方案先通过电催化结合生物合成的方式,将CO2高效还原成醋酸,再利用微生物发酵获得葡萄糖,为人工和半人工合成“粮食”提供了新技术。
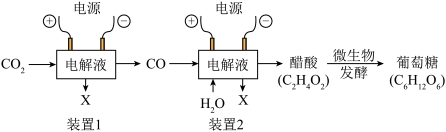
②通电条件下,装置1中CO2分解成CO和常见气体单质X,X的化学式为
③写出装置2中一氧化碳转化成醋酸的化学反应方程式
④试计算理论上恰好合成葡萄糖所需CO2与H2O的质量比为
您最近一年使用:0次
解题方法
6 . 《石灰吟》是明代政治家、文学家于谦创作的一首七言绝句。全诗内容为“千锤万凿出深山,烈火焚烧若等闲。粉骨碎身浑不怕,要留清白在人间”。诗中涉及的化学反应可用图1表示。_______ 反应(填基本反应类型)。
(2)过程Ⅱ发生的反应是_______ (填“放热”或“吸热”)反应。
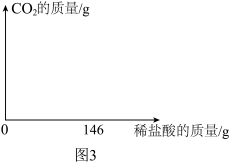
(3)化学兴趣小组的同学欲对石灰石样品进行探究。在烧杯中加入石灰石样品25g(其中CaCO3质量分数为80%),然后逐滴加入稀盐酸,烧杯中石灰石样品的质量与滴入稀盐酸的质量关系曲线如图2所示(假设石灰石中的杂质既不反应,也不溶于水)。
①当加入稀盐酸146g时(即图中B点),求此时生成二氧化碳的质量_______ 。(根据化学方程式计算,并写出计算过程)
②分析表数据,请在3图中画出加入0~146g稀盐酸过程中,产生二氧化碳质量对应的变化曲线图,并标注必要的数值_______ 。

(2)过程Ⅱ发生的反应是
(3)化学兴趣小组的同学欲对石灰石样品进行探究。在烧杯中加入石灰石样品25g(其中CaCO3质量分数为80%),然后逐滴加入稀盐酸,烧杯中石灰石样品的质量与滴入稀盐酸的质量关系曲线如图2所示(假设石灰石中的杂质既不反应,也不溶于水)。
①当加入稀盐酸146g时(即图中B点),求此时生成二氧化碳的质量
②分析表数据,请在3图中画出加入0~146g稀盐酸过程中,产生二氧化碳质量对应的变化曲线图,并标注必要的数值
您最近一年使用:0次
2024九年级下·广东·专题练习
7 . I.如图是实验室制取常见气体的相关装置:
(1)仪器X的名称是___________ 。
(2)装置C中明显的一处错误是___________ 。
(3)用D装置收集氧气,判断集气瓶已收集满气体所依据的实验现象是___________ 。
(4)若用A、E、F装置制取并收集干燥的二氧化碳,管口正确的连接顺序是___________ (填管口序号)。
II.某兴趣小组设计了一个创新实验,如图所示。___________ 。该装置中CO2换成HCl气体,也会出现同样实验现象。
(6)该创新实验装置的目的是___________ 。
(7)该装置___________ (填“能”“不能”)证明二氧化碳与水反应,原因是___________ 。
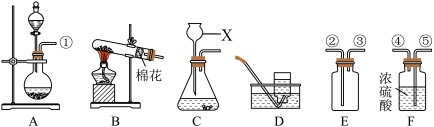
(1)仪器X的名称是
(2)装置C中明显的一处错误是
(3)用D装置收集氧气,判断集气瓶已收集满气体所依据的实验现象是
(4)若用A、E、F装置制取并收集干燥的二氧化碳,管口正确的连接顺序是
II.某兴趣小组设计了一个创新实验,如图所示。
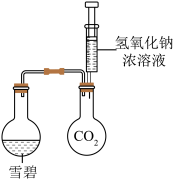
(6)该创新实验装置的目的是
(7)该装置
您最近一年使用:0次
2024九年级下·广东·专题练习
8 . 化学是一门以实验为基础的学科。请回答下列问题。
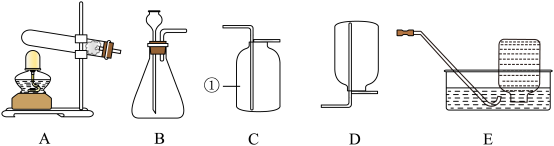
I.下列装置常用于实验室制取气体,___________ 。
(2)实验室常用大理石和稀盐酸在常温下反应制取二氧化碳气体,应选择的发生装置是___________ (填字母代号)。
(3)由于在相同条件下二氧化碳的密度比空气___________ ,所以可以选择C装置收集二氧化碳气体。
(4)检验二氧化碳的方法:将气体通入澄清的石灰水中,若___________ ,则为二氧化碳。
II.项目式学习小组用紫茄子皮在实验室制作酸碱指示剂。相关步骤如下。回答下列小题。
(5)利用上述步骤制作指示剂,正确顺序是___________ (填序号)。
(6)常温下,三种试剂分别滴加上述指示剂后的显色情况如下表。
i.如果紫茄子皮指示剂遇到某溶液显红色,则该溶液的pH___________ 7(填“>”“<”“=”)。
ii.该指示剂___________ (填“能”“不能”)鉴别石灰水和纯碱溶液,理由是___________ 。
iii.紫茄子皮指示剂遇到pH=7的液体显___________ 色。
iv.鉴别稀盐酸和石灰水的实验方案是___________ 。
I.下列装置常用于实验室制取气体,
(2)实验室常用大理石和稀盐酸在常温下反应制取二氧化碳气体,应选择的发生装置是
(3)由于在相同条件下二氧化碳的密度比空气
(4)检验二氧化碳的方法:将气体通入澄清的石灰水中,若
II.项目式学习小组用紫茄子皮在实验室制作酸碱指示剂。相关步骤如下。回答下列小题。
|
|
|
| ①用酒精浸泡 | ②捣烂 | ③过滤 |
(6)常温下,三种试剂分别滴加上述指示剂后的显色情况如下表。
| 试剂 | 稀盐酸 | 石灰水 | 蒸馏水 |
| 滴加紫茄子皮指示剂后的颜色 | 红色 | 绿色 | 紫色 |
ii.该指示剂
iii.紫茄子皮指示剂遇到pH=7的液体显
iv.鉴别稀盐酸和石灰水的实验方案是
您最近一年使用:0次
解题方法
9 . CO2是一种常见物质,在生活和生产中应用广泛。小圳同学学习了CO2的相关内容后,进行了多个和CO2相关的实践活动。
(1)利用下列微型装置完成CO2制取及检验实验
该实验中用到的石灰石样品中碳酸钙的质量分数为50%,请根据化学方程式:计算2g石灰石样品理论上产生CO2的质量(写出详细的计算过程)。
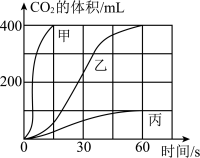
取等质量的同种石灰石加入足量酸(杂质不与酸反应),产生CO2的体积随时间变化曲线如图所示。
①如表中实验Ⅰ对应如图曲线_______ (选填“甲”“乙”或“丙”)。
②依据曲线图,小圳同学决定用实验Ⅱ的药品,而不用实验Ⅲ的药品制备二氧化碳的原因是_______ 。
(3)学习CO2的释放和捕捉工艺
(1)利用下列微型装置完成CO2制取及检验实验
该实验中用到的石灰石样品中碳酸钙的质量分数为50%,请根据化学方程式:计算2g石灰石样品理论上产生CO2的质量(写出详细的计算过程)。

取等质量的同种石灰石加入足量酸(杂质不与酸反应),产生CO2的体积随时间变化曲线如图所示。
| 实验编号 | 药品 |
| Ⅰ | 块状石灰石、7%稀硫酸 |
| Ⅱ | 块状石灰石、7%稀盐酸 |
| Ⅲ | 粉状石灰石、7%稀盐酸 |
②依据曲线图,小圳同学决定用实验Ⅱ的药品,而不用实验Ⅲ的药品制备二氧化碳的原因是
(3)学习CO2的释放和捕捉工艺
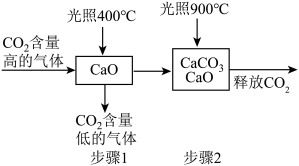
| A.原料易得且可循环使用 | B.充分利用太阳能 | C.可全地域全天候使用 |
您最近一年使用:0次
2024九年级下·广东·专题练习
解题方法
10 . I.根据下列装置图回答问题是(所用装置图用序号表示)___________ ,___________ 。
(2)实验室用大理石和稀盐酸反应制取二氧化碳,化学方程式为___________ 。应选用的气体发生装置和收集装置为___________ 。
(3)若用A装置来进行加热高锰酸钾制取氧气实验,应该在A装置中作适当的变化是___________ 。若用A装置来进行木炭粉还原氧化铜的实验,应该在A装置中作适当的变化是___________ 。
II.盐湖提钾后产生的天然结晶水氯镁石中含有较多量的MgCl2,少量的KCl、NaCl及泥沙。图1为从天然结晶水氯镁石提纯结晶水氯镁石(MgCl2·6H2O)的某工艺流程。
(4)选用无水乙醇而不选用水进行溶解的原因是___________ 。
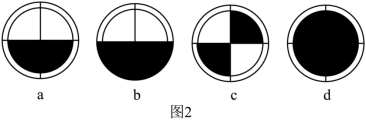
(5)操作完毕后展开滤纸,若黑色代表滤渣,则看到的情况最接近图中___________ (填字母)。
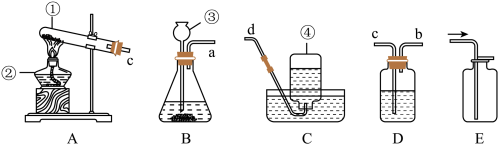
(2)实验室用大理石和稀盐酸反应制取二氧化碳,化学方程式为
(3)若用A装置来进行加热高锰酸钾制取氧气实验,应该在A装置中作适当的变化是
II.盐湖提钾后产生的天然结晶水氯镁石中含有较多量的MgCl2,少量的KCl、NaCl及泥沙。图1为从天然结晶水氯镁石提纯结晶水氯镁石(MgCl2·6H2O)的某工艺流程。
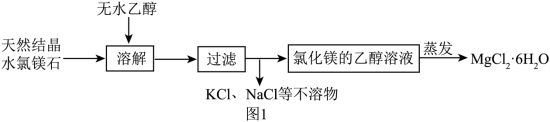
(4)选用无水乙醇而不选用水进行溶解的原因是
(5)操作完毕后展开滤纸,若黑色代表滤渣,则看到的情况最接近图中
您最近一年使用:0次