1 . 化学实验是科学探究的重要途径。试结合以下装置回答:______ 。
(2)若实验室用高锰酸钾制氧气,应在装置A的试管口______ 。
(3)用注射器可检查装置B的气密性,将活塞缓慢向外拉、若观察到______ 则证明气密性良好。
(4)若选用双氧水和二氧化锰制取氧气,其化学反应方程式是______ ,可以选择装置F收集氧气,气体从______ (选填“b”或“d”)端进入。
(5)在实验室里常用稀盐酸和大理石反应,用B或C装置制取CO2,其中采用C的优点是______ 。
(6)将产生的CO2依次通入如图所示的装置中,可观察到G中紫色石蕊溶液变红,是因为______ ,H中气球______ ,说明CO2密度比空气大。

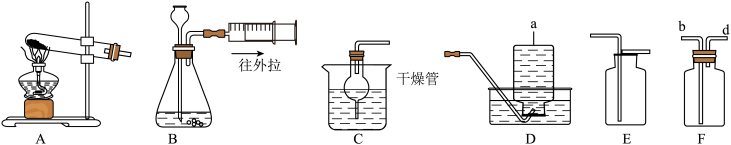
(2)若实验室用高锰酸钾制氧气,应在装置A的试管口
(3)用注射器可检查装置B的气密性,将活塞缓慢向外拉、若观察到
(4)若选用双氧水和二氧化锰制取氧气,其化学反应方程式是
(5)在实验室里常用稀盐酸和大理石反应,用B或C装置制取CO2,其中采用C的优点是
(6)将产生的CO2依次通入如图所示的装置中,可观察到G中紫色石蕊溶液变红,是因为

您最近一年使用:0次
解题方法
2 . 超细氮化铝(AlN)粉末被广泛应用于大规模集成电路生产领域。制取原理为: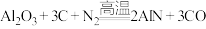 。
。
(1)氮化铝中元素质量比为______ 。
(2)现欲用以上方法来制备16.4t氮化铝,需要参加反应的氧化铝质量是多少?(写出计算过程)
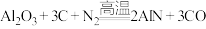 。
。(1)氮化铝中元素质量比为
(2)现欲用以上方法来制备16.4t氮化铝,需要参加反应的氧化铝质量是多少?(写出计算过程)
您最近一年使用:0次
解题方法
3 . 氟化钠是某些牙膏的添加剂。结合下列钠、氟元素的相关信息,判断下列说法中正确的是

| A.钠原子的中子数为11 |
| B.氟元素的相对原子质量为19.0g |
C.钠元素与氟元素形成化合物的化学式是 |
| D.在元素周期表中,钠元素和氟元素位于同一周期 |
您最近一年使用:0次
4 . 中国航天技术在人类探索浩渺宇宙的前沿不断创新、突破。
(1)“嫦娥五号”取回的月岩主要成分是钛酸亚铁(化学式为 ),在钛酸亚铁中钛元素(Ti)的化合价为
),在钛酸亚铁中钛元素(Ti)的化合价为______ ,钛酸亚铁中亚铁离子的化学符号是______ 。
(2)2024年4月30日17时46分,神舟十七号载人飞船返回舱在东风着陆场成功着陆。5月3日17日时27分,“嫦娥六号”成功发射。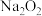 )吸收二氧化碳,生成碳酸钠和氧气。然后净化后的空气再重新流回舱内。此处理方式的优点是
)吸收二氧化碳,生成碳酸钠和氧气。然后净化后的空气再重新流回舱内。此处理方式的优点是______ (写一点,合理即可)。
②飞船返回舱返回时的动力来自液氢和液氧,它们提供动力时,发生反应的化学方程式为______ 。反应的基本类型为______ ,即将着陆前,要迅速释放剩余的燃料,这样做的目的是______ 。
(3)“嫦娥六号”使用了大量复合材料。下列关于复合材料的说法中正确的是______(选填字母)。
(1)“嫦娥五号”取回的月岩主要成分是钛酸亚铁(化学式为
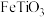 ),在钛酸亚铁中钛元素(Ti)的化合价为
),在钛酸亚铁中钛元素(Ti)的化合价为(2)2024年4月30日17时46分,神舟十七号载人飞船返回舱在东风着陆场成功着陆。5月3日17日时27分,“嫦娥六号”成功发射。


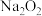 )吸收二氧化碳,生成碳酸钠和氧气。然后净化后的空气再重新流回舱内。此处理方式的优点是
)吸收二氧化碳,生成碳酸钠和氧气。然后净化后的空气再重新流回舱内。此处理方式的优点是②飞船返回舱返回时的动力来自液氢和液氧,它们提供动力时,发生反应的化学方程式为
(3)“嫦娥六号”使用了大量复合材料。下列关于复合材料的说法中正确的是______(选填字母)。
| A.不锈钢是常见的复合材料 |
| B.复合材料属于混合物 |
| C.有机高分子合成材料是复合材料 |
| D.玻璃钢是复合材料 |
您最近一年使用:0次
5 . 下列实验操作中正确的是
A.熄灭酒精灯 | B.加热液体 |
C.蒸发NaCl溶液 | D.处理废弃溶液 |
您最近一年使用:0次
6 . 下列实验操作中不能达到实验目的的是
| 选项 | 实验目的 | 主要实验操作 |
| A | 除去 溶液中混有的少量 溶液中混有的少量 | 加入适量的 溶液,过滤 溶液,过滤 |
| B | 鉴别蔗糖和 固体 固体 | 加水溶解 |
| C | 分离粗盐中混有的泥沙 | 溶解、过滤、蒸发 |
| D | 检验碳酸钠溶液中是否含有氯化钠 | 加过量的稀盐酸后,再滴加硝酸银溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 构建思维导图是一种重要的学习方法。请根据下列酸和碱的化学性质思维导图,回答下列问题:(“—”表示相连的两类物质之间可以发生化学反应)。______ 。
(2) 是一种复合肥料,按物质分类一股的方法,下列物质的类别与它最相似的是______。
是一种复合肥料,按物质分类一股的方法,下列物质的类别与它最相似的是______。
(3)酸和碱能与指示剂反应,而使指示剂显示不同的颜色。如NaOH溶液能使无色酚酞变成______ 。 、
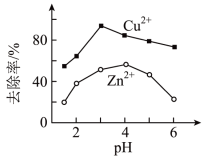
、 可用铁炭混合物(铁粉和活性炭的混合物)除去。其他条件不变,废水pH对
可用铁炭混合物(铁粉和活性炭的混合物)除去。其他条件不变,废水pH对 、
、 去除率的影响如上图所示。
去除率的影响如上图所示。
①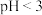 时,铁炭混合物表面有大量气泡产生,产生该现象的化学方程式为
时,铁炭混合物表面有大量气泡产生,产生该现象的化学方程式为______ 。
②相同pH条件下, 的去除率远高于
的去除率远高于 的原因可能是
的原因可能是______ 。
(5)酸碱盐的水溶液都具有导电性,原因酸、碱、盐溶于水在水分子的作用下都能解离出自由移动的离子。电导率是衡量溶液导电能力大小的物理量。在相同条件下,电导水与离子浓度(单位体积内的离子个数)成正比。如图所示是利用数字传感技术测定氢氧化钠溶液与稀硫酸反应过程中的电导率变化。______ 。
②P点和N点的电导率相同,对应溶液中的离子是否相同?______ (选填“相同”或“不相同”)。

(2)
 是一种复合肥料,按物质分类一股的方法,下列物质的类别与它最相似的是______。
是一种复合肥料,按物质分类一股的方法,下列物质的类别与它最相似的是______。A. | B. | C. | D.KOH |
(3)酸和碱能与指示剂反应,而使指示剂显示不同的颜色。如NaOH溶液能使无色酚酞变成
 、
、 可用铁炭混合物(铁粉和活性炭的混合物)除去。其他条件不变,废水pH对
可用铁炭混合物(铁粉和活性炭的混合物)除去。其他条件不变,废水pH对 、
、 去除率的影响如上图所示。
去除率的影响如上图所示。①
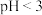 时,铁炭混合物表面有大量气泡产生,产生该现象的化学方程式为
时,铁炭混合物表面有大量气泡产生,产生该现象的化学方程式为②相同pH条件下,
 的去除率远高于
的去除率远高于 的原因可能是
的原因可能是(5)酸碱盐的水溶液都具有导电性,原因酸、碱、盐溶于水在水分子的作用下都能解离出自由移动的离子。电导率是衡量溶液导电能力大小的物理量。在相同条件下,电导水与离子浓度(单位体积内的离子个数)成正比。如图所示是利用数字传感技术测定氢氧化钠溶液与稀硫酸反应过程中的电导率变化。

②P点和N点的电导率相同,对应溶液中的离子是否相同?
您最近一年使用:0次
解题方法
8 . 碱式碳酸铜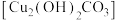 俗称铜绿,是一种蓝绿色固体,难溶于水,应用广泛。化学兴趣小组以“碱式碳酸铜的组成、结构、性质、应用和制备”为主题,开展项目式学习。
俗称铜绿,是一种蓝绿色固体,难溶于水,应用广泛。化学兴趣小组以“碱式碳酸铜的组成、结构、性质、应用和制备”为主题,开展项目式学习。
【任务一】认识铜绿的组成与结构
(1)铜绿的结构如图1所示,其中“ ”表示铜离子,“
”表示铜离子,“ ”表示碳酸根离子,则“
”表示碳酸根离子,则“ ”表示
”表示______ (填微粒名称)。
(2)探究铜绿的性质与转化
①铜绿呈蓝绿色,易被发现和识别,这利用的是铜绿的______ (选填“物理”或“化学”)性质。
② ,X的化学式为
,X的化学式为______ 。
③兴趣小组基于“结构决定性质”的学科观念,猜想铜绿能与盐酸反应生成 气体:猜想的依据是铜绿中含有
气体:猜想的依据是铜绿中含有______ (填离子符号)。
④兴趣小组用图2所示装置进行验证。若猜想正确,能观察到的现象是______ 。
(3)铜绿是一种农业上常用的杀菌剂,可用硫酸铜和碳酸钠溶液混合加热进行制备: 。
。
为了探究适宜反应温度,进行如下三个实验:
【实验分析】
实验2中所用 溶液的体积x为
溶液的体积x为______ mL。制备时适宜的反应温度为______ 。
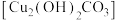 俗称铜绿,是一种蓝绿色固体,难溶于水,应用广泛。化学兴趣小组以“碱式碳酸铜的组成、结构、性质、应用和制备”为主题,开展项目式学习。
俗称铜绿,是一种蓝绿色固体,难溶于水,应用广泛。化学兴趣小组以“碱式碳酸铜的组成、结构、性质、应用和制备”为主题,开展项目式学习。【任务一】认识铜绿的组成与结构
(1)铜绿的结构如图1所示,其中“
 ”表示铜离子,“
”表示铜离子,“ ”表示碳酸根离子,则“
”表示碳酸根离子,则“ ”表示
”表示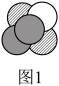
(2)探究铜绿的性质与转化
①铜绿呈蓝绿色,易被发现和识别,这利用的是铜绿的
②
 ,X的化学式为
,X的化学式为③兴趣小组基于“结构决定性质”的学科观念,猜想铜绿能与盐酸反应生成
 气体:猜想的依据是铜绿中含有
气体:猜想的依据是铜绿中含有④兴趣小组用图2所示装置进行验证。若猜想正确,能观察到的现象是
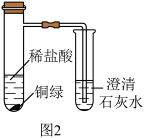
(3)铜绿是一种农业上常用的杀菌剂,可用硫酸铜和碳酸钠溶液混合加热进行制备:
 。
。为了探究适宜反应温度,进行如下三个实验:
| 编号 |  溶液体积/mL 溶液体积/mL |  溶液体积/mL 溶液体积/mL | 反应温度℃ | 实验现象 |
| 1 | 2.4 | 2.0 | 20 | 反应速度慢,得到蓝色沉淀 |
| 2 | x | 2.0 | 50 | 反应速度适中,得到蓝绿色沉淀 |
| 3 | 2.4 | 2.0 | 90 | 反应速度快,得到浅蓝色沉淀,逐渐变为黑褐色 |
实验2中所用
 溶液的体积x为
溶液的体积x为
您最近一年使用:0次
解题方法
9 . 化学知识来源于日常生活,下列解释说明中错误的是
| 选项 | 日常生活 | 解释说明 |
| A | 养花时撒熟石灰改良酸性土壤 | 熟石灰能与酸反应 |
| B | 炒菜时添加碘盐 | 补碘能预防骨质疏松症 |
| C | 利用“真金不怕火炼”识别真假黄金 | 金的化学性质稳定 |
| D | 用干布擦净被雨水淋湿的自行车 | 防止生锈 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 下列过程中一定发生化学变化的是
| A.切割玻璃 | B.食物腐烂 | C.冰雪消融 | D.电灯发光 |
您最近一年使用:0次



