解题方法
1 . “焰火穿盛唐,一眼越万年”。大年初一,洛阳用一场烟花盛宴迎接盛世龙年。烟花主要包括氧化剂、可燃物、显色剂和增亮剂四大部分。根据所学知识回答下列问题:
(1)烟花颜色主要来自金属盐在灼烧时所产生的特殊火焰颜色。下列关于盐的说法正确的是_______ 。
a.盐就是食盐 b.盐都有咸味
c.盐中一定含金属元素 d.盐中不一定含原子团
(2)可燃物主要包括木炭粉、硫磺等。请分析燃放烟花产生的空气污染物有哪些?
(3)增亮剂的作用是使烟花更加明亮绚丽,主要利用了镁粉、铝粉在燃烧时发出耀眼的强光。
①请写出增亮剂中镁粉燃烧的化学方程式_______ 。
②某实践活动小组设计如图实验方案探究镁、铝、铜三种金属的活动性顺序。请你写出能发生反应的化学方程式_______ 。_______ 。
(4)燃放烟花需要氧气,氧气是常见的助燃剂。利用下列装置图可在实验室制取氧气,请回答:_______ 。
②用F装置收集氧气,如何检验氧气已收集满?_______
③实验室用3.16g高锰酸钾完全分解制取氧气,试计算生成氧气的质量_______ 。
(1)烟花颜色主要来自金属盐在灼烧时所产生的特殊火焰颜色。下列关于盐的说法正确的是
a.盐就是食盐 b.盐都有咸味
c.盐中一定含金属元素 d.盐中不一定含原子团
(2)可燃物主要包括木炭粉、硫磺等。请分析燃放烟花产生的空气污染物有哪些?
(3)增亮剂的作用是使烟花更加明亮绚丽,主要利用了镁粉、铝粉在燃烧时发出耀眼的强光。
①请写出增亮剂中镁粉燃烧的化学方程式
②某实践活动小组设计如图实验方案探究镁、铝、铜三种金属的活动性顺序。请你写出能发生反应的化学方程式

(4)燃放烟花需要氧气,氧气是常见的助燃剂。利用下列装置图可在实验室制取氧气,请回答:

②用F装置收集氧气,如何检验氧气已收集满?
③实验室用3.16g高锰酸钾完全分解制取氧气,试计算生成氧气的质量
您最近一年使用:0次
解题方法
2 . 请回答下列问题。
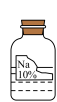
(1)实验室有一瓶试剂标签破损,其残缺的标签中只剩下“Na”和“溶质质量分数10%”字样(如图)。已知它是初中化学常用的试剂,某实验小组想确定它是哪种溶液,并进行实验探究。______ 的溶液(填选项序号之一)。
A.酸 B.碱 C.盐
②初中化学常见的含钠化合物有NaCl、NaOH、 、
、 四种物质的溶解度的数据如下:
四种物质的溶解度的数据如下:
请根据溶解度数据推理,该溶液的溶质不可能是______ (填化学式)。
③取少量试剂向其中滴加几滴无色酚酞试液,溶液呈红色,则该溶液不可能是______ 溶液(填物质名称)。
④另取少量试剂,向其中滴加少量稀硫酸有气泡产生,则该物质为______ (填化学式)
(2)已知某 样品A中可能含有
样品A中可能含有 、
、 、
、 、
、 四种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理。(设过程中所有发生的反应都恰好完全反应)
四种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理。(设过程中所有发生的反应都恰好完全反应)
Ⅰ、取一定量的固体混合物A加入适量稀硫酸并过滤,产生白色沉淀B和无色滤液C.向沉淀B中加入适量稀硝酸,沉淀不溶解。
Ⅱ、另取一定量固体A加入适量氢氧化钠并加热,得无色溶液D和无色气体E,将无色气体E通入无色酚酞,溶液变红色。
Ⅲ、将无色溶液C和无色溶液D混合后,加入适量硝酸银过滤得沉淀F和无色滤液G。
请根据实验过程和发生的现象填写以下空白:
①无色气体E的水溶液的pH______ 7(填“大于”“小于”“等于”)
②写出步骤Ⅱ中生成气体E的化学方程式______ 。
③在无色滤液G中,一定大量存在的阳离子是______ (填离子符号)。
④根据上述实验现象推断,在固体混合物A中,
______ (选填“一定存在”“一定不存在”“无法确定”之一),得出此结论的理由是______ 。
(1)实验室有一瓶试剂标签破损,其残缺的标签中只剩下“Na”和“溶质质量分数10%”字样(如图)。已知它是初中化学常用的试剂,某实验小组想确定它是哪种溶液,并进行实验探究。
A.酸 B.碱 C.盐
②初中化学常见的含钠化合物有NaCl、NaOH、
 、
、 四种物质的溶解度的数据如下:
四种物质的溶解度的数据如下:| 物质 | NaCl | NaOH |  |  |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
③取少量试剂向其中滴加几滴无色酚酞试液,溶液呈红色,则该溶液不可能是
④另取少量试剂,向其中滴加少量稀硫酸有气泡产生,则该物质为
(2)已知某
 样品A中可能含有
样品A中可能含有 、
、 、
、 、
、 四种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理。(设过程中所有发生的反应都恰好完全反应)
四种物质中的两种或多种。按下述步骤进行实验探究,观察实验现象,并加以分析推理。(设过程中所有发生的反应都恰好完全反应)Ⅰ、取一定量的固体混合物A加入适量稀硫酸并过滤,产生白色沉淀B和无色滤液C.向沉淀B中加入适量稀硝酸,沉淀不溶解。
Ⅱ、另取一定量固体A加入适量氢氧化钠并加热,得无色溶液D和无色气体E,将无色气体E通入无色酚酞,溶液变红色。
Ⅲ、将无色溶液C和无色溶液D混合后,加入适量硝酸银过滤得沉淀F和无色滤液G。
请根据实验过程和发生的现象填写以下空白:
①无色气体E的水溶液的pH
②写出步骤Ⅱ中生成气体E的化学方程式
③在无色滤液G中,一定大量存在的阳离子是
④根据上述实验现象推断,在固体混合物A中,

您最近一年使用:0次
3 . 氢经济被认为是21世纪世界经济新的转折点,关于氢能的研究是世界热点。
I.制氢
(1)工业上以甲醇(CH3OH)和水蒸气重整制H2,制取原理如图1所示:_______ (写化学式)。
②重整反应器中甲醇与足量的水蒸气反应,生成的二氧化碳与参加反应的甲醇的分子个数比为______ 。
II.储氢
(2)镁铝合金(Mg17Al12)是理想的储氢合金,其贮氢与释氢过程如图2:________ 。
②镁铝合金在一定条件下完全吸氢形成氢气球磨镁铝合金。图3为氢气球磨镁铝合金在不同温度下的储氢曲线(氢气球磨镁铝合金材料的储氢量约为3.03%),下列关于镁铝合金储氢的说法正确的是________ (填序号)。
a.镁铝合金的熔点介于金属镁和金属铝之间
b.镁铝合金在氩气中熔炼的目的是防止金属被氧化
c.由图3可知,温度升高镁铝合金储氢的速度变快
III.用氢
(3)①某新能源汽车以氢气为燃料,使用1kg氢气平均可行驶150km。如果通过图1所示的甲醇催化重整来产生氢气,64kg甲醇重整产生的氢气理论上可供这辆汽车行驶多远_______ ?(写出计算过程)
②目前氢能还没有得到广泛应用,其原因是_______ (写一条即可)。
I.制氢
(1)工业上以甲醇(CH3OH)和水蒸气重整制H2,制取原理如图1所示:

②重整反应器中甲醇与足量的水蒸气反应,生成的二氧化碳与参加反应的甲醇的分子个数比为
II.储氢
(2)镁铝合金(Mg17Al12)是理想的储氢合金,其贮氢与释氢过程如图2:

②镁铝合金在一定条件下完全吸氢形成氢气球磨镁铝合金。图3为氢气球磨镁铝合金在不同温度下的储氢曲线(氢气球磨镁铝合金材料的储氢量约为3.03%),下列关于镁铝合金储氢的说法正确的是
a.镁铝合金的熔点介于金属镁和金属铝之间
b.镁铝合金在氩气中熔炼的目的是防止金属被氧化
c.由图3可知,温度升高镁铝合金储氢的速度变快
III.用氢
(3)①某新能源汽车以氢气为燃料,使用1kg氢气平均可行驶150km。如果通过图1所示的甲醇催化重整来产生氢气,64kg甲醇重整产生的氢气理论上可供这辆汽车行驶多远
②目前氢能还没有得到广泛应用,其原因是
您最近一年使用:0次
4 . 镁和纯碱在工业生产中有广泛的用途。某地菱镁矿中主要含有 及少量
及少量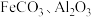 和
和 ,以菱镁矿等为原料制备镁和纯碱的工艺流程如图。
,以菱镁矿等为原料制备镁和纯碱的工艺流程如图。_______ (填“纯净物”或“混合物”)。
(2) 与盐酸反应的化学方程式为
与盐酸反应的化学方程式为_______ 。
(3)向饱和食盐水中通入 气体时,需加压通入的气体是
气体时,需加压通入的气体是_______ 。
(4)氨气还可用于处理酸性废水。工业上用氨气处理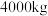 含有
含有 的质量分数为
的质量分数为 的酸性废水,反应原理为
的酸性废水,反应原理为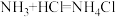 。理论上需要氨气的质量是多少?(写出计算过程)
。理论上需要氨气的质量是多少?(写出计算过程)
(5)反应③是无水 在熔融状态下,通电后反应生成
在熔融状态下,通电后反应生成 和
和 ,反应的化学方程式为
,反应的化学方程式为_______ ;反应②③均属于_______ 反应(填基本反应类型)。
(6)此工艺条件下金属离子开始沉淀和沉淀完全时的 如表。向a溶液中通入足量空气后,溶液中
如表。向a溶液中通入足量空气后,溶液中_______ 元素的化合价发生了改变;向b溶液中加入 调节溶液
调节溶液 ,所调
,所调 范围为
范围为_______ 。
 及少量
及少量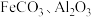 和
和 ,以菱镁矿等为原料制备镁和纯碱的工艺流程如图。
,以菱镁矿等为原料制备镁和纯碱的工艺流程如图。
(2)
 与盐酸反应的化学方程式为
与盐酸反应的化学方程式为(3)向饱和食盐水中通入
 气体时,需加压通入的气体是
气体时,需加压通入的气体是(4)氨气还可用于处理酸性废水。工业上用氨气处理
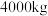 含有
含有 的质量分数为
的质量分数为 的酸性废水,反应原理为
的酸性废水,反应原理为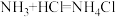 。理论上需要氨气的质量是多少?(写出计算过程)
。理论上需要氨气的质量是多少?(写出计算过程)(5)反应③是无水
 在熔融状态下,通电后反应生成
在熔融状态下,通电后反应生成 和
和 ,反应的化学方程式为
,反应的化学方程式为| 金属离子 |  |  |  |
开始沉淀的 | 8.9 | 3.4 | 1.5 |
沉淀完全的 | 10.9 | 4.7 | 2.8 |
(6)此工艺条件下金属离子开始沉淀和沉淀完全时的
 如表。向a溶液中通入足量空气后,溶液中
如表。向a溶液中通入足量空气后,溶液中 调节溶液
调节溶液 ,所调
,所调 范围为
范围为
您最近一年使用:0次
解题方法
5 . 某化学学习小组对泡腾片的成分和原理产生了兴趣。某品牌维生素C泡腾片部分标签如图所示,据此回答问题。
(1)碳酸氢钠(NaHCO3)属于_______ (填“酸”“碱”或“盐”)。
(2)取泡腾片溶于水,滴加紫色石蕊试剂,溶液变红﹐说明溶液pH______ 7(填“>”“<”或“=”)。
(3)泡腾片溶于水时闻到“橙味”香气,从微观角度解释其原因是______ 。
【任务二】测定柠檬酸的含量
(4)碳酸氢钠(NaHCO3)与柠檬酸(C6H8O7,相对分子质量为192)发生的反应为:3NaHCO3+ C6H8O7=Na3C6H5O7+3H2O+3CO2↑。该小组将4g泡腾片投入蒸馏水,反应过程中,相关测量数据如下表。根据化学方程式计算该品牌泡腾片中柠檬酸的质量分数。(假设泡腾片中的NaHCO3完全参与反应,其他物质均不产生气体)

(1)碳酸氢钠(NaHCO3)属于
(2)取泡腾片溶于水,滴加紫色石蕊试剂,溶液变红﹐说明溶液pH
(3)泡腾片溶于水时闻到“橙味”香气,从微观角度解释其原因是
【任务二】测定柠檬酸的含量
(4)碳酸氢钠(NaHCO3)与柠檬酸(C6H8O7,相对分子质量为192)发生的反应为:3NaHCO3+ C6H8O7=Na3C6H5O7+3H2O+3CO2↑。该小组将4g泡腾片投入蒸馏水,反应过程中,相关测量数据如下表。根据化学方程式计算该品牌泡腾片中柠檬酸的质量分数。(假设泡腾片中的NaHCO3完全参与反应,其他物质均不产生气体)
| 反应时间/min | 0 | t1 | t2 | t3 | t4 |
| 锥形瓶及瓶内物质总质量/g | 250.00 | 249.68 | 249.48 | 249.34 | 249.34 |
您最近一年使用:0次
2024·河南·一模
解题方法
6 . 某小组同学调查了市面上几种家用清洁剂的功能和有效成分,结果如下表。
(1)这三种清洁剂的有效成分中属于氧化物的是______ (填化学式);
(2)“漂白水”的有效成分是NaClO,能与HCl发生化学反应产生有毒的氯气(Cl2),化学方程式为______ 。所以漂白水和洁厕灵不能混合使用。
(3)该小组同学在实验室用红色布条探究“彩漂液”有效成分H2O2的漂白性,实验方案如下表所示。
资料:10%表示浓度,10%双氧水表示每100g双氧水中含有H2O2的质量为10g。
①通过以上实验得出结论:影响双氧水漂白性的因素除NaOH溶液外,还有______ 和______ 。
②本实验探究利用的科学方法是______ (填“控制变量法”,“假设实验法”或“模型研究法”)。
③欲进一步探究NaOH溶液的用量对双氧水的漂白性的影响,可补充实验:另取一条红色布条,______ (写出主要实验操作),观察实验现象。
(4)工业上常将干燥的氯气通入NaOH溶液中制得漂白水,反应的化学方程式是:______ ;
(5)若要制出NaClO含量16.9%的漂白水500kg,需要氢氧化钠多少千克?
| 清洁剂 | 洁厕灵 | 彩漂液 | 漂白水 |
| 功能 | 清除污垢,除异味 | 漂洗衣物,使色彩鲜艳 | 漂除衣物污渍 |
| 有效成分 | HCl | H2O2 | NaClO |
(1)这三种清洁剂的有效成分中属于氧化物的是
(2)“漂白水”的有效成分是NaClO,能与HCl发生化学反应产生有毒的氯气(Cl2),化学方程式为
(3)该小组同学在实验室用红色布条探究“彩漂液”有效成分H2O2的漂白性,实验方案如下表所示。
资料:10%表示浓度,10%双氧水表示每100g双氧水中含有H2O2的质量为10g。
| 实验Ⅰ | 实验Ⅱ | 实验Ⅲ | 实验Ⅳ |
|
|
|
|
| 20分钟后布条无明显变化 | 20分钟后布条颜色稍变浅 | 20分钟后布条颜色明显变浅 | 1分钟后布条红色褪去 |
②本实验探究利用的科学方法是
③欲进一步探究NaOH溶液的用量对双氧水的漂白性的影响,可补充实验:另取一条红色布条,
(4)工业上常将干燥的氯气通入NaOH溶液中制得漂白水,反应的化学方程式是:
(5)若要制出NaClO含量16.9%的漂白水500kg,需要氢氧化钠多少千克?
您最近一年使用:0次
解题方法
7 . 化学实践小组的同学们在百二河五堰段取河水,设计了一系列实践活动,对水质检测、水的净化、水的组成进行了项目化学习。
任务一:检测水质
【查阅资料】
1.水的检测指标包括色度、浑浊度、气味、硬度、肉眼可见物等。检测方法包括看、闻、尝、品、查,更详细的指标需要通过精密的仪器测定。
2.同学们查阅了相关资料,了解到国家有关水的硬度的标准为:
(1)【初步检测】同学们取少量河水,用便携式水硬度检测仪测得该自来水的硬度为311.2 mg/L,说明该河水属于______ 。
任务二:净化水
河水转化为自来水需要经过一系列步骤,但是自来水送到用户过程中仍可能被污染,因此很多公共场所使用直饮机。______ 操作。
(3)活性炭滤芯具有______ 作用,除去颜色异味的同时也除去重金属离子。
(4)紫外线灯管照射是为了杀菌消毒。直饮机使用方便,只要将其与自来水管对接,截留清除水中的有害物质(如细菌,微生物等)便能得到直饮水,直饮水属于______ (选填“纯净物”或“混合物”)。
任务三:验证水的组成
兴趣小组同学利用下图所示装置进行电解水实验。______ 。
(6)以上实验可以证明水的组成,若要证明水的组成,还可以进行的实验方案是______ 。(含操作和现象)
【成果分享】通过实践小组的合作,同学们学到了水质检测的方法、了解净水机的原理,学习了根据“化学反应中元素种类不变"来探究物质的组成,今后可以通过化学手段对更多的物质进行探索。
任务一:检测水质
【查阅资料】
1.水的检测指标包括色度、浑浊度、气味、硬度、肉眼可见物等。检测方法包括看、闻、尝、品、查,更详细的指标需要通过精密的仪器测定。
2.同学们查阅了相关资料,了解到国家有关水的硬度的标准为:
| 类别 | 极软水 | 软水 | 中硬水 | 硬水 | 高硬水 |
| 以CaCO3浓度计/(mg/L) | 0~75 | 75 ~ 150 | 150 ~300 | 300 ~450 | 450~700 |
(1)【初步检测】同学们取少量河水,用便携式水硬度检测仪测得该自来水的硬度为311.2 mg/L,说明该河水属于
任务二:净化水
河水转化为自来水需要经过一系列步骤,但是自来水送到用户过程中仍可能被污染,因此很多公共场所使用直饮机。

(3)活性炭滤芯具有
(4)紫外线灯管照射是为了杀菌消毒。直饮机使用方便,只要将其与自来水管对接,截留清除水中的有害物质(如细菌,微生物等)便能得到直饮水,直饮水属于
任务三:验证水的组成
兴趣小组同学利用下图所示装置进行电解水实验。

(6)以上实验可以证明水的组成,若要证明水的组成,还可以进行的实验方案是
【成果分享】通过实践小组的合作,同学们学到了水质检测的方法、了解净水机的原理,学习了根据“化学反应中元素种类不变"来探究物质的组成,今后可以通过化学手段对更多的物质进行探索。
您最近一年使用:0次
2024-04-21更新
|
81次组卷
|
2卷引用:湖北省十堰市房县2023-2024学年九年级下学期期中检测化学试题
解题方法
8 . 生活中含碳物质种类繁多、应用广泛。根据如图回答问题。

(1)图1中物质的类别未包括___________ (填字母)。
a.酸 b.碱 c.盐 d.氧化物
(2)图1中物质转化可通过化合反应实现的是___________ (填序号)。
(3) 转化为CO从能量角度来看,属于
转化为CO从能量角度来看,属于___________ (填“吸热”或“放热”)反应。
(4)图2实验能否证明二氧化碳与水发生了化学反应?判断并说明理由___________ 。
(5)用熟石灰吸收 可以固碳。根据化学方程式计算,吸收4.4g
可以固碳。根据化学方程式计算,吸收4.4g 至少需要熟石灰的质量为多少?
至少需要熟石灰的质量为多少?

(1)图1中物质的类别未包括
a.酸 b.碱 c.盐 d.氧化物
(2)图1中物质转化可通过化合反应实现的是
(3)
 转化为CO从能量角度来看,属于
转化为CO从能量角度来看,属于(4)图2实验能否证明二氧化碳与水发生了化学反应?判断并说明理由
(5)用熟石灰吸收
 可以固碳。根据化学方程式计算,吸收4.4g
可以固碳。根据化学方程式计算,吸收4.4g 至少需要熟石灰的质量为多少?
至少需要熟石灰的质量为多少?
您最近一年使用:0次
解题方法
9 . 水是常用溶剂,某同学进行如图实验。

(1)①倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是______ 。
②实验可知,溶质状态可以是______ 。
③实验结束后,用洗涤剂洗净B试管,原理是______ 。
④D组实验后溶液中含有的离子是______ 。
(2)询问老师得知用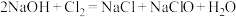 可处理
可处理 。根据化学方程式计算,处理
。根据化学方程式计算,处理 至少需
至少需 的质量是多少?(根据方程式写出详细计算过程)
的质量是多少?(根据方程式写出详细计算过程)

(1)①倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是
②实验可知,溶质状态可以是
③实验结束后,用洗涤剂洗净B试管,原理是
④D组实验后溶液中含有的离子是
(2)询问老师得知用
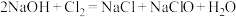 可处理
可处理 。根据化学方程式计算,处理
。根据化学方程式计算,处理 至少需
至少需 的质量是多少?(根据方程式写出详细计算过程)
的质量是多少?(根据方程式写出详细计算过程)
您最近一年使用:0次
10 . 我国科研团队研发了一种纳米“蓄水”膜反应器(如图所示),内部封装了特定催化剂,该催化剂能够实现在3MPa、240℃条件下,将二氧化碳和氢气转化成水和乙醇。纳米“蓄水”膜反应器的壳层具有高选择性,反应后,能保证生成的水集中到内部而乙醇溢出。

二氧化碳不仅能制造乙醇,还能制造淀粉、蛋白质、甲醇、尿素、纯碱、灭火剂等。
(1)图中“ ”表示的物质属于
”表示的物质属于_______ (填“有机化合物”或“无机化合物”)。
(2)壳层的优点是_______ 。
(3)纳米“蓄水”膜反应器内发生反应的化学方程式为_______ 。
(4)该技术的研发有利于缓解_______ 问题(写一条)。
我国化学工作者正在围绕绿色、低碳、环保、高效的主题,继续推进碳捕捉、碳中和,以实现二氧化碳资源的高价值利用。工业上有一种利用烧碱溶液实现“碳捕捉”的技术,其主要流程如图:

(5)分离区进行的实验操作是______ (填操作名称)。
(6)该流程中可循环利用的物质甲、乙分别是:甲______ 、乙______ 。
(7)反应区1中发生的属于复分解反应的化学方程式为_______ 。
(8)我国力争在2060年前实现“碳中和”。下列措施不利于大气中CO2,减少的是

二氧化碳不仅能制造乙醇,还能制造淀粉、蛋白质、甲醇、尿素、纯碱、灭火剂等。
(1)图中“
 ”表示的物质属于
”表示的物质属于(2)壳层的优点是
(3)纳米“蓄水”膜反应器内发生反应的化学方程式为
(4)该技术的研发有利于缓解
我国化学工作者正在围绕绿色、低碳、环保、高效的主题,继续推进碳捕捉、碳中和,以实现二氧化碳资源的高价值利用。工业上有一种利用烧碱溶液实现“碳捕捉”的技术,其主要流程如图:

(5)分离区进行的实验操作是
(6)该流程中可循环利用的物质甲、乙分别是:甲
(7)反应区1中发生的属于复分解反应的化学方程式为
(8)我国力争在2060年前实现“碳中和”。下列措施不利于大气中CO2,减少的是
| A.用氨水抽集废气中的CO2,将其转化为氨肥 |
| B.大力推广使用干冰实现人工增雨,缓解旱情 |
| C.利用和开发风能、太阳能、氢能等清洁能源 |
| D.通过植树造林,利用光合作用吸收大气中的CO2 |
您最近一年使用:0次







