解题方法
1 . 氢气的开发利用是氢能研究的热点。
一、氢气的发现和制备
(1)1766年,英国科学家卡文迪许用铁与稀盐酸作用,制得了可燃性的H2,同时还得到了浅绿色的氯化亚铁溶液,写出该反应的符号表达式___________ 。
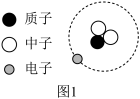
(2)目前制氢的方法主要有电解水制氢。电解水制氢中,使用氚进行核能发电,图1能表示氚的原子结构,氚属于___________ 元素的一种原子,氚原子的相对原子质量约为___________ 。
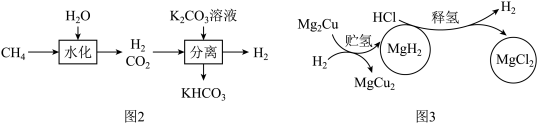
(3)甲烷和水蒸气催化重整是制高纯氢的方法之一,主要流程如图2:
①“分离”时K2CO3溶液吸收CO2生成KHCO3,反应的符号表达式为___________ 。
②甲烷无氧催化重整可获得碳氢化合物X,X的相对分子质量为106,且碳、氢元素的质量比为48:5,则X的化学式为___________ 。
二、氢气的贮存和释放
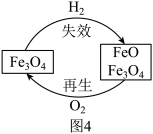
Mg2Cu可用于化学储氢,其贮氢与释氢过程如图3所示。
(4)贮氢反应需要在高温和隔绝空气的条件下进行,隔绝空气的原因___________ 。
(5)释氢释放的H2比贮氢吸收的H2___________ (选填“多”或“少”)
(6)释放出的氢气可用作氢燃料电池,氢燃料电池工作时将___________ 能转化为电能。
(7)2022年北京冬奥会火炬“飞扬”以氢气为燃料,氢气燃烧的符号表达式为___________ 。
三、氢气在工业生产中的应用
合成氨工艺需要用到氢气,在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨气。
(8)N2是合成氨的重要原料。工业上可从空气中获得N2,利用空气中各成分的___________ 不同将空气成分进行分离。
(9)Fe3O4是铁触媒的主要成分。合成氨催化过程中因部分Fe3O4与H2反应使催化剂“失效”。在一定温度下可用O2将其“再生”,原理如图4所示。“再生”过程中铁元素的质量分数___________ (选填“变大”、“不变”或“变小”)。
(10)图5是Fe3O4在失效和再生过程中的质量与时间变化的关系图。

T1~T3时刻,是Fe3O4失效过程,T4~T5时刻,是固体再生过程。
则:A点处,固体中铁元素的质量=___________ g。
B点处,固体中含Fe3O4的质量为46.4g,则M=___________ g。
C点处,Fe3O4和FeO的质量比为___________ 。
一、氢气的发现和制备
(1)1766年,英国科学家卡文迪许用铁与稀盐酸作用,制得了可燃性的H2,同时还得到了浅绿色的氯化亚铁溶液,写出该反应的符号表达式
(2)目前制氢的方法主要有电解水制氢。电解水制氢中,使用氚进行核能发电,图1能表示氚的原子结构,氚属于

(3)甲烷和水蒸气催化重整是制高纯氢的方法之一,主要流程如图2:

①“分离”时K2CO3溶液吸收CO2生成KHCO3,反应的符号表达式为
②甲烷无氧催化重整可获得碳氢化合物X,X的相对分子质量为106,且碳、氢元素的质量比为48:5,则X的化学式为
二、氢气的贮存和释放
Mg2Cu可用于化学储氢,其贮氢与释氢过程如图3所示。
(4)贮氢反应需要在高温和隔绝空气的条件下进行,隔绝空气的原因
(5)释氢释放的H2比贮氢吸收的H2
(6)释放出的氢气可用作氢燃料电池,氢燃料电池工作时将
(7)2022年北京冬奥会火炬“飞扬”以氢气为燃料,氢气燃烧的符号表达式为
三、氢气在工业生产中的应用
合成氨工艺需要用到氢气,在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨气。
(8)N2是合成氨的重要原料。工业上可从空气中获得N2,利用空气中各成分的

(9)Fe3O4是铁触媒的主要成分。合成氨催化过程中因部分Fe3O4与H2反应使催化剂“失效”。在一定温度下可用O2将其“再生”,原理如图4所示。“再生”过程中铁元素的质量分数
(10)图5是Fe3O4在失效和再生过程中的质量与时间变化的关系图。

T1~T3时刻,是Fe3O4失效过程,T4~T5时刻,是固体再生过程。
则:A点处,固体中铁元素的质量=
B点处,固体中含Fe3O4的质量为46.4g,则M=
C点处,Fe3O4和FeO的质量比为
您最近一年使用:0次
解题方法
2 . 芯片是中美经贸摩擦的焦点之一、制造芯片的高纯硅可以用下述方法制取(反应条件略):
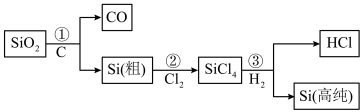
下列有关说法错误的是

下列有关说法错误的是
| A.硅原子的核电荷数为14 | B.SiCl4中Si的化合价为+4 |
| C.反应①、③均为置换反应 | D.反应前后化合价发生改变的元素只有Si |
您最近一年使用:0次
名校
3 . 元素周期表是学习和研究化学的重要工具。根据图甲、图乙、图丙回答下列问题:

(1)图甲中所示粒子共表示_________ 种元素,_________ (填字母序号)表示的微粒性质较稳定。
(2)原子序数为13的元素与图甲中D元素组成的化合物的化学式是_________ 。
(3)嫦娥五号采集的月壤样品中存在着大量的氦-3(氦-3是含有2个质子和1个中子的氦原子),其原子结构示意图为图甲中的_________ (填字母序号)。图甲中表示离子结构的是_________ (填字母符号)。
(4)图甲中E为硒的原子结构示意图,则X=_________ ,它与图乙中_________ (填元素名称)的化学性质相似。
(5)原子得到或失去电子后形成离子。图丙为某粒子的结构示意图:

①当a=9时,该粒子是_________ (选填“原子”或“阳离子”或“阴离子”)。
②当a=_________ ,该粒子是带有2个单位正电荷的阳离子。

(1)图甲中所示粒子共表示
(2)原子序数为13的元素与图甲中D元素组成的化合物的化学式是
(3)嫦娥五号采集的月壤样品中存在着大量的氦-3(氦-3是含有2个质子和1个中子的氦原子),其原子结构示意图为图甲中的
(4)图甲中E为硒的原子结构示意图,则X=
(5)原子得到或失去电子后形成离子。图丙为某粒子的结构示意图:

①当a=9时,该粒子是
②当a=
您最近一年使用:0次
解题方法
4 . 在宏观、微观和符号之间建立联系是化学特有的思维方式。
(1)嫦娥五号完成我国首次月球采样任务,带回了1731g月壤月壤中含有丰富的氦3,已知氦3的质子数为2,中子数为1,氦3的核外电子数为_______ 。
(2)氟元素是人体必须的微量元素,图甲是氟元素的部分信息,图乙是A~E五种粒子的结构示意图。
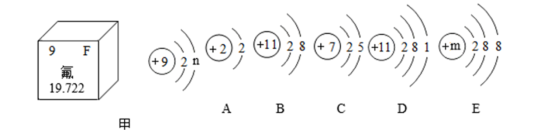
①图中n的值______ ,氟是一种______ (填金属或非金属)元素, 氟元素位于元素周期表的第______ 周期。
②A~D四种粒子中属于同种元素的是_____ (填序号,下同),具有相对稳定结构的是____ 。
③若E为某原子得到一个电子形成的离子,则m的数值是_____ 。
④D粒子在化学反应中容易__________ (填得到或失去)电子,形成_____ (填阴或阳)离子。
(1)嫦娥五号完成我国首次月球采样任务,带回了1731g月壤月壤中含有丰富的氦3,已知氦3的质子数为2,中子数为1,氦3的核外电子数为
(2)氟元素是人体必须的微量元素,图甲是氟元素的部分信息,图乙是A~E五种粒子的结构示意图。

①图中n的值
②A~D四种粒子中属于同种元素的是
③若E为某原子得到一个电子形成的离子,则m的数值是
④D粒子在化学反应中容易
您最近一年使用:0次
解题方法
5 . 完成下列计算题:
(1)某元素R的原子能够形成核外有10个电子的Rn+,则元素R的原子序数为_____。
(2)已知:一个C﹣12原子的质量为m克,一个氧原子的质量为n克,则该氧原子的相对原子质量为_____(用m、n表示)。
(3)配制1000g 10%的氯化钠溶液,需要的溶质质量为_____。
(1)某元素R的原子能够形成核外有10个电子的Rn+,则元素R的原子序数为_____。
(2)已知:一个C﹣12原子的质量为m克,一个氧原子的质量为n克,则该氧原子的相对原子质量为_____(用m、n表示)。
(3)配制1000g 10%的氯化钠溶液,需要的溶质质量为_____。
您最近一年使用:0次
解题方法
6 . 1.根据下图提供的信息,请回答问题:
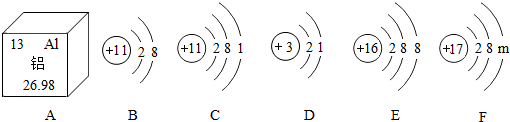
(1)A中铝原子的核电荷数为_________ ,铝元素的相对原子质量为_________ 。
(2)C在化学反应中易_________ (填“得”或“失”)电子达到稳定结构,若F为某元素的原子,则m为________ 。
(3)属于同种元素的是______ (填字母);表示阴离子的是________ (填字母)。
(4)B和E两种粒子构成化合物的化学式为_________ 。
(5)相同质量的钠和铝两种金属,所含原子较多的是_________ 。

(1)A中铝原子的核电荷数为
(2)C在化学反应中易
(3)属于同种元素的是
(4)B和E两种粒子构成化合物的化学式为
(5)相同质量的钠和铝两种金属,所含原子较多的是
您最近一年使用:0次
2016-11-28更新
|
85次组卷
|
2卷引用:2016届江苏省无锡市崇安区九年级上学期期中测试化学试卷



