解题方法
1 . 某微粒的结构示意图为: 回答下列有关问题:
回答下列有关问题:
(1)X的值为______ 。根据元素原子结构示意图,不能直接获得的信息是______ (填序号)
①核电荷数 ②相对原子质量 ③电子层数
(2)与元素的化学性质关系最密切的是______ (填序号);
①原子的核外电子数 ②元素的核电荷数 ③原子的最外层电子数
(3)该图表示______ 元素的微粒结构示意图(填“金属”或“非金属”);
(4)该示意图表示的化学符号为______ 。
 回答下列有关问题:
回答下列有关问题:(1)X的值为
①核电荷数 ②相对原子质量 ③电子层数
(2)与元素的化学性质关系最密切的是
①原子的核外电子数 ②元素的核电荷数 ③原子的最外层电子数
(3)该图表示
(4)该示意图表示的化学符号为
您最近一年使用:0次
解题方法
2 . 按要求回答:
(1)“人造太阳”将为人类提供永不枯竭的清洁能源。“人造太阳”合理利用了可控核聚变,氘、氚是核聚变的热核材料。
①从上表中可知,氘和氚属于同种元素的原子,其判断的依据______ ;上表中x=______ 。
②贮存氘气的钢瓶禁止靠近明火,据此推测氘气具有的化学性质是______ 。
③除核能外清洁能源还有______ 。(任写一种)
(2)常温下,在空气中铝的表面会形成致密的氧化膜。铝粉俗称银粉、银漆,常用做涂料,保护铁制品不被锈蚀。铝的密度很小,质地较软,可制成硬铝、超硬铝、防锈铝等各种铝合金。一架超音速飞机约由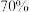 的铝及其合金制成。铝热法是一种金属热还原法,利用铝热法可焊接铁轨,如铝与氧化铁在高温条件下反应生成氧化铝和一种单质,可使温度达2000℃
的铝及其合金制成。铝热法是一种金属热还原法,利用铝热法可焊接铁轨,如铝与氧化铁在高温条件下反应生成氧化铝和一种单质,可使温度达2000℃ 以上。
以上。
①“银粉”、“银漆”保护铁制品不被锈蚀的原因是______ 。
②铝合金制造超音速飞机是利用了铝合金______ 的性质。(至少答出2点)
③铝热法焊接铁轨时,铝与氧化铁的反应的化学方程式是______ 。
④高炉炼铁的主要原理同样是运用了热还原法,写出以磁铁矿为原料炼铁的化学方程式:______ 。
(1)“人造太阳”将为人类提供永不枯竭的清洁能源。“人造太阳”合理利用了可控核聚变,氘、氚是核聚变的热核材料。
| 原子种类 | 质子数 | 中子数 | 核外电子数 |
| 氘 | 1 | 1 | 1 |
| 氚 | 1 | 2 | x |
①从上表中可知,氘和氚属于同种元素的原子,其判断的依据
②贮存氘气的钢瓶禁止靠近明火,据此推测氘气具有的化学性质是
③除核能外清洁能源还有
(2)常温下,在空气中铝的表面会形成致密的氧化膜。铝粉俗称银粉、银漆,常用做涂料,保护铁制品不被锈蚀。铝的密度很小,质地较软,可制成硬铝、超硬铝、防锈铝等各种铝合金。一架超音速飞机约由
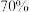 的铝及其合金制成。铝热法是一种金属热还原法,利用铝热法可焊接铁轨,如铝与氧化铁在高温条件下反应生成氧化铝和一种单质,可使温度达2000℃
的铝及其合金制成。铝热法是一种金属热还原法,利用铝热法可焊接铁轨,如铝与氧化铁在高温条件下反应生成氧化铝和一种单质,可使温度达2000℃ 以上。
以上。①“银粉”、“银漆”保护铁制品不被锈蚀的原因是
②铝合金制造超音速飞机是利用了铝合金
③铝热法焊接铁轨时,铝与氧化铁的反应的化学方程式是
④高炉炼铁的主要原理同样是运用了热还原法,写出以磁铁矿为原料炼铁的化学方程式:
您最近一年使用:0次
解题方法
3 . “宏观一微观一符号”是化学视角认识物质的方法。根据下列图示回答问题:
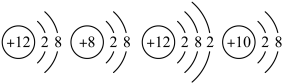
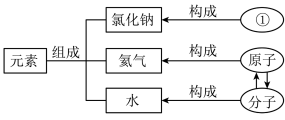
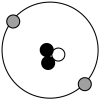
图1 图2 图3
(1)图1中,属于原子的是_______ (填字母,下同);稳定结构的粒子是___________ ;属于同种元素的是__________ ,理由是_________ 。
(2)图2中的①处所填内容是________ ,氯化钠的符号_________ 。
(3)图3是某原子的结构模型,该原子的中子数是________ 。
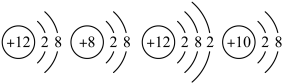


图1 图2 图3
(1)图1中,属于原子的是
(2)图2中的①处所填内容是
(3)图3是某原子的结构模型,该原子的中子数是
您最近一年使用:0次
2021-11-25更新
|
324次组卷
|
3卷引用:广东省中山市2021-2022学年九年级上学期期中化学试题
名校
4 . 阅读下面两条信息,回答问题。
信息一:金是一种广受欢迎的贵金属,有金黄色金属光泽,密度大,延展性好,而且金非常稳定,与大多数物质都不发生反应,常用来加工首饰。
信息二:金元素在自然界的含量非常稀少,它的化学符号是Au,原子序数是79,相对原子质量是197.00。
(1)根据信息一:找出金的物理性质和化学性质(各一条)
物理性质:____________________________________ ;
化学性质:____________________________________ 。
(2)金原子的核外电子数是______ ;质子数是______ ;中子数是______ 。
信息一:金是一种广受欢迎的贵金属,有金黄色金属光泽,密度大,延展性好,而且金非常稳定,与大多数物质都不发生反应,常用来加工首饰。
信息二:金元素在自然界的含量非常稀少,它的化学符号是Au,原子序数是79,相对原子质量是197.00。
(1)根据信息一:找出金的物理性质和化学性质(各一条)
物理性质:
化学性质:
(2)金原子的核外电子数是
您最近一年使用:0次
2018-04-29更新
|
460次组卷
|
3卷引用:吉林省长春汽车经济技术开发区第九中学教育联盟2017-2018学年八年级下学期期中质量检测化学试题
名校
解题方法
5 . 金属铁是目前世界上使用最多的金属,在生产和生活中有着广泛的用途。
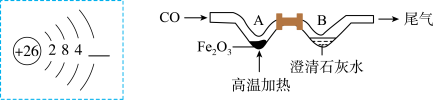
(1)请将上边虚线框内铁原子的结构示意图补画完整______ 。
(2)铁可制成铁锅烹调食物,利用了铁的延展性和_______ 性。
(3)用如图所示微型装置模拟工业炼铁。V形管中A处发生反应的化学方程式是_____ ;B处V形管内可观察到的现象是_____ ;
(4)某化学小组将一定量的铁粉加入到Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,滤液呈蓝色,则该实验过程中首先发生反应的化学方程式为_____ ;向滤渣中滴加盐酸时______ (填“有”或“没有”)气泡产生;滤液中一定含有的溶质是______ (写化学式);
(5)某实验室用废硫酸与铁反应制取硫酸亚铁。98g废硫酸与足量铁完全反应,生成0.2g气体,废硫酸中溶质的质量分数是_____ 。

(1)请将上边虚线框内铁原子的结构示意图补画完整
(2)铁可制成铁锅烹调食物,利用了铁的延展性和
(3)用如图所示微型装置模拟工业炼铁。V形管中A处发生反应的化学方程式是
(4)某化学小组将一定量的铁粉加入到Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,滤液呈蓝色,则该实验过程中首先发生反应的化学方程式为
(5)某实验室用废硫酸与铁反应制取硫酸亚铁。98g废硫酸与足量铁完全反应,生成0.2g气体,废硫酸中溶质的质量分数是
您最近一年使用:0次
解题方法
6 . 2020--2022 年,中国的科技成果“井喷”。长征 5 号、嫦娥 5 号、“奋斗者”号载人潜水器、“人造太阳”核聚变有了历史突破等令世界瞩目,让国人自豪。
(1)月球土壤中含有大量的 He—3 原子,是热核聚变重要原料。He—3 原子的原子核内有 2个质子和 1 个中子,则 He—3 原子的原子核外电子数为______(填字母)。
(2)潜航员、航天员的食品种类繁多、营养全面。某种水果每 100 克食用部分中的营养成分含量如下表。
表中属于人体必需的微量元素的是铁和______ ,人体缺乏______ 元素会导致贫血,缺钙会导致人患上______ (填写“侏儒症”或“骨质疏松”)。
(3)载人潜水器中的空气要与地表空气的组成基本一致,其中含量最多的是______ (填化学式)。
(4)钛合金具有熔点高、强度大、可塑性好、易于加工,钛合金与人体有很好的“相容性”等优良性能,下列用途与钛合金性能相符的是______(填字母)。
(5)下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:

①右上图为镁元素的某种微粒结构示意图,该图表示______ (填字母)。
A.原子 B.阳离子 C.阴离子
②已知:镁除了能与氧气反应,还可与氮气,二氧化碳反应。镁在氮气中燃烧能生成氮化镁(氮元素化合价为-3 价),则此反应的化学符号表达式为______ 。
③反应Ⅱ需在下列哪种环境中进行______ (填字母)。
A.稀有气体中 B.空气中 C.氮气中 D.CO2气体中
(1)月球土壤中含有大量的 He—3 原子,是热核聚变重要原料。He—3 原子的原子核内有 2个质子和 1 个中子,则 He—3 原子的原子核外电子数为______(填字母)。
| A.1 | B.2 | C.3 |
(2)潜航员、航天员的食品种类繁多、营养全面。某种水果每 100 克食用部分中的营养成分含量如下表。
蛋白质/g | 脂肪/g | 糖类/g | 钙 | 铁 | 锌 | 维生素A/mg | 维生素C/mg |
0.8 | 0.2 | 10.5 | 20 | 0.4 | 0.14 | 27 | 33 |
(3)载人潜水器中的空气要与地表空气的组成基本一致,其中含量最多的是
(4)钛合金具有熔点高、强度大、可塑性好、易于加工,钛合金与人体有很好的“相容性”等优良性能,下列用途与钛合金性能相符的是______(填字母)。
| A.人造关节 | B.“奋斗者”号潜航器 | C.保险丝 |
(5)下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:

①右上图为镁元素的某种微粒结构示意图,该图表示
A.原子 B.阳离子 C.阴离子
②已知:镁除了能与氧气反应,还可与氮气,二氧化碳反应。镁在氮气中燃烧能生成氮化镁(氮元素化合价为-3 价),则此反应的化学符号表达式为
③反应Ⅱ需在下列哪种环境中进行
A.稀有气体中 B.空气中 C.氮气中 D.CO2气体中
您最近一年使用:0次
解题方法
7 . 建立“宏观—微观—符号”之间的联系,是化学学习的重要方法。
(1)北斗三号卫星上采用了我国自主研发的更高稳定度、更小漂移率的新型高精度铷原子钟,该时钟每三千年误差不到一秒。铷和钠的相关信息如下图。

铷的化学性质与钠的化学性质相似,判断依据是_______ 。
(2)“嫦娥四号”在月球土壤中发现了丰富的He—3,图为He—3发生的一种核聚变示意图。
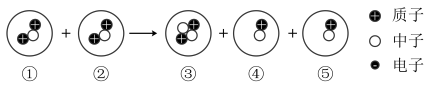
①②③④⑤中共有_______ 种元素,相对原子质量最大的是_______ (填序号)。
(3)科学家发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。它与天体中的中子星构成类似。有关该粒子的说法正确的是_______。
(4)经检验,NaHSO4在水中解离出两种阳离子和一种阴离子,微观示意图如下图。
a.请在图中圆圈处补充硫酸氢钠溶液中带电的微粒符号_____ ;
b.在溶液中滴加_______ (写化学式)溶液既能降低该溶液的酸性又能生成沉淀。

(5)如下图,硫化氢在氧气中燃烧的微观示意图,实际参加反应的D,E的分子个数比为____ 。

(1)北斗三号卫星上采用了我国自主研发的更高稳定度、更小漂移率的新型高精度铷原子钟,该时钟每三千年误差不到一秒。铷和钠的相关信息如下图。

铷的化学性质与钠的化学性质相似,判断依据是
(2)“嫦娥四号”在月球土壤中发现了丰富的He—3,图为He—3发生的一种核聚变示意图。

①②③④⑤中共有
(3)科学家发现一种只有四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。它与天体中的中子星构成类似。有关该粒子的说法正确的是_______。
| A.不显电性 |
| B.失去一个中子后显+1 价 |
| C.质量相当于一个氦(He)原子的质量 |
| D.在现有的周期表中不可能有它的位置 |
a.请在图中圆圈处补充硫酸氢钠溶液中带电的微粒符号
b.在溶液中滴加

(5)如下图,硫化氢在氧气中燃烧的微观示意图,实际参加反应的D,E的分子个数比为

您最近一年使用:0次
解题方法
8 . 2020年6月23日,长征三号乙运载火箭将北斗三号最后一颗组网卫星成功送入预定轨道,我国北斗导航地位将进一步提升。从化学视角回答下列问题:
(1)卫星制造使用了黄金、钛合金,其中用作天线的是______ 。使用黄金制作卫星的电子元件,利用了金的什么化学性质?______ 填序号。
A.光泽好 B.耐磨、易加工 C.容易导电 D.很难被氧化
(2)卫星的太阳能电池帆板用先进的砷化镓主板和铝合金边框制成,砷(As)原子的结构示意图如图,其中X=______ 。铝合金比纯铝具有的优势是______ (写出1条即可)。

(3)运载火箭用偏二甲肼(C2H8N2)作燃料,N2O4作氧化剂。火箭发射时,燃料与氧化剂剧烈反应放出大量的热,并生成对空气无污染的两种氧化物和一种单质,这种单质的化学式为______ ,两种氧化物中相对分子质量较大的是______ 。
(1)卫星制造使用了黄金、钛合金,其中用作天线的是
A.光泽好 B.耐磨、易加工 C.容易导电 D.很难被氧化
(2)卫星的太阳能电池帆板用先进的砷化镓主板和铝合金边框制成,砷(As)原子的结构示意图如图,其中X=

(3)运载火箭用偏二甲肼(C2H8N2)作燃料,N2O4作氧化剂。火箭发射时,燃料与氧化剂剧烈反应放出大量的热,并生成对空气无污染的两种氧化物和一种单质,这种单质的化学式为
您最近一年使用:0次
解题方法
9 . (1)用化学用语填空:
①75%乙醇溶液能有效灭活“新冠肺炎病毒”,乙醇溶液的溶剂为_____ 。
②写出2个锰酸根离子,并标出其中金属元素的化合价:_______ 。
(2)锌是一种使用非常广泛的金属,我国古代就已掌握了炼锌技术。

①《天工开物》中介绍了锌的冶炼方法:把炉甘石(ZnCO3)和煤炭饼装入炼锌罐(如右图所示),泥封,“其底铺薪,发火煅红”,“冷定毁罐取出”。请解释“冷定(即冷却)后才可毁罐取锌”的原因:______ 。
②在已调平的托盘大平的左右两端各放一只质量相等的烧杯,烧杯内各盛有等质量等质量分数的足量稀盐酸。然后先向左边烧杯中加入8.1g的氧化锌,若要天平最终保持平衡,则向右边烧杯中加入碳酸锌的质量为____ g;若想让天平指针最终偏向左边,则右边烧杯加入的锌粒质量最多为_____ g(精确到0.1g)。
(3) 、
、 分别表示氧元素的两种不同的原子,在化学原理探究和核化学方面有广泛应用,
分别表示氧元素的两种不同的原子,在化学原理探究和核化学方面有广泛应用, 、
、 可简写成
可简写成 、
、 。
。
①两种原子中,_______ 数目相等。
a 质子
b 中子
c 电子
d 核电荷数
e 最外层电子数
②若H2与 反应生成的水表示为H218O,则如下反应的微观模拟图的化学方程式为
反应生成的水表示为H218O,则如下反应的微观模拟图的化学方程式为_____ 。

①75%乙醇溶液能有效灭活“新冠肺炎病毒”,乙醇溶液的溶剂为
②写出2个锰酸根离子,并标出其中金属元素的化合价:
(2)锌是一种使用非常广泛的金属,我国古代就已掌握了炼锌技术。

①《天工开物》中介绍了锌的冶炼方法:把炉甘石(ZnCO3)和煤炭饼装入炼锌罐(如右图所示),泥封,“其底铺薪,发火煅红”,“冷定毁罐取出”。请解释“冷定(即冷却)后才可毁罐取锌”的原因:
②在已调平的托盘大平的左右两端各放一只质量相等的烧杯,烧杯内各盛有等质量等质量分数的足量稀盐酸。然后先向左边烧杯中加入8.1g的氧化锌,若要天平最终保持平衡,则向右边烧杯中加入碳酸锌的质量为
(3)
 、
、 分别表示氧元素的两种不同的原子,在化学原理探究和核化学方面有广泛应用,
分别表示氧元素的两种不同的原子,在化学原理探究和核化学方面有广泛应用, 、
、 可简写成
可简写成 、
、 。
。①两种原子中,
a 质子
b 中子
c 电子
d 核电荷数
e 最外层电子数
②若H2与
 反应生成的水表示为H218O,则如下反应的微观模拟图的化学方程式为
反应生成的水表示为H218O,则如下反应的微观模拟图的化学方程式为
您最近一年使用:0次
解题方法
10 . 我国探月工程“嫦娥五号”探测器首次从月球带回约1731g月壤,国家航天局同步发布了《月球样品管理办法》。根据所学知识回答下列问题:
(1)“嫦娥五号”探测器的关键部件采用铝合金而不采用纯铝,原因是________ 。
(2)月球制氧机利用月球土壤制备出氧气,用于未来人类移民。月球制氧机可使用太阳能电池板,将丰富的太阳光能转换成______ 能,月壤中一定含有____ (填“氧气”或“氧元素”)。
(3)月壤样品中发现核聚变发电的理想原料氦﹣3,其原子核中质子数为2、中子数为1,氦原子中的核电荷数为____ ,氦与其它物质____ (填“容易”或“不易”)发生化学反应。
(4)月球表面富含钛铁矿,钛因其硬度大、熔点高、常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”。工业上以钛铁矿为(主要成分为钛酸亚铁FeTiO3)为原料生产钛,其主要工艺流程如下图所示。

①写出镁在高温下与TiCl4反应生成钛和氯化镁的化学方程式_________ ,此反应说明金属钛的活动性比镁_________ (填“强”或“弱”)。
②上述生产过程中得到的金属钛中混有少量金属杂质,可加入____ 除去(填试剂名称)。
(1)“嫦娥五号”探测器的关键部件采用铝合金而不采用纯铝,原因是
(2)月球制氧机利用月球土壤制备出氧气,用于未来人类移民。月球制氧机可使用太阳能电池板,将丰富的太阳光能转换成
(3)月壤样品中发现核聚变发电的理想原料氦﹣3,其原子核中质子数为2、中子数为1,氦原子中的核电荷数为
(4)月球表面富含钛铁矿,钛因其硬度大、熔点高、常温下耐酸碱、耐腐蚀等优良的性能,被誉为“未来金属”。工业上以钛铁矿为(主要成分为钛酸亚铁FeTiO3)为原料生产钛,其主要工艺流程如下图所示。

①写出镁在高温下与TiCl4反应生成钛和氯化镁的化学方程式
②上述生产过程中得到的金属钛中混有少量金属杂质,可加入
您最近一年使用:0次



