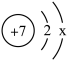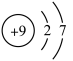解题方法
1 . 海水中含有大量的氯化钠、氯化镁等,研究它们的组成和性质具有重要意义。
(1)海水晒盐时,液态水蒸发为水蒸气的过程中,水分子的结构________ (填“发生”或“没有”)改变。
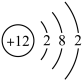
(2)钠原子的结构示意图为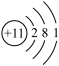 ,氯原子的结构示意图为
,氯原子的结构示意图为 。
。
①钠原子转变为钠离子时,发生变化的是________ (填“质子数”或“电子数”)。
② 的数值为
的数值为________ 。
(3)标出氯化镁中镁元素的化合价________ 。
(1)海水晒盐时,液态水蒸发为水蒸气的过程中,水分子的结构
(2)钠原子的结构示意图为
 ,氯原子的结构示意图为
,氯原子的结构示意图为 。
。①钠原子转变为钠离子时,发生变化的是
②
 的数值为
的数值为(3)标出氯化镁中镁元素的化合价
您最近一年使用:0次
2024·江苏南京·二模
解题方法
2 . 第十九届亚运会秉持着“绿色、智能、节俭、文明”的办会理念。
(1)“薪火”火炬燃料采用生物质燃气。生物质燃气是利用农作物粘杆、禽畜粪便等原料转化成可燃性能源,其属于_____________ (选填“可再生”或“不可再生”)能源。
(2)建筑墙体采用隔热、保温性能好的聚氨酯材料,聚氨酯属于_____________ (填“无机非金属材料”或“有机高分子材料”)。
(3)燃料创新使用“零碳甲醇燃料”,即通过二氧化碳和氢气在一定条件下生成甲(CH3OH)和一种常见的液体,该反应的化学方程式为_____________ ,设计实验,证明甲醇的组成中含有氢元素。
(4)月壤中存在着大量的3He有望成为未来的清洁能源。3He原子内质子数为2,中子数为1,核外电子数为_____________ 。
(5)单晶硅为信息技术领域提供了基础材料。工业上利用二氧化硅和碳在高温条件下反应制得粗硅,同时生成一种可燃性气体,预测该可燃性气体是_____________ (填化学式)。
(6)锂电池是现代通讯工具常用电池,放电过程中,锂原子因_____________ (选填“得到”或“失去”)电子而变成带1个单位正电荷的锂离子。
(1)“薪火”火炬燃料采用生物质燃气。生物质燃气是利用农作物粘杆、禽畜粪便等原料转化成可燃性能源,其属于
(2)建筑墙体采用隔热、保温性能好的聚氨酯材料,聚氨酯属于
(3)燃料创新使用“零碳甲醇燃料”,即通过二氧化碳和氢气在一定条件下生成甲(CH3OH)和一种常见的液体,该反应的化学方程式为
| 实验步骤 | 实验现象 | 实验结论 |
| 甲醇的组成中含有氢元素 |
(5)单晶硅为信息技术领域提供了基础材料。工业上利用二氧化硅和碳在高温条件下反应制得粗硅,同时生成一种可燃性气体,预测该可燃性气体是
(6)锂电池是现代通讯工具常用电池,放电过程中,锂原子因
您最近一年使用:0次
解题方法
3 . 第十九届亚运会秉持着“绿色、智能、节俭、文明”的办会理念。
(1)“薪火”火炬燃料采用生物质燃气。生物质燃气是利用农作物粘杆、禽畜粪便等原料转化成可燃性能源,其属于_____________ (选填“可再生”或“不可再生”)能源。
(2)建筑墙体采用隔热、保温性能好的聚氨酯材料,聚氨酯属于_____________ (填“无机非金属材料”或“有机高分子材料”)。
(3)燃料创新使用“零碳甲醇燃料”,即通过二氧化碳和氢气在一定条件下生成甲(CH3OH)和一种常见的液体,该反应的化学方程式为_____________ 。
(4)月壤中存在着大量的3He有望成为未来的清洁能源。3He原子内质子数为2,中子数为1,核外电子数为_____________ 。
(5)单晶硅为信息技术领域提供了基础材料。工业上利用二氧化硅和碳在高温条件下反应制得粗硅,同时生成一种可燃性气体,预测该可燃性气体是_____________ (填化学式)。
(6)锂电池是现代通讯工具常用电池,放电过程中,锂原子因_____________ (选填“得到”或“失去”)电子而变成带1个单位正电荷的锂离子。
(1)“薪火”火炬燃料采用生物质燃气。生物质燃气是利用农作物粘杆、禽畜粪便等原料转化成可燃性能源,其属于
(2)建筑墙体采用隔热、保温性能好的聚氨酯材料,聚氨酯属于
(3)燃料创新使用“零碳甲醇燃料”,即通过二氧化碳和氢气在一定条件下生成甲(CH3OH)和一种常见的液体,该反应的化学方程式为
(4)月壤中存在着大量的3He有望成为未来的清洁能源。3He原子内质子数为2,中子数为1,核外电子数为
(5)单晶硅为信息技术领域提供了基础材料。工业上利用二氧化硅和碳在高温条件下反应制得粗硅,同时生成一种可燃性气体,预测该可燃性气体是
(6)锂电池是现代通讯工具常用电池,放电过程中,锂原子因
您最近一年使用:0次
2024九年级·江苏·专题练习
解题方法
4 . 宏观和微观相结合是认识物质结构与性质的重要方法。
下表为三种元素原子的结构示意图。
(1)上表中x=______ 。氟原子在反应中易______ 选填(得到或失去)电子。
(2)镁原子失去2个电子所形成离子的符号为______ 。
(3)已知这三种原子的核外电子层数越多,原子半径越大;核外电子层数相等时,核电荷数越多,原子半径越小。这三种原子中半径最小的是______ 。
下表为三种元素原子的结构示意图。
| 元素名称 | 氮 | 氟 | 镁 |
| 原子结构示意图 |
|
|
|
(1)上表中x=
(2)镁原子失去2个电子所形成离子的符号为
(3)已知这三种原子的核外电子层数越多,原子半径越大;核外电子层数相等时,核电荷数越多,原子半径越小。这三种原子中半径最小的是
您最近一年使用:0次
2024九年级·江苏·专题练习
解题方法
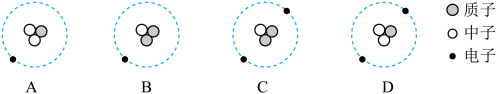
5 . 电解水法制氢的能量转化如图所示,氚可用于核能发电,氚是一种原子核中有1个质子和2个中子的原子。氚属于______ 元素的一种原子。下列示意图能表示氚原子的是______ (填序号)。
您最近一年使用:0次
名校
解题方法
6 . 阅读下列短文,回答相关问题。
氢能是一种二次能源(自然界中以现成形式提供的能源称为一次能源,需要依靠其他能源的能量间接制取的能源称为二次能源)。在人类生存的地球上,几乎没有现成的氢,因此必须将含氢物质加工后方能得到氢气。最丰富的含物质是水,其次就是各种矿物燃料(煤、石油、天然气、硫化氢)及各种生物质等。
美国拉斯阿拉莫斯实验室最先提出了一种零排放的煤制氢技术,其主要流程如图所示:
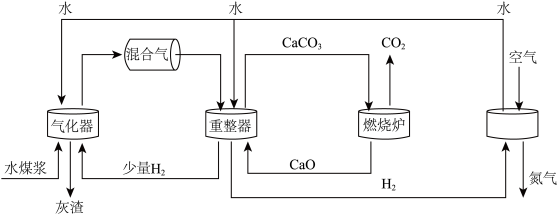
该系统输入煤和水,产生电能和热,整个制氢过程几乎不产生污染物,达到近零排放的目的。
氢是宇宙中最丰富的元素。构成宇宙的物质的元素中,氢大约占据宇宙质量的75%。地球之母——太阳,就是依靠氢的同位素氘和氚的聚合反应生成巨量的热和光,温暖着地球,照耀着地球。使用氢作为能源,就是回归宇宙法则,“替天行道”。
(1)下列能源中属于二次能源的是(填字母序号)______ 。
(2)如图气化器中发生的主要反应有:C+H2O CO+H2,CO+H2O
CO+H2,CO+H2O CO2+H2。向重整器中加入CaO的作用是
CO2+H2。向重整器中加入CaO的作用是______ ;煅烧炉中发生反应的化学方程式为______ 。
(3)如图流程中可以循环利用的物质有______ (填字母序号)。
(4)氚可用于核能发电,氚是一种原子核中有1个质子和2个中子的原子。下列示意图能表示氚原子的是______ (填序号)。
(5)化学上把具有相同质子数和不同中子数的同一元素的不同原子互称同位素。氘和氚是核聚变的原料,已知氘、氚原子核内都只有1个质子,但含不同数目的中子。根据以上叙述,下列说法正确的是______ 。
科技助力氢能
化石能源是当今世界能源市场的支柱和世界经济发展的动力。然而化石燃料的广泛使用,对全球环境造成了很大威胁。化石能源是一种有限的资源,而且存在明显的地理分布不均匀性。现在,世界能源结构正在发生第三次革命,从以化石燃料为主的能源系统转向可再生能源、氢能等多元化结构。环境要求是本次能源革命的主要动因。氢能是一种二次能源(自然界中以现成形式提供的能源称为一次能源,需要依靠其他能源的能量间接制取的能源称为二次能源)。在人类生存的地球上,几乎没有现成的氢,因此必须将含氢物质加工后方能得到氢气。最丰富的含物质是水,其次就是各种矿物燃料(煤、石油、天然气、硫化氢)及各种生物质等。
美国拉斯阿拉莫斯实验室最先提出了一种零排放的煤制氢技术,其主要流程如图所示:

该系统输入煤和水,产生电能和热,整个制氢过程几乎不产生污染物,达到近零排放的目的。
氢是宇宙中最丰富的元素。构成宇宙的物质的元素中,氢大约占据宇宙质量的75%。地球之母——太阳,就是依靠氢的同位素氘和氚的聚合反应生成巨量的热和光,温暖着地球,照耀着地球。使用氢作为能源,就是回归宇宙法则,“替天行道”。
(1)下列能源中属于二次能源的是(填字母序号)
| A.煤 | B.汽油 | C.天然气 |
(2)如图气化器中发生的主要反应有:C+H2O
 CO+H2,CO+H2O
CO+H2,CO+H2O CO2+H2。向重整器中加入CaO的作用是
CO2+H2。向重整器中加入CaO的作用是(3)如图流程中可以循环利用的物质有
| A.CaO | B.H2O | C.H2 |
(4)氚可用于核能发电,氚是一种原子核中有1个质子和2个中子的原子。下列示意图能表示氚原子的是
A.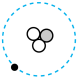 | B.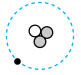 | C.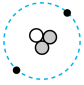 | D. |
(5)化学上把具有相同质子数和不同中子数的同一元素的不同原子互称同位素。氘和氚是核聚变的原料,已知氘、氚原子核内都只有1个质子,但含不同数目的中子。根据以上叙述,下列说法正确的是
| A.氘原子和氚原子是氢的不同元素 |
| B.氘原子和氚原子是氢的两种同位素 |
| C.氘原子和氚原子的相对原子质量相同 |
您最近一年使用:0次
7 . 好茶看茶叶。茶叶中含有多种成分。
(1)茶叶含氟较高,对预防龋齿有一定效果。这里的“氟”指的是___________ (填“元素”或“单质”)。
(2)茶叶中的硒有防癌作用。硒原子结构示意图如图所示,x=___________ ,硒元素在化学反应中易___________ (填“得到”或“失去”)电子。

(3)茶叶中的茶多酚具有强血管降血脂的作用。某种茶多酚的化学式为C6H6O2,其氢、氧元素的质量比为___________ 。
(1)茶叶含氟较高,对预防龋齿有一定效果。这里的“氟”指的是
(2)茶叶中的硒有防癌作用。硒原子结构示意图如图所示,x=

(3)茶叶中的茶多酚具有强血管降血脂的作用。某种茶多酚的化学式为C6H6O2,其氢、氧元素的质量比为
您最近一年使用:0次
解题方法
8 . 模型认知是建立宏观与微观联系的思维方法。
(1)“人造太阳”合理利用了可控核聚变,氘、氚是核聚变的热核材料。
①氘和氚属于___________ (选填“同种”或“不同种")元素,上表中x=___________ 。
②贮存氘气的钢瓶禁止掌近明火,据此推测氘气具有的化学性质是___________ 。
③超重水有一定的放射性,一个超重水分子是由两个氚原子和一个氧原子构成,其化学式可表示为T2O,该分子的相对分子质量为___________ 。
(2)据报道,我国科学家研制出以石墨烯为载体的催化剂,在25℃下将CH4转化为甲醇(CH3OH)、甲醛(CH2O)等,主要原理如图所示:

①中“ ”表示
”表示__________ (填微粒名称)。
②步骤i、ii的总反应化学方程式是___________ 。
③这一系列的催化反应中(不考虑催化剂),没有发生变化的粒子是___________ 。
④步骤vi与步骤ii反应类似,试推步骤vi的产物是__________ (填“化学式”)和H2O。
(1)“人造太阳”合理利用了可控核聚变,氘、氚是核聚变的热核材料。
| 原子种类 | 质子数 | 中子数 | 核外电子数 |
| 氘 | 1 | 1 | 1 |
| 氚 | 1 | 2 | x |
②贮存氘气的钢瓶禁止掌近明火,据此推测氘气具有的化学性质是
③超重水有一定的放射性,一个超重水分子是由两个氚原子和一个氧原子构成,其化学式可表示为T2O,该分子的相对分子质量为
(2)据报道,我国科学家研制出以石墨烯为载体的催化剂,在25℃下将CH4转化为甲醇(CH3OH)、甲醛(CH2O)等,主要原理如图所示:

①中“
 ”表示
”表示②步骤i、ii的总反应化学方程式是
③这一系列的催化反应中(不考虑催化剂),没有发生变化的粒子是
④步骤vi与步骤ii反应类似,试推步骤vi的产物是
您最近一年使用:0次
解题方法
9 . 请分别用“大于”“小于”或“等于”填空。
(1)核外电子数:镁离子______ 氖原子。
(2)质子数:镁离子______ 水分子。
(3)碳元素的质量分数:甲酸(HCOOH)______ 醋酸(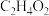 )。
)。
(4)50mL无水酒精和50mL蒸馏水充分混合后所得溶液的体积______ 100mL。
(1)核外电子数:镁离子
(2)质子数:镁离子
(3)碳元素的质量分数:甲酸(HCOOH)
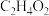 )。
)。(4)50mL无水酒精和50mL蒸馏水充分混合后所得溶液的体积
您最近一年使用:0次
解题方法
10 . “化学观念”是一种化学学科素养。
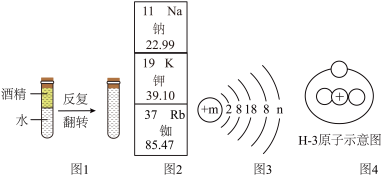
(1)观察如图1实验,回答:水与酒精混合后,总体积______ 30mL(填“>”“=”或“<”)。该实验说明______ 。
(2)“天宫二号”使用的冷原子钟精度居于世界最高,三千万年误差小于1秒,制作该冷原子钟应用了铷原子。图2为元素周期表部分信息,图3为铷原子结构示意图。
①铷的相对原子质量为85.47,m=______ 。
②铷元素与钠元素的化学性质______ (填“相似”或“不相似”)。它们的原子在化学反应中都比较容易______ (填“得到”或“失去”)电子形成稳定结构。
(3)日本向海洋倾倒被福岛H—3核污染的废水,将长期严重污染太平洋,威胁生命安全,H—3是一种核内含有2个中子的具有放射性的氢原子。如图4所示。下列有关说法不正确的是 (填字母)。

(1)观察如图1实验,回答:水与酒精混合后,总体积
(2)“天宫二号”使用的冷原子钟精度居于世界最高,三千万年误差小于1秒,制作该冷原子钟应用了铷原子。图2为元素周期表部分信息,图3为铷原子结构示意图。
①铷的相对原子质量为85.47,m=
②铷元素与钠元素的化学性质
(3)日本向海洋倾倒被福岛H—3核污染的废水,将长期严重污染太平洋,威胁生命安全,H—3是一种核内含有2个中子的具有放射性的氢原子。如图4所示。下列有关说法不正确的是 (填字母)。
| A.H-3、H-2与H-1(即普通氢原子)都属于氢元素 |
| B.H-3与普通氢原子相比,原子核外都有1个电子,但含有不同的中子数 |
| C.H-3的相对原子质量为2 |
您最近一年使用:0次