解题方法
1 . 在宏观、微观和符号之间建立联系是学习化学的重要思维方式。
(1)从宏观角度分析,氧气是由氧________ (填“元素”或“原子”)组成的。
(2)中国科学院院士张青莲教授于1983年当选为国际原子量委员会委员,他主持测定了多种元素相对原子质量的新值,其中相对原子质量确定为152的铕元素的原子序数为63,则铕原子的核外电子数为_______ 。
(3)根据下列粒子的结构示意图,回答下列问题:_____ (填数字)种。
②与氧元素具有相似化学性质的是_____ (填元素符号)。
③由镁和氯两种元素组成化合物的化学式为__________ 。
(4)氦气是由_______ (填“分子、原子、离子”)构成,二氧化碳是由_______ (填“分子、原子、离子”)构成,氯化钠是由_______ (填“分子、原子、离子”)构成。
(1)从宏观角度分析,氧气是由氧
(2)中国科学院院士张青莲教授于1983年当选为国际原子量委员会委员,他主持测定了多种元素相对原子质量的新值,其中相对原子质量确定为152的铕元素的原子序数为63,则铕原子的核外电子数为
(3)根据下列粒子的结构示意图,回答下列问题:

②与氧元素具有相似化学性质的是
③由镁和氯两种元素组成化合物的化学式为
(4)氦气是由
您最近一年使用:0次
解题方法
2 . 阅读材料,回答相关问题。
钠元素在自然界中分布很广,常以氯化钠、碳酸钠、硫酸钠等物质存在。
钠是一种银白色金属,质软。金属钠的性质很活泼,能与许多物质发生化学反应。钠暴露在空气中,与氧气反应生成氧化钠( );钠遇水立即发生剧烈反应,生成氢氧化钠和氢气。因此,实验室常将钠保存在煤油中。金属钠的用途广泛。钠和钾形成的合金熔点低,常温下呈液态,可用作快中子反应堆的热交换剂。利用钠的强还原性,在一定条件下可以将钛(Ti)、锆(Zr)等稀有金属从其氯化物中置换出来。
);钠遇水立即发生剧烈反应,生成氢氧化钠和氢气。因此,实验室常将钠保存在煤油中。金属钠的用途广泛。钠和钾形成的合金熔点低,常温下呈液态,可用作快中子反应堆的热交换剂。利用钠的强还原性,在一定条件下可以将钛(Ti)、锆(Zr)等稀有金属从其氯化物中置换出来。
(1)自然界中钠元素以___________ (填“单质”或“化合物”)形式存在;金属钠应保存在___________ 中。
(2)氧化钠中的阳离子为 ,1个
,1个 中含有的电子数为
中含有的电子数为___________ 。
(3)钠钾合金可用作热交换剂,由此推测钠钾合金具有良好的___________ 性。
(4)写出钠暴露在空气中与氧气反应的化学方程式:___________ 。
钠元素在自然界中分布很广,常以氯化钠、碳酸钠、硫酸钠等物质存在。
钠是一种银白色金属,质软。金属钠的性质很活泼,能与许多物质发生化学反应。钠暴露在空气中,与氧气反应生成氧化钠(
 );钠遇水立即发生剧烈反应,生成氢氧化钠和氢气。因此,实验室常将钠保存在煤油中。金属钠的用途广泛。钠和钾形成的合金熔点低,常温下呈液态,可用作快中子反应堆的热交换剂。利用钠的强还原性,在一定条件下可以将钛(Ti)、锆(Zr)等稀有金属从其氯化物中置换出来。
);钠遇水立即发生剧烈反应,生成氢氧化钠和氢气。因此,实验室常将钠保存在煤油中。金属钠的用途广泛。钠和钾形成的合金熔点低,常温下呈液态,可用作快中子反应堆的热交换剂。利用钠的强还原性,在一定条件下可以将钛(Ti)、锆(Zr)等稀有金属从其氯化物中置换出来。(1)自然界中钠元素以
(2)氧化钠中的阳离子为
 ,1个
,1个 中含有的电子数为
中含有的电子数为(3)钠钾合金可用作热交换剂,由此推测钠钾合金具有良好的
(4)写出钠暴露在空气中与氧气反应的化学方程式:
您最近一年使用:0次
解题方法
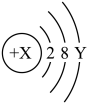
3 . 如图是某粒子的结构示意图,回答下列问题:______ ;
(2)若该粒子为原子,当X=12时,Y=______ ;
(3)若该粒子带1个单位负电荷,当X=17时,则Y=______ 。
(2)若该粒子为原子,当X=12时,Y=
(3)若该粒子带1个单位负电荷,当X=17时,则Y=
您最近一年使用:0次
解题方法
4 . 请回答下列问题。
(1)已知碳-12原子的质量是mkg,A原子的质量是akg,若A原子核内中子数比质子数多1,求:
①A原子的相对原子质量_______ 。
②A原子的核外电子数_______ 。
(2)已知某粒子符号为Rm+,其核外电子数为n,则其质子数为_______ 。
(3)已知相对原子质量:Na:23、Mg:24、Al:27。比较相同质量的钠、镁、铝三种金属,所含原子个数最多的是_______ ,所含原子个数最少的是_______ 。(填符号)
(1)已知碳-12原子的质量是mkg,A原子的质量是akg,若A原子核内中子数比质子数多1,求:
①A原子的相对原子质量
②A原子的核外电子数
(2)已知某粒子符号为Rm+,其核外电子数为n,则其质子数为
(3)已知相对原子质量:Na:23、Mg:24、Al:27。比较相同质量的钠、镁、铝三种金属,所含原子个数最多的是
您最近一年使用:0次
5 . 元素周期表是学习和研究化学的重要工具,下图是元素周期表的一部分,按要求回答问题:
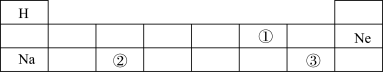
(1)元素②的原子内质子数是___________ ;
(2)元素③的原子在化学反应中容易___________ (填“得到”或“失去”)电子。
(3)人体中含量最多的金属元素是___________ (填符号)。

(1)元素②的原子内质子数是
(2)元素③的原子在化学反应中容易
(3)人体中含量最多的金属元素是
您最近一年使用:0次
解题方法
6 . 在宏观、微观与符号之间建立联系,是化学学科的特点。
(1)元素、物质、微粒三者之间的关系如图所示。
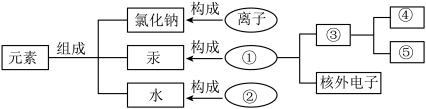
①应填______ ;
②应填______ ;
③应填______ ;
④为带正电荷的粒子,应填______ 。
(2)请根据下列元素的信息和原子结构示意图,回答问题。
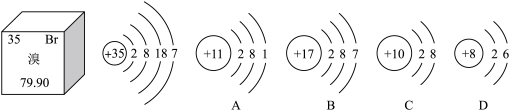
①溴的核电荷数为______ ;溴元素位于第______ 周期。
②A、B、C、D四种元素中,化学性质最稳定的是______ (填元素符号)。
③A、B、C、D四种元素中,与溴化学性质相似的是______ (填字母)。
(3)硒被医药界和营养学界尊称为“生命的火种”,享有“长寿元素”、“抗癌之王”、“心脏守护神”、“天然解毒剂”等美誉。如图为硒在元素周期表中的相关信息及原子结构示意图,请回答下列问题:
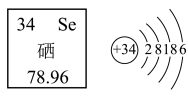
①硒元素属于______ (填“金属”或“非金属”)元素,该元素原子的中子数为______ ,其中78.96表示的是______ 。
②硒原子在化学反应中容易______ (填“得到”或“失去”)电子形成______ (写出离子符号),该性质由______ 决定。
③已知一个C-12原子(质子数为6,中子数为6)的实际质量是ag,那么一个硒原子的实际质量是(用带a的式子表示)______ g。
(1)元素、物质、微粒三者之间的关系如图所示。

①应填
②应填
③应填
④为带正电荷的粒子,应填
(2)请根据下列元素的信息和原子结构示意图,回答问题。

①溴的核电荷数为
②A、B、C、D四种元素中,化学性质最稳定的是
③A、B、C、D四种元素中,与溴化学性质相似的是
(3)硒被医药界和营养学界尊称为“生命的火种”,享有“长寿元素”、“抗癌之王”、“心脏守护神”、“天然解毒剂”等美誉。如图为硒在元素周期表中的相关信息及原子结构示意图,请回答下列问题:

①硒元素属于
②硒原子在化学反应中容易
③已知一个C-12原子(质子数为6,中子数为6)的实际质量是ag,那么一个硒原子的实际质量是(用带a的式子表示)
您最近一年使用:0次
解题方法
7 . 在宏观、微观和符号之间建立联系是化学特有的思维方式。
(1)月球上存在丰富的氦-3,已知氦-3原子的相对原子质量是3,下图能正确表示氦-3原子的结构模型图的是___________ (填字母)。

(2)如图甲是氟元素的部分信息,如图乙是A~E五种粒子的结构示意图。
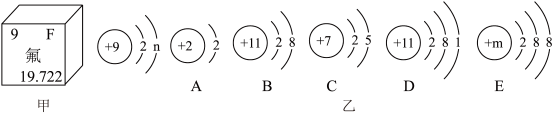
①氟元素是人体必须的微量元素,从甲图可知,氟元素的相对原子质量是___________ ,氟原子的结构示意图中n的值是___________ 。
②A~D四种粒子中属于同种元素的是___________ (填序号,下同),具有相对稳定结构的原子是___________ 。
③若E为某原子得到一个电子形成的离子,则m的数值是___________ 。
④C粒子在化学反应中容易___________ (填“得到”或“失去”)电子而形成离子,它与B相互作用形成化合物的化学式是___________ 。
(1)月球上存在丰富的氦-3,已知氦-3原子的相对原子质量是3,下图能正确表示氦-3原子的结构模型图的是

(2)如图甲是氟元素的部分信息,如图乙是A~E五种粒子的结构示意图。

①氟元素是人体必须的微量元素,从甲图可知,氟元素的相对原子质量是
②A~D四种粒子中属于同种元素的是
③若E为某原子得到一个电子形成的离子,则m的数值是
④C粒子在化学反应中容易
您最近一年使用:0次
解题方法
8 . 在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
(1)元素周期表中原子序数为101的元素被命名为“钔”(元素符号为Md),用来纪念门捷列夫编制元素周期表所作出的巨大贡献。钔的相对原子质量为258,则钔原子的质子数为___________ 。
(2)根据下列粒子的结构示意图,回答问题。
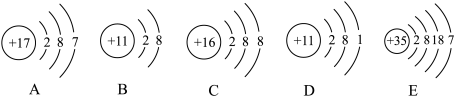
①图中粒子共表示___________ 种元素。
②与A的化学性质最相似的是___________ (填字母)。
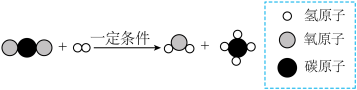
(3)为减少CO2的排放,可将CO2进行转化。图中反应的化学方程式为___________ 。
(1)元素周期表中原子序数为101的元素被命名为“钔”(元素符号为Md),用来纪念门捷列夫编制元素周期表所作出的巨大贡献。钔的相对原子质量为258,则钔原子的质子数为
(2)根据下列粒子的结构示意图,回答问题。

①图中粒子共表示
②与A的化学性质最相似的是
(3)为减少CO2的排放,可将CO2进行转化。图中反应的化学方程式为

您最近一年使用:0次
名校
解题方法
9 . 阅读下列短文,回答相关问题。
氢能是一种二次能源(自然界中以现成形式提供的能源称为一次能源,需要依靠其他能源的能量间接制取的能源称为二次能源)。在人类生存的地球上,几乎没有现成的氢,因此必须将含氢物质加工后方能得到氢气。最丰富的含物质是水,其次就是各种矿物燃料(煤、石油、天然气、硫化氢)及各种生物质等。
美国拉斯阿拉莫斯实验室最先提出了一种零排放的煤制氢技术,其主要流程如图所示:
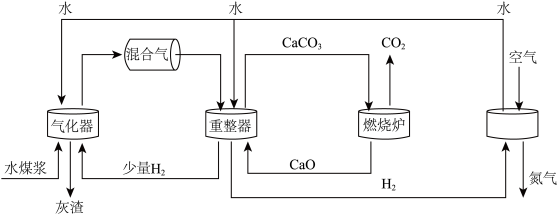
该系统输入煤和水,产生电能和热,整个制氢过程几乎不产生污染物,达到近零排放的目的。
氢是宇宙中最丰富的元素。构成宇宙的物质的元素中,氢大约占据宇宙质量的75%。地球之母——太阳,就是依靠氢的同位素氘和氚的聚合反应生成巨量的热和光,温暖着地球,照耀着地球。使用氢作为能源,就是回归宇宙法则,“替天行道”。
(1)下列能源中属于二次能源的是(填字母序号)______ 。
(2)如图气化器中发生的主要反应有:C+H2O CO+H2,CO+H2O
CO+H2,CO+H2O CO2+H2。向重整器中加入CaO的作用是
CO2+H2。向重整器中加入CaO的作用是______ ;煅烧炉中发生反应的化学方程式为______ 。
(3)如图流程中可以循环利用的物质有______ (填字母序号)。
(4)氚可用于核能发电,氚是一种原子核中有1个质子和2个中子的原子。下列示意图能表示氚原子的是______ (填序号)。
(5)化学上把具有相同质子数和不同中子数的同一元素的不同原子互称同位素。氘和氚是核聚变的原料,已知氘、氚原子核内都只有1个质子,但含不同数目的中子。根据以上叙述,下列说法正确的是______ 。
科技助力氢能
化石能源是当今世界能源市场的支柱和世界经济发展的动力。然而化石燃料的广泛使用,对全球环境造成了很大威胁。化石能源是一种有限的资源,而且存在明显的地理分布不均匀性。现在,世界能源结构正在发生第三次革命,从以化石燃料为主的能源系统转向可再生能源、氢能等多元化结构。环境要求是本次能源革命的主要动因。氢能是一种二次能源(自然界中以现成形式提供的能源称为一次能源,需要依靠其他能源的能量间接制取的能源称为二次能源)。在人类生存的地球上,几乎没有现成的氢,因此必须将含氢物质加工后方能得到氢气。最丰富的含物质是水,其次就是各种矿物燃料(煤、石油、天然气、硫化氢)及各种生物质等。
美国拉斯阿拉莫斯实验室最先提出了一种零排放的煤制氢技术,其主要流程如图所示:

该系统输入煤和水,产生电能和热,整个制氢过程几乎不产生污染物,达到近零排放的目的。
氢是宇宙中最丰富的元素。构成宇宙的物质的元素中,氢大约占据宇宙质量的75%。地球之母——太阳,就是依靠氢的同位素氘和氚的聚合反应生成巨量的热和光,温暖着地球,照耀着地球。使用氢作为能源,就是回归宇宙法则,“替天行道”。
(1)下列能源中属于二次能源的是(填字母序号)
| A.煤 | B.汽油 | C.天然气 |
(2)如图气化器中发生的主要反应有:C+H2O
 CO+H2,CO+H2O
CO+H2,CO+H2O CO2+H2。向重整器中加入CaO的作用是
CO2+H2。向重整器中加入CaO的作用是(3)如图流程中可以循环利用的物质有
| A.CaO | B.H2O | C.H2 |
(4)氚可用于核能发电,氚是一种原子核中有1个质子和2个中子的原子。下列示意图能表示氚原子的是
A.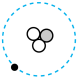 | B.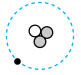 | C.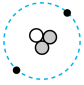 | D. |
(5)化学上把具有相同质子数和不同中子数的同一元素的不同原子互称同位素。氘和氚是核聚变的原料,已知氘、氚原子核内都只有1个质子,但含不同数目的中子。根据以上叙述,下列说法正确的是
| A.氘原子和氚原子是氢的不同元素 |
| B.氘原子和氚原子是氢的两种同位素 |
| C.氘原子和氚原子的相对原子质量相同 |
您最近一年使用:0次
解题方法
10 . 2023年10月26日,神舟十七号载人飞船成功发射,这是镉镍蓄电池在中国航天器领域的“收官之战”。如图是镍元素在元素周期表中的信息和原子结构示意图,x=______ ,镍元素在元素周期表中位于第______ 周期,其相对原子质量为______ 。


您最近一年使用:0次
2024-02-23更新
|
28次组卷
|
2卷引用:河南省郑州市新郑市2023-2024学年九年级上学期1月期末化学试题



