名校
解题方法
1 . 某Na2CO3样品混有少量的Na2SO4,为测定该样品中Na2CO3的含量,进行以下实验:取一定量该样品,加入水中溶解得到100g溶液,然后加入98g一定质量分数的稀硫酸,恰好完全反应,得到溶液195.8g。蒸干溶液后得到固体7.6g(不考虑气体的溶解)。
已知相对分子质量:Na2CO3:106 H2SO4:98 Na2SO4:142 CO2:44
(1)Na2CO3和Na2SO4中钠元素的质量分数较大的是______ 。
(2)稀硫酸的溶质质量分数为______ 。
(3)样品中Na2CO3的质量分数(计算结果精确到0.1%)。
已知相对分子质量:Na2CO3:106 H2SO4:98 Na2SO4:142 CO2:44
(1)Na2CO3和Na2SO4中钠元素的质量分数较大的是
(2)稀硫酸的溶质质量分数为
(3)样品中Na2CO3的质量分数(计算结果精确到0.1%)。
您最近一年使用:0次
解题方法
2 . 用于识别考生信息的条形码背面的胶黏剂成分主要为丙烯酸(C3H4O2)。下列有关说法正确的是
| A.丙烯酸中含有两个水分子 |
| B.丙烯酸中碳元素的质量分数最大 |
| C.丙烯酸分子是由碳元素、氢元素、氧元素组成的 |
| D.丙烯酸由3个碳原子、4个氢原子和2个氧原子构成 |
您最近一年使用:0次
3 . 以石灰石为原料制得的碳酸钙应用十分广泛。
(1)日常生活中使用的牙膏里面都含有一定量的摩擦剂(主要成分碳酸钙),根据你的推测,摩擦剂应具备下列性质中的___________(填字母)。
(2)甲同学设计的实验方案为:

乙同学设计的实验方案为:
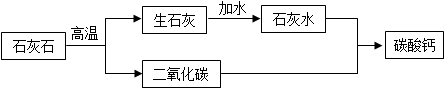
①你认为甲、乙两位同学谁的实验方案更好,理由是___________ 。
②甲同学向氯化钙中加入足量5.3%的碳酸钠溶液,产生沉淀的质量与滴入碳酸钠溶液的质量关系如图1所示。试计算反应所得碳酸钙的质量___________ (写出计算过程)。

(3)碳酸钙是常见的补钙剂,某钙片标签如图2所示,若药品中的钙元素完全来自碳酸钙,则此钙片中碳酸钙的质量分数为___________ 。
(1)日常生活中使用的牙膏里面都含有一定量的摩擦剂(主要成分碳酸钙),根据你的推测,摩擦剂应具备下列性质中的___________(填字母)。
| A.易溶于水 | B.难溶于水 | C.坚硬 | D.柔软 | E.颗粒较大 | F.颗粒较小 |

乙同学设计的实验方案为:

①你认为甲、乙两位同学谁的实验方案更好,理由是
②甲同学向氯化钙中加入足量5.3%的碳酸钠溶液,产生沉淀的质量与滴入碳酸钠溶液的质量关系如图1所示。试计算反应所得碳酸钙的质量

(3)碳酸钙是常见的补钙剂,某钙片标签如图2所示,若药品中的钙元素完全来自碳酸钙,则此钙片中碳酸钙的质量分数为
您最近一年使用:0次
解题方法
4 . 氧化锌广泛地应用于塑料、合成橡胶、药膏等产品的制作中。
Ⅰ.氧化锌的制备利用氧化锌矿(含少量CuO、NiO)为原料制备高纯氧化锌的流程如下:
②碳酸氢铵1000元/吨,碳酸钠2650元/吨。
(1)“酸溶”步骤中发生反应的化学方程式有_______ 。_______ 。
(3)“酸溶”后溶液中含有的阳离子有Zn2+、Ni2+、_______ 。
(4)“过滤I”所得滤渣中所含的金属有_______ (填化学式)。
(5)“反应”可加入碳酸钠制备碱式碳酸锌,反应原理为:3Na2CO3+3ZnSO4+3H2O=ZnCO3·2Zn(OH)2·H2O↓+3Na2SO4+2CO2↑。亦可采用新工艺,即选用碳酸氢铵来代替碳酸钠制备碱式碳酸锌,反应原理为6NH4HCO3+3ZnSO4=ZnCO3·2Zn(OH)2·H2O↓+3(NH4)2SO4+5CO2↑。
①选用碳酸氢铵来代替碳酸钠制备碱式碳酸锌的优点是_______ 。
②新工艺常控制在40°C条件下进行,其目的是_______ 、_______ 。
Ⅱ.氧化锌的应用炉甘石始栽于《外丹本草》,主要成分为碳酸锌(ZnCO3)和碱式碳酸锌,炮制后主要成分为氧化锋(ZnO),可添加至药膏用作外用药。
(6)炉甘石“炮制”的工艺方式(反应条件)是_______ 。
(7)氧化锌、碳酸锌、碱式碳酸锌都有一定的抑菌活性,说明起抑菌作用的有效成分可能是锌_______ (选填“单质”或“元素”)。
(8)药效高低与有效成分的含量相关。碳酸锌的抑菌活性低于相同质量的氧化锌,可能的原因是_______ 。
Ⅰ.氧化锌的制备利用氧化锌矿(含少量CuO、NiO)为原料制备高纯氧化锌的流程如下:
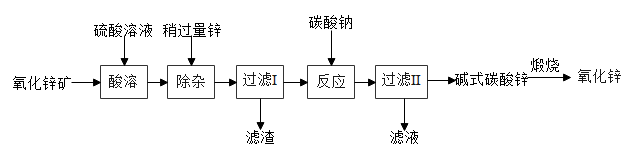
②碳酸氢铵1000元/吨,碳酸钠2650元/吨。
(1)“酸溶”步骤中发生反应的化学方程式有
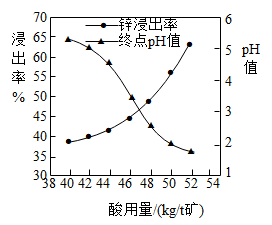
(3)“酸溶”后溶液中含有的阳离子有Zn2+、Ni2+、
(4)“过滤I”所得滤渣中所含的金属有
(5)“反应”可加入碳酸钠制备碱式碳酸锌,反应原理为:3Na2CO3+3ZnSO4+3H2O=ZnCO3·2Zn(OH)2·H2O↓+3Na2SO4+2CO2↑。亦可采用新工艺,即选用碳酸氢铵来代替碳酸钠制备碱式碳酸锌,反应原理为6NH4HCO3+3ZnSO4=ZnCO3·2Zn(OH)2·H2O↓+3(NH4)2SO4+5CO2↑。
①选用碳酸氢铵来代替碳酸钠制备碱式碳酸锌的优点是
②新工艺常控制在40°C条件下进行,其目的是
Ⅱ.氧化锌的应用炉甘石始栽于《外丹本草》,主要成分为碳酸锌(ZnCO3)和碱式碳酸锌,炮制后主要成分为氧化锋(ZnO),可添加至药膏用作外用药。
(6)炉甘石“炮制”的工艺方式(反应条件)是
(7)氧化锌、碳酸锌、碱式碳酸锌都有一定的抑菌活性,说明起抑菌作用的有效成分可能是锌
(8)药效高低与有效成分的含量相关。碳酸锌的抑菌活性低于相同质量的氧化锌,可能的原因是
您最近一年使用:0次
解题方法
5 . 河南特产大枣富含维生素C(化学式为C6H8O6)。下列有关维生素C的说法中正确的是
| A.维生素C是氧化物 | B.维生素C燃烧可能生成一氧化碳 |
| C.维生素C中含有3个氧分子 | D.维生素C中氢元素的质量分数最大 |
您最近一年使用:0次
名校
解题方法
6 . 中国科学家研制的具有自主知识产权的新型抗癌药——西达本胺(化学式为C22H19FN4O2)挽收了无数病人的生命。下列有关说法正确的是
| A.西达本胺由五种元素组成,属于氧化物 |
| B.西达本胺中氢、氧元素的质量比为19:2 |
| C.西达本胺中碳元素的质量分数最大 |
| D.一个西达本胺分子中含有一个氧分子 |
您最近一年使用:0次
2023-05-01更新
|
179次组卷
|
4卷引用:2023年广东省深圳市中考化学真题变式题(选择题1~6)
(已下线)2023年广东省深圳市中考化学真题变式题(选择题1~6)广东省深圳市南山外国语学校2022-2023学年九年级下学期四月月考化学试题2023年4月广东省深圳市南山第二外国语学校中考二模化学试题2023年安徽省淮南市寿县广岩初级中学中考模拟化学试题20
解题方法
7 . 木糖醇(C5H12O5)是一种甜味剂。按要求计算:
(1)木糖醇分子中C、H、O原子个数比为______ ;
(2)木糖醇中碳元素和氢元素的质量比为______ (写最简比);
(3)木糖醇的相对分子质量为______ ;
(4)152 g的木糖醇中含有氧元素的质量为______ g。
(1)木糖醇分子中C、H、O原子个数比为
(2)木糖醇中碳元素和氢元素的质量比为
(3)木糖醇的相对分子质量为
(4)152 g的木糖醇中含有氧元素的质量为
您最近一年使用:0次
解题方法
8 . 能源利用和环境保护是人类共同关注的问题。
(1)目前,人们利用最多的能源是______ 、石油和天然气等化石燃料。
(2)写出甲烷在空气中充分燃烧的化学方程式______ 。
(3)下列叙述正确的是______(填字母序号)。
(4)将23 g乙醇与一定量氧气在密闭容器中点燃,在一定条件下充分反应,生成一氧化碳、二氧化碳和水。恢复到室温,测得一氧化碳和二氧化碳混合气体中氧元素质量分数为70%,则燃烧生成水的质量为______ g;一氧化碳和二氧化碳的质量比为______ 。
(1)目前,人们利用最多的能源是
(2)写出甲烷在空气中充分燃烧的化学方程式
(3)下列叙述正确的是______(填字母序号)。
| A.化学反应伴随着能量变化 |
| B.化学反应过程中都会发生放热的现象 |
| C.人类利用的能源都是通过化学反应获得的 |
您最近一年使用:0次
解题方法
9 . 在SO3+H2O=H2SO4的反应中,下列说法不正确 的是
| A.SO3可与碱反应 |
| B.该反应为化合反应 |
| C.SO3中S元素的质量分数为40% |
| D.参加反应的SO3和H2O的质量比为5∶1 |
您最近一年使用:0次
解题方法
10 . 等物质的量的SO2、CO2具有相同的
| A.质量 | B.氧原子个数 |
| C.氧元素的质量分数 | D.分子个数 |
您最近一年使用:0次



