解题方法
1 . 中和反应在工农业生产中有广泛的应用。某工厂化验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40g,洗涤后的溶液呈中性。
(1)再列举一例中和反应在实际中的应用_______ 。
(2)这一定量的石油产品中含H2SO4的质量是多少?
(1)再列举一例中和反应在实际中的应用
(2)这一定量的石油产品中含H2SO4的质量是多少?
您最近一年使用:0次
名校
解题方法
2 . 酸、碱、盐是几类重要化合物,与人类日常生产生活关系十分密切。
(1)实验室中,氢氧化钠可用于干燥气体,原因是氢氧化钠具有___________ 性。下列气体不能用氢氧化钠干燥的是___________ (填标号)。
A.O2 B.CO2 C.H2 D.N2
(2)农业上可用石灰乳与硫酸铜等配制具有杀菌作用的波尔多液作为农药使用,石灰乳的有效成分是___________ (填化学式)。
(3)下图是稀硝酸滴入氢氧化钾溶液中恰好完全反应的微观示意图,反应前后不变的离子有 和
和___________ (填离子符号)。___________ 。
(5)某溶液中的溶质可能是HCl、H2SO4、Na2CO3、MgCl2中的一种或多种。为探究溶质成分,小迪同学向一定量该溶液中逐滴加入Ba(OH)2溶液,如图表示加入Ba(OH)2溶液的质量与产生沉淀和另一种物质的质量变化关系。___________ ;
②a表示的物质是___________ 。
(1)实验室中,氢氧化钠可用于干燥气体,原因是氢氧化钠具有
A.O2 B.CO2 C.H2 D.N2
(2)农业上可用石灰乳与硫酸铜等配制具有杀菌作用的波尔多液作为农药使用,石灰乳的有效成分是
(3)下图是稀硝酸滴入氢氧化钾溶液中恰好完全反应的微观示意图,反应前后不变的离子有
 和
和
(5)某溶液中的溶质可能是HCl、H2SO4、Na2CO3、MgCl2中的一种或多种。为探究溶质成分,小迪同学向一定量该溶液中逐滴加入Ba(OH)2溶液,如图表示加入Ba(OH)2溶液的质量与产生沉淀和另一种物质的质量变化关系。

②a表示的物质是
您最近一年使用:0次
解题方法
3 . 氢氧化钠是实验室常用的化学试剂。下列关于氢氧化钠的描述中正确的是
| A.露置在空气中易潮解 | B.能与CO2发生复分解反应 |
| C.常用于中和酸性土壤 | D.氢氧化钠固体溶于水吸热 |
您最近一年使用:0次
解题方法
4 . 物质的用途是由性质决定。下列物质的性质与用途相对应的是
| A.氢气具有还原性,可以制氢气球 | B.氢氧化铝能与酸反应,可以中和胃酸 |
| C.浓盐酸具有挥发性,可用于金属除锈 | D.石墨具有导电性,可用于制作铅笔芯 |
您最近一年使用:0次
名校
解题方法
5 . 如表为一些食物的近似pH,胃酸过多的人空腹时最适宜吃的食物是
| 食物 | ①苹果 | ②橘子 | ③牛奶 | ④玉米粥 |
| pH | 2.9~3.3 | 3.0~4.0 | 6.3~6.6 | 6.8~8.0 |
| A.① | B.④ | C.①④ | D.①②③ |
您最近一年使用:0次
解题方法
6 . 下列化学方程式中符合题意且书写正确的是
A.酸雨形成的原因: 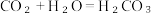 |
B.用稀硫酸除铁锈:  |
C.用铜和稀硫酸制硫酸铜:  |
D.用氢氧化镁治疗胃酸过多症:  |
您最近一年使用:0次
2024-06-14更新
|
51次组卷
|
3卷引用:2024年河南省周口市沈丘县2校中考二模化学试题
解题方法
7 . 学习化学让我们知道,物质的性质决定其用途。下列关于物质的性质与用途关联错误的是
| 选项 | 物质 | 性质 | 用途 |
| A | 明矾 | 能与水生成胶状物 | 吸附水中悬浮颗粒物发生沉降 |
| B | 金刚石 | 硬度大 | 作钻探机的钻头 |
| C | 干冰 | 升华吸热 | 作制冷剂 |
| D | 烧碱 | 易溶于水且水溶液呈碱性 | 改良酸性土壤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 某研究小组对家用除湿袋产生浓厚的兴趣,在化学老师指导下进行项目化研究。
项目一:探究家用除湿袋中的物质成分
【资料信息】
吸湿区内白色颗粒是初中化学常见物质。使用一段时间后,集水袋内有大量液体和少量固体,且气温越低固体越多。
【提出问题】白色颗粒是什么物质?
(1)据所学知识进行作出猜想。猜想I:氧化钙,依据:______ (用化学方程式表示);猜想II:氢氧化钠固体,依据:______ 。
【进行实验】
步骤1:取8g白色颗粒于烧杯A中,加入10mL的20℃的水中(室温20℃),搅拌,观察到固体全部溶解,一段时间后有晶体析出。
(2)步骤2:取少量步骤1中的上层溶液于试管中,向其中滴加无色酚酞,观察到______ 。
结论:猜想I和猜想II均不成立。
阅读标签后,项目研究小组成员了解到白色颗粒为无水氯化钙。
项目二:探究家用除湿袋中的物质除湿原理
【资料信息】
1.常见氯化钙产品有无水氯化钙和CaCl2•xH2O(x=1、2、4、6),其中CaCl2•6H2O不具有吸水性,常温下饱和氯化钙溶液中析出的晶体是CaCl2•6H2O。
2.不同温度下氯化钙在水中的溶解度
小王同学对步骤1中现象产生浓厚兴趣,结合分析,预测产生现象的原因可能与氯化钙溶于水放热及溶解度随温度的变化等有关。
(3)请设计实验方案:在烧杯中加入10mL水,______ ,验证氯化钙固体溶于水是否放热。(写出必要的实验操作、现象,本实验中需要使用5g 氯化钙固体 )
(4)步骤3:另取8g无水氯化钙固体加入盛有10mL水的烧杯中,冷却至室温,过滤,称量析出的晶体质量为3.9g。过滤时所用玻璃仪器有玻璃棒、烧杯和______ ,所得滤液中溶质的质量分数为______ (列计算式 ),结合溶解度表数据,若按析出无水氯化钙计算质量为0.55g,实际析出固体质量大于0.55g的原因:______ 。
(5)步骤4:将步骤3过滤所得固体置于烘箱中,260℃烘干半小时得到无水氯化钙。写出烘干制得无水氯化钙的化学方程式:______ 。
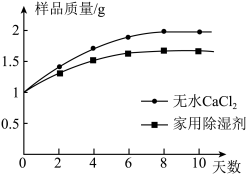
(6)步骤5:小杨同学分别称取1g无水氯化钙和1g某家用氯化钙除湿剂置于培养皿中,敞口放置在空气中,每天同一时间观察,测量质量,如图所示。请分析,两曲线差异的可能原因是______ 。
(7)小霞同学利用某常见气体的实验室制备原理制备氯化钙,其制备原理为______ (用化学方程式表示),制得的氯化钙溶液中常混有一定量盐酸,完成除去溶液中盐酸的方案:______ (本实验条件下,氯化钙溶液 pH=6 ,实验中需要使用Ca(OH)2粉末)。所得的氯化钙溶液经一系列操作转化为氯化钙固体,放入塑料瓶中自制了氯化钙除湿盒。
项目一:探究家用除湿袋中的物质成分
【资料信息】
吸湿区内白色颗粒是初中化学常见物质。使用一段时间后,集水袋内有大量液体和少量固体,且气温越低固体越多。
【提出问题】白色颗粒是什么物质?
(1)据所学知识进行作出猜想。猜想I:氧化钙,依据:
【进行实验】
步骤1:取8g白色颗粒于烧杯A中,加入10mL的20℃的水中(室温20℃),搅拌,观察到固体全部溶解,一段时间后有晶体析出。
(2)步骤2:取少量步骤1中的上层溶液于试管中,向其中滴加无色酚酞,观察到
结论:猜想I和猜想II均不成立。
阅读标签后,项目研究小组成员了解到白色颗粒为无水氯化钙。
项目二:探究家用除湿袋中的物质除湿原理
【资料信息】
1.常见氯化钙产品有无水氯化钙和CaCl2•xH2O(x=1、2、4、6),其中CaCl2•6H2O不具有吸水性,常温下饱和氯化钙溶液中析出的晶体是CaCl2•6H2O。
2.不同温度下氯化钙在水中的溶解度
| 温度/℃ | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 60℃ | 80℃ |
| 溶解度/g | 59.5 | 64.7 | 74.5 | 100 | 128 | 137 | 147 |
(3)请设计实验方案:在烧杯中加入10mL水,
(4)步骤3:另取8g无水氯化钙固体加入盛有10mL水的烧杯中,冷却至室温,过滤,称量析出的晶体质量为3.9g。过滤时所用玻璃仪器有玻璃棒、烧杯和
(5)步骤4:将步骤3过滤所得固体置于烘箱中,260℃烘干半小时得到无水氯化钙。写出烘干制得无水氯化钙的化学方程式:
(6)步骤5:小杨同学分别称取1g无水氯化钙和1g某家用氯化钙除湿剂置于培养皿中,敞口放置在空气中,每天同一时间观察,测量质量,如图所示。请分析,两曲线差异的可能原因是
(7)小霞同学利用某常见气体的实验室制备原理制备氯化钙,其制备原理为
您最近一年使用:0次
2024-06-13更新
|
79次组卷
|
3卷引用:江苏省泰州市医药高新区(高港区)2024年中考二模物理、化学试题-初中化学
江苏省泰州市医药高新区(高港区)2024年中考二模物理、化学试题-初中化学2024年江苏省泰州市高新(高港)区中考二模化学试题(已下线)专题11 实验探究-【好题汇编】2024年中考化学二模试题分类汇编(江苏专用)
2024·湖北·二模
解题方法
9 . 某工厂化验室用10.0%的氢氧化钠溶液洗涤100.0g石油产品中的含硫酸的残余废液,共消耗氢氧化钠溶液40.0g,洗涤后的溶液呈中性。(废液中其他物质不与氢氧化钠反应)
(1)洗涤过程中主要发生的化学反应的类型为______ (填基本反应类型)。
(2)求该残余废液中硫酸的溶质质量分数(精确到0.1%)。
(1)洗涤过程中主要发生的化学反应的类型为
(2)求该残余废液中硫酸的溶质质量分数(精确到0.1%)。
您最近一年使用:0次
解题方法
10 . 阅读下面科普短文。
土壤酸化是农业面临的问题之一。我国南方部分稻田土壤已出现不同程度的酸化,表现为部分稻田土壤的pH低于5.5。土壤酸化面积与强度仍在加剧。导致土壤酸化的原因有:过量施用氮肥等酸性肥料;工业排放的废气、废水等;不当的农业管理,如频繁耕作等。
水稻和油菜是耐酸性较强的作物,但在土壤酸化程度逐渐加剧的情况下,水稻和油菜的生产明显受到影响。向土壤中加入熟石灰调节pH可有效改良酸性土壤。
科研人员通过实验研究土壤的pH对水稻、油菜产量的影响。原有土壤的pH为4.5,加入一定量的熟石灰,将土壤的pH分别调至5.0、5.5、6.0、6.5和7.0,需要加入熟石灰的用量如下表所示。
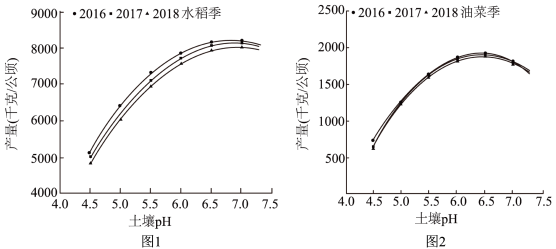
在同一土壤交替种植水稻和油菜,水稻、油菜产量随土壤pH的变化如下图所示。
依据文章内容回答下列问题。
(1)我国南方部分稻田土壤出现酸化的表现是______ 。
(2)土壤酸化与二氧化硫的排放有关,空气中二氧化硫增多的原因是______ (写一点)。
(3)假设土壤中的酸性物质为硫酸,写出熟石灰改良酸性土壤的化学方程式______ 。
(4)将pH=4.5的酸性土壤改良为pH=6.5,每公顷需要加入熟石灰的质量为______ kg。
(5)由图1可得出“2016、2017、2018三年,土壤的pH对水稻产量影响的变化趋势基本相同”,这一结论______ (填“成立”或“不成立”)。
(6)由图2可得出,油菜的产量与土壤pH的关系为______ 。
(7)预防土壤酸化可以采取哪些措施______ (写两点)。
土壤酸化是农业面临的问题之一。我国南方部分稻田土壤已出现不同程度的酸化,表现为部分稻田土壤的pH低于5.5。土壤酸化面积与强度仍在加剧。导致土壤酸化的原因有:过量施用氮肥等酸性肥料;工业排放的废气、废水等;不当的农业管理,如频繁耕作等。
水稻和油菜是耐酸性较强的作物,但在土壤酸化程度逐渐加剧的情况下,水稻和油菜的生产明显受到影响。向土壤中加入熟石灰调节pH可有效改良酸性土壤。
科研人员通过实验研究土壤的pH对水稻、油菜产量的影响。原有土壤的pH为4.5,加入一定量的熟石灰,将土壤的pH分别调至5.0、5.5、6.0、6.5和7.0,需要加入熟石灰的用量如下表所示。
| 土壤pH | 4.5 | 5.0 | 5.5 | 6.0 | 6.5 | 7.0 |
| 熟石灰用量(千克/公顷) | 0 | 1492 | 3154 | 4815 | 6477 | 8139 |
依据文章内容回答下列问题。
(1)我国南方部分稻田土壤出现酸化的表现是
(2)土壤酸化与二氧化硫的排放有关,空气中二氧化硫增多的原因是
(3)假设土壤中的酸性物质为硫酸,写出熟石灰改良酸性土壤的化学方程式
(4)将pH=4.5的酸性土壤改良为pH=6.5,每公顷需要加入熟石灰的质量为
(5)由图1可得出“2016、2017、2018三年,土壤的pH对水稻产量影响的变化趋势基本相同”,这一结论
(6)由图2可得出,油菜的产量与土壤pH的关系为
(7)预防土壤酸化可以采取哪些措施
您最近一年使用:0次
2024-06-13更新
|
214次组卷
|
4卷引用:辽宁省本溪市2024年中考二模考试物理化学试题 (1)-初中化学
辽宁省本溪市2024年中考二模考试物理化学试题 (1)-初中化学2024年辽宁省本溪市中考模拟化学试题2024年辽宁省辽阳市中考第二次模拟考试化学试题(已下线)专题07 燃烧及灭火 能源 环境保护-【好题汇编】2024年中考化学二模试题分类汇编(辽宁专用)



