名校
解题方法
1 . 某无色透明溶液中只可能含有Na+、SO 、Cl-、HCO
、Cl-、HCO 、CO
、CO 、H+、Cu2+中的几种,且每种离子的物质的量均为1mol。依次进行下列实验,每步所加试剂均过量,观察到的现象如表。下列结论正确的是
、H+、Cu2+中的几种,且每种离子的物质的量均为1mol。依次进行下列实验,每步所加试剂均过量,观察到的现象如表。下列结论正确的是
 、Cl-、HCO
、Cl-、HCO 、CO
、CO 、H+、Cu2+中的几种,且每种离子的物质的量均为1mol。依次进行下列实验,每步所加试剂均过量,观察到的现象如表。下列结论正确的是
、H+、Cu2+中的几种,且每种离子的物质的量均为1mol。依次进行下列实验,每步所加试剂均过量,观察到的现象如表。下列结论正确的是| 步骤 | 操作 | 现象 |
| (1) | 用紫色石蕊试液检验 | 溶液变红 |
| (2) | 向溶液中滴加BaCl2和稀HCl | 有白色沉淀生成 |
| (3) | 将(2)中所得混合物过滤,向滤液中加入AgNO3溶液和稀硝酸 | 有白色沉淀生成 |
| A.该实验无法确定是否含有Cl- |
B.可能含有的离子是Na+、SO 、Cl- 、Cl- |
C.肯定含有的离子是Na+、SO 、H+ 、H+ |
D.肯定没有的离子只有Cl-、HCO 、CO 、CO |
您最近一年使用:0次
2023-08-29更新
|
198次组卷
|
2卷引用:陕西省西安中学2023-2024学年高三上学期8月月考化学试题
名校
解题方法
2 . 化学小组通过实验探究分析一包KCl固体中的杂质成分并进行分离提纯。
(1)取该固体溶于水得无色溶液,则三位同学的检测结果正确的是___________ (填写代号)
(2)对该KCl固体精制的实验流程如图所示:

①配制100mL 0.1 KOH溶液时需要用到的玻璃仪器有;烧杯、玻璃棒、量筒、
KOH溶液时需要用到的玻璃仪器有;烧杯、玻璃棒、量筒、___________ 、胶头滴管;称量KOH固体时间过长,所配溶液的浓度___________ (填“偏高”“偏低”或“无影响”)。
②试剂A的化学式为___________ 。
③操作1的名称是___________ 。
④滴加稀盐酸后,大量减少的离子有___________ 。
(3)准确称取134.5g该固体溶于水,加入足量 溶液后过滤、洗涤、干燥、称量得沉淀29.1g,在所得沉淀中继续滴加足量稀盐酸,再次过滤、洗涤、干燥、称量得沉淀23.3g,计算知该固体中KCl的质量分数为
溶液后过滤、洗涤、干燥、称量得沉淀29.1g,在所得沉淀中继续滴加足量稀盐酸,再次过滤、洗涤、干燥、称量得沉淀23.3g,计算知该固体中KCl的质量分数为___________ 。
(1)取该固体溶于水得无色溶液,则三位同学的检测结果正确的是
| 检测同学 | 检测结果 |
| 甲 | KCl、 、 、 |
| 乙 | KCl、 、 、 |
| 丙 | KCl、 、 、 |

①配制100mL 0.1
 KOH溶液时需要用到的玻璃仪器有;烧杯、玻璃棒、量筒、
KOH溶液时需要用到的玻璃仪器有;烧杯、玻璃棒、量筒、②试剂A的化学式为
③操作1的名称是
④滴加稀盐酸后,大量减少的离子有
(3)准确称取134.5g该固体溶于水,加入足量
 溶液后过滤、洗涤、干燥、称量得沉淀29.1g,在所得沉淀中继续滴加足量稀盐酸,再次过滤、洗涤、干燥、称量得沉淀23.3g,计算知该固体中KCl的质量分数为
溶液后过滤、洗涤、干燥、称量得沉淀29.1g,在所得沉淀中继续滴加足量稀盐酸,再次过滤、洗涤、干燥、称量得沉淀23.3g,计算知该固体中KCl的质量分数为
您最近一年使用:0次
2023-08-21更新
|
59次组卷
|
2卷引用:广西河池市罗城仫佬族自治县高级中学等2校2022-2023学年高一上学期12月月考化学试题
名校
解题方法
3 . 某混合物的水溶液,只可能含有以下离子中的若干种: 、
、 、
、 、
、 、
、 、
、 、
、 ,现每次取100mL进行实验。(已知
,现每次取100mL进行实验。(已知 与
与 在溶液中可发生下列反应:
在溶液中可发生下列反应: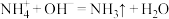 )
)
(1)第一份加入 溶液有沉淀产生。
溶液有沉淀产生。
(2)第二份加足量NaOH后加热,收集到气体0.896L(标准状况下)。
(3)第三份加足量 后,得干燥沉淀6.27g,沉淀经足量盐酸洗涤干燥后,剩余固体2.33g。根据以上实验,以下推测正确的是
后,得干燥沉淀6.27g,沉淀经足量盐酸洗涤干燥后,剩余固体2.33g。根据以上实验,以下推测正确的是
① 一定存在;
一定存在;
②100mL里面含有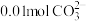 ;
;
③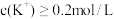 ;
;
④ 一定不存在,
一定不存在, 可能存在;
可能存在;
⑤ 离子浓度为0.1mol/L
离子浓度为0.1mol/L
 、
、 、
、 、
、 、
、 、
、 、
、 ,现每次取100mL进行实验。(已知
,现每次取100mL进行实验。(已知 与
与 在溶液中可发生下列反应:
在溶液中可发生下列反应: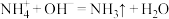 )
)(1)第一份加入
 溶液有沉淀产生。
溶液有沉淀产生。(2)第二份加足量NaOH后加热,收集到气体0.896L(标准状况下)。
(3)第三份加足量
 后,得干燥沉淀6.27g,沉淀经足量盐酸洗涤干燥后,剩余固体2.33g。根据以上实验,以下推测正确的是
后,得干燥沉淀6.27g,沉淀经足量盐酸洗涤干燥后,剩余固体2.33g。根据以上实验,以下推测正确的是①
 一定存在;
一定存在;②100mL里面含有
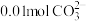 ;
;③
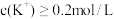 ;
;④
 一定不存在,
一定不存在, 可能存在;
可能存在;⑤
 离子浓度为0.1mol/L
离子浓度为0.1mol/L| A.①②③ | B.①③⑤ | C.①②④ | D.②③⑤ |
您最近一年使用:0次
2023-08-20更新
|
162次组卷
|
2卷引用:浙江省杭州市缙云中学等4校2022-2023学年高一上学期12月月考化学试题
解题方法
4 . 现有一混合溶液,可能含有以下离子中的若干种: 、
、 、
、 、
、 、
、 、
、 、
、 ,现取三份100mL该混合溶液进行如下实验。(已知:
,现取三份100mL该混合溶液进行如下实验。(已知: )
)
实验(1):向第一份混合溶液中加入 溶液,有沉淀产生;
溶液,有沉淀产生;
实验(2):向第二份混合溶液中滴加 的NaOH溶液,溶液中沉淀的质量与氢氧化钠的体积关系如图所示:
的NaOH溶液,溶液中沉淀的质量与氢氧化钠的体积关系如图所示:

实验(3):向第三份混合溶液中加入足量 溶液后,得到干燥的沉淀9.32g。
溶液后,得到干燥的沉淀9.32g。
下列说法正确的是
 、
、 、
、 、
、 、
、 、
、 、
、 ,现取三份100mL该混合溶液进行如下实验。(已知:
,现取三份100mL该混合溶液进行如下实验。(已知: )
)实验(1):向第一份混合溶液中加入
 溶液,有沉淀产生;
溶液,有沉淀产生;实验(2):向第二份混合溶液中滴加
 的NaOH溶液,溶液中沉淀的质量与氢氧化钠的体积关系如图所示:
的NaOH溶液,溶液中沉淀的质量与氢氧化钠的体积关系如图所示:
实验(3):向第三份混合溶液中加入足量
 溶液后,得到干燥的沉淀9.32g。
溶液后,得到干燥的沉淀9.32g。下列说法正确的是
| A.实验(1)中的沉淀全为AgCl |
B.该混合溶液中一定没有 、 、 |
C.该混合溶液中一定含有 、 、 、 、 、 、 、 、 ,且每一份中 ,且每一份中 |
D.加入V(NaOH)为80~100时发生的离子反应为 |
您最近一年使用:0次
名校
解题方法
5 . 下列是某化学研究性学习小组对某无色水样成分的检验过程,已知该水样中只可能含有K+、Mg2+、Cu2+、Ag+、Ca2+、CO 、SO
、SO 、Cl-中的若干种离子,该小组同学取100mL水样进行实验:向样品中先滴加氯化钡溶液,再滴加
、Cl-中的若干种离子,该小组同学取100mL水样进行实验:向样品中先滴加氯化钡溶液,再滴加 盐酸,实验过程中沉淀质量的变化如图所示。下列说法正确的是
盐酸,实验过程中沉淀质量的变化如图所示。下列说法正确的是

 、SO
、SO 、Cl-中的若干种离子,该小组同学取100mL水样进行实验:向样品中先滴加氯化钡溶液,再滴加
、Cl-中的若干种离子,该小组同学取100mL水样进行实验:向样品中先滴加氯化钡溶液,再滴加 盐酸,实验过程中沉淀质量的变化如图所示。下列说法正确的是
盐酸,实验过程中沉淀质量的变化如图所示。下列说法正确的是
| A.水样中一定不存在Mg2+、Cu2+、Ca2+,可能存在Ag+ |
B.水样中一定存在CO 、SO 、SO 和Cl- 和Cl- |
| C.由B点到C点变化过程中消耗盐酸的体积为40mL |
| D.水样中一定存在K+,且c(K+)≥0.3mol·L-1 |
您最近一年使用:0次
解题方法
6 . 某溶液中可能存在K+、Na+、Fe2+、Al3+、 、
、 中的若干种(除水电离出的H+,OH-之外),并且每种离子的浓度均为0.2mol·L-1。为确定溶液的组成进行了如下实验:
中的若干种(除水电离出的H+,OH-之外),并且每种离子的浓度均为0.2mol·L-1。为确定溶液的组成进行了如下实验:
i.取100mL原溶液,加入稀硝酸,产生气泡,该气泡遇空气立即变为红棕色。
ii.往i反应后的溶液中加入BaCl2溶液,产生难溶于水的白色沉淀。
下列判断正确的是
 、
、 中的若干种(除水电离出的H+,OH-之外),并且每种离子的浓度均为0.2mol·L-1。为确定溶液的组成进行了如下实验:
中的若干种(除水电离出的H+,OH-之外),并且每种离子的浓度均为0.2mol·L-1。为确定溶液的组成进行了如下实验:i.取100mL原溶液,加入稀硝酸,产生气泡,该气泡遇空气立即变为红棕色。
ii.往i反应后的溶液中加入BaCl2溶液,产生难溶于水的白色沉淀。
下列判断正确的是
| A.Fe2+、Al3+可能同时存在于溶液中 |
B.若溶液中有 ,则蘸取该溶液做焰色试验,可能观察到黄色火焰 ,则蘸取该溶液做焰色试验,可能观察到黄色火焰 |
C.溶液中可能有Al3+,一定没有 |
D.产生红棕色气体的离子方程式一定是3Fe2++4H++ =3Fe3++NO↑+2H2O =3Fe3++NO↑+2H2O |
您最近一年使用:0次
解题方法
7 . 某工业废水中可能含有 、
、 、
、 、
、 、
、 中的几种离子,为确定废水组成设计以下实验:
中的几种离子,为确定废水组成设计以下实验:
①取0.1L废水滴加足量氢氧化钠溶液,生成沉淀0.04mol;
②另取0.1L废水滴加足量氯化钡溶液,生成白色沉淀6.99g,再加入足量稀盐酸无明显变化。
回答下列问题:
(1)溶液中一定没有的离子是___________ 。
(2)溶液中可能含有的离子是___________ 。
(3)步骤①中产生沉淀的成分是___________ (用化学式表示);步骤②中加入氯化钡溶液发生反应的离子方程式是___________ 。
(4)溶液中一定含有的离子是___________ ;其中离子的物质的量一定能确定的离子是___________ 。
 、
、 、
、 、
、 、
、 中的几种离子,为确定废水组成设计以下实验:
中的几种离子,为确定废水组成设计以下实验:①取0.1L废水滴加足量氢氧化钠溶液,生成沉淀0.04mol;
②另取0.1L废水滴加足量氯化钡溶液,生成白色沉淀6.99g,再加入足量稀盐酸无明显变化。
回答下列问题:
(1)溶液中一定没有的离子是
(2)溶液中可能含有的离子是
(3)步骤①中产生沉淀的成分是
(4)溶液中一定含有的离子是
您最近一年使用:0次
名校
解题方法
8 . 常温下,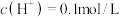 的某溶液中可能有
的某溶液中可能有 中的某几种,现取100mL该溶液进行如图实验。
中的某几种,现取100mL该溶液进行如图实验。

已知:单质碘是紫黑色固体,且氧化性 。
。
根据上述实验,回答下列问题:
(1)步骤①的实验操作名称是_____ ,步骤①中生成紫黑色固体单质的离子方程式是_____ 。
(2)此溶液中_____ (填“是”或“否”)存在 。若存在,则其物质的量浓度为
。若存在,则其物质的量浓度为_____ (若不存在,此问不作答)
(3)该溶液中一定不存在的离子有_____ 。
(4)根据整个实验过程推断 是否存在并说明理由。
是否存在并说明理由。_____ 。若存在,计算其物质的量浓度_____ 。(若不存在,此问不作答)
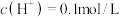 的某溶液中可能有
的某溶液中可能有 中的某几种,现取100mL该溶液进行如图实验。
中的某几种,现取100mL该溶液进行如图实验。
已知:单质碘是紫黑色固体,且氧化性
 。
。根据上述实验,回答下列问题:
(1)步骤①的实验操作名称是
(2)此溶液中
 。若存在,则其物质的量浓度为
。若存在,则其物质的量浓度为(3)该溶液中一定不存在的离子有
(4)根据整个实验过程推断
 是否存在并说明理由。
是否存在并说明理由。
您最近一年使用:0次
解题方法
9 . 某化学兴趣小组在一化工厂周围收集到一包10 g重的白色粉末状固体(已知其可能由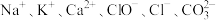 组成),欲探究其组成,进行了下列实验:
组成),欲探究其组成,进行了下列实验:
实验1:将白色粉末状固体溶于适量水中,过滤后得到50 mL滤液和1.165 g固体。
实验2:将实验1中所得固体加入盐酸中,完全溶解,有能使澄清石灰水变浑浊的气体产生。
实验3:将实验1中所得滤液分成两份,一份滴入纯碱溶液,无明显现象;将另一份溶液稀释至50 mL,向其中滴入2 mol/L的稀硫酸,仅产生黄绿色气体。当不再产生黄绿色气体时,测得消耗10 mL稀硫酸(不考虑反应可逆);再向溶液中加入10 mL2 mol/LBa(NO3)2溶液,恰好使 沉淀完全,过滤后向滤液中滴入1.5 mol/L的AgNO3溶液10 mL,恰好不再产生沉淀(体积变化忽略不计)。
沉淀完全,过滤后向滤液中滴入1.5 mol/L的AgNO3溶液10 mL,恰好不再产生沉淀(体积变化忽略不计)。
(1)由实验1可推断白色粉末状固体中含有___________ (填离子符号)。
(2)写出实验2中固体溶于盐酸的离子方程式:___________ 。
(3)实验3中滴入稀硫酸时发生反应的离子方程式为___________ 。
(4)白色粉末状固体中氯元素的质量为___________ g。
(5)通过计算,判断该白色粉末状固体___________ (填“含”或“不含”) 元素,若含有
元素,若含有 元素,则实验1的滤液中c(K+)=
元素,则实验1的滤液中c(K+)=___________ mol/L(若不含,此空不填);还可以通过___________ 判断白色粉末状固体是否含有 元素。
元素。
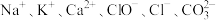 组成),欲探究其组成,进行了下列实验:
组成),欲探究其组成,进行了下列实验:实验1:将白色粉末状固体溶于适量水中,过滤后得到50 mL滤液和1.165 g固体。
实验2:将实验1中所得固体加入盐酸中,完全溶解,有能使澄清石灰水变浑浊的气体产生。
实验3:将实验1中所得滤液分成两份,一份滴入纯碱溶液,无明显现象;将另一份溶液稀释至50 mL,向其中滴入2 mol/L的稀硫酸,仅产生黄绿色气体。当不再产生黄绿色气体时,测得消耗10 mL稀硫酸(不考虑反应可逆);再向溶液中加入10 mL2 mol/LBa(NO3)2溶液,恰好使
 沉淀完全,过滤后向滤液中滴入1.5 mol/L的AgNO3溶液10 mL,恰好不再产生沉淀(体积变化忽略不计)。
沉淀完全,过滤后向滤液中滴入1.5 mol/L的AgNO3溶液10 mL,恰好不再产生沉淀(体积变化忽略不计)。(1)由实验1可推断白色粉末状固体中含有
(2)写出实验2中固体溶于盐酸的离子方程式:
(3)实验3中滴入稀硫酸时发生反应的离子方程式为
(4)白色粉末状固体中氯元素的质量为
(5)通过计算,判断该白色粉末状固体
 元素,若含有
元素,若含有 元素,则实验1的滤液中c(K+)=
元素,则实验1的滤液中c(K+)= 元素。
元素。
您最近一年使用:0次
名校
解题方法
10 . 已知1L待测液中含有下列离子中的6种: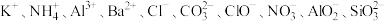 。现进行如下实验操作(每次实验所加试剂均足量);
。现进行如下实验操作(每次实验所加试剂均足量);
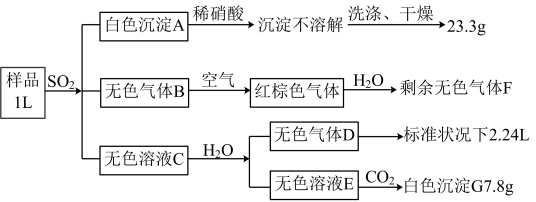
(1)生成无色气体B的离子方程式为_____ 。
(2)无色溶液 中通入足量二氧化碳生成白色沉淀
中通入足量二氧化碳生成白色沉淀 时,发生反应的离子方程式为
时,发生反应的离子方程式为_____ 。
(3)已知无色气体D能使湿润的红色石菠试纸变蓝,写出少量的 气体通入气体
气体通入气体 的水溶液中反应的离子方程式
的水溶液中反应的离子方程式_____ 。
(4)结合上述分析,白色沉淀 一定含
一定含_____ 。
(5)无色溶液C中大量含有的离子是_____ 。
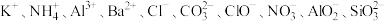 。现进行如下实验操作(每次实验所加试剂均足量);
。现进行如下实验操作(每次实验所加试剂均足量);
(1)生成无色气体B的离子方程式为
(2)无色溶液
 中通入足量二氧化碳生成白色沉淀
中通入足量二氧化碳生成白色沉淀 时,发生反应的离子方程式为
时,发生反应的离子方程式为(3)已知无色气体D能使湿润的红色石菠试纸变蓝,写出少量的
 气体通入气体
气体通入气体 的水溶液中反应的离子方程式
的水溶液中反应的离子方程式(4)结合上述分析,白色沉淀
 一定含
一定含(5)无色溶液C中大量含有的离子是
您最近一年使用:0次



