名校
解题方法
1 . 分类是科学研究的重要方法,下列物质分类正确的是
A.酸性氧化物: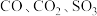 | B.常见氧化剂: |
C.同素异形体:石墨、 、金刚石 、金刚石 | D.电解质: 、氨水、 、氨水、 |
您最近半年使用:0次
解题方法
2 . 下列物质分类正确的是
选项 | 酸性氧化物 | 强酸 | 碱 |
A | 二氧化碳 | 硫酸氢钠 | 氢氧化钾 |
B | 三氧化硫 | 醋酸 | 纯碱 |
C | 一氧化碳 | 硫酸 | 氢氧化铜 |
D | 三氧化硫 | 硝酸 | 烧碱 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
3 . 研究物质性质具有重要的价值,根据所学知识回答下列问题:
(1)FeCl3是黑棕色晶体,主要用于金属蚀刻,污水处理。按照物质的分类方法,FeCl3应属于___________ (填序号)。
①酸;②氯化物;③混合物;④盐;⑤化合物;⑥电解质;⑦易溶于水物质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为___________ ;判断胶体制备是否成功可利用胶体的___________ ;
(3)铁元素是组成人体必不可少的元素之一,以下几种常见的铁元素粒子,既有氧化性又有还原性的是___________ 。
A.Fe B.Fe2+ C.Fe3+
(4)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。上述反应中氧化剂:___________ ;氧化产物:___________ 。
(1)FeCl3是黑棕色晶体,主要用于金属蚀刻,污水处理。按照物质的分类方法,FeCl3应属于
①酸;②氯化物;③混合物;④盐;⑤化合物;⑥电解质;⑦易溶于水物质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为
(3)铁元素是组成人体必不可少的元素之一,以下几种常见的铁元素粒子,既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(4)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。上述反应中氧化剂:
您最近半年使用:0次
4 . 化学基本概念和研究方法要准确掌握,下列是某同学对有关物质进行分类的列表:
(1)上述三组分类中的错误物质有______ 种。
(2)砷是与磷相邻同主族元素,则其在周期表的位置是______ ;砷化氢的电子式:______ ,它是一种有剧毒恶臭的无色气体,还原性极强,能与硝酸银反应生成Ag和砒霜(As2O3),反应的离子方程式为______ 。
(3)已知: ,在标准状况下,750ml含有O3的O2,当其中所含O3完全分解后体积变为780ml,若将此含有O3的O2lL通入KI溶液中,能析出
,在标准状况下,750ml含有O3的O2,当其中所含O3完全分解后体积变为780ml,若将此含有O3的O2lL通入KI溶液中,能析出______ 克I2(小数点后保留2位)。
(4)除去KCl溶液中少量的K2SO4杂质,要判断所加BaCl2溶液已经过量,操作是______ 。
(5)依据化学方程式,回答下列问题: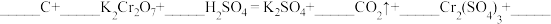
①配平完善化学方程式:_______________ 。
②H2SO4在上述反应中表现出来的性质是______ 。
③若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为______ L。
| 组序号 | 单质 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| ① | 灰砷(α-As) | Na2CO3 | H2C2O4 | K2SO4 | Na2O2 | SO3 |
| ② | 臭氧 | Fe(OH)3胶体 | H37Cl | KAl(SO4)2 | CaO | As2O3 |
| ③ | I2 | Al(OH)3 | CH3OH | K2Cr2O7 | Al2O3 | NO2 |
(2)砷是与磷相邻同主族元素,则其在周期表的位置是
(3)已知:
 ,在标准状况下,750ml含有O3的O2,当其中所含O3完全分解后体积变为780ml,若将此含有O3的O2lL通入KI溶液中,能析出
,在标准状况下,750ml含有O3的O2,当其中所含O3完全分解后体积变为780ml,若将此含有O3的O2lL通入KI溶液中,能析出(4)除去KCl溶液中少量的K2SO4杂质,要判断所加BaCl2溶液已经过量,操作是
(5)依据化学方程式,回答下列问题:
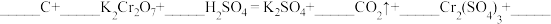
①配平完善化学方程式:
②H2SO4在上述反应中表现出来的性质是
③若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为
您最近半年使用:0次
解题方法
5 . 回答下列问题。
(1)请对下列物质进行归类。
 、
、 、
、 、
、 、
、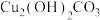 、
、 、
、 、
、 、
、
①属于酸的是___________ (写化学式,下同);属于碱的是___________ ;属于盐的是___________ 。
②属于碱性氧化物的是___________ ;属于酸性氧化物的是___________ 。
③属于酸式盐的是___________ ;属于碱式盐的是___________ ;属于钠盐的是___________ 。
(2)按要求书写出下列化学方程式。
①二氧化硫和氧化钠:___________ 。
②二氧化硫和过量的氢氧化钠溶液反应:___________ 。
③氧化钙和稀盐酸:___________ 。
④氧化钙和水:___________ 。
(1)请对下列物质进行归类。
 、
、 、
、 、
、 、
、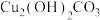 、
、 、
、 、
、 、
、
①属于酸的是
②属于碱性氧化物的是
③属于酸式盐的是
(2)按要求书写出下列化学方程式。
①二氧化硫和氧化钠:
②二氧化硫和过量的氢氧化钠溶液反应:
③氧化钙和稀盐酸:
④氧化钙和水:
您最近半年使用:0次
6 . 构建知识网络是一种重要的学习方法。如图是关于盐酸化学性质的知识网络图:“﹣”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质。若A、B、C分别属于不同类别的化合物,则A、B、C可能是


A. | B. |
C.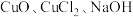 | D. |
您最近半年使用:0次
解题方法
7 . 下列物质的转变,不能一步实现的是
A. | B. |
C. | D.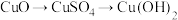 |
您最近半年使用:0次
解题方法
8 . 下列说法中不正确的有几个
①将碳酸钡放入水中不能导电,所以碳酸钡是非电解质
②氨气溶于水得到的氨水能导电,所以氨水是电解质
③铜的导电性良好,所以铜是电解质
④ 电离时生成的阳离子有氢离子,所以是酸
电离时生成的阳离子有氢离子,所以是酸
⑤稀盐酸中 在电流的作用下电离出
在电流的作用下电离出 和
和
①将碳酸钡放入水中不能导电,所以碳酸钡是非电解质
②氨气溶于水得到的氨水能导电,所以氨水是电解质
③铜的导电性良好,所以铜是电解质
④
 电离时生成的阳离子有氢离子,所以是酸
电离时生成的阳离子有氢离子,所以是酸⑤稀盐酸中
 在电流的作用下电离出
在电流的作用下电离出 和
和
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近半年使用:0次
解题方法
9 . 下列关于物质分类的正确组合是
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | Na2CO3 | H2SO4 | NaHCO3 | Na2O2 | CO2 |
| B | NaOH | HCl | NH4NO3 | Na2O | SO3 |
| C | Mg(OH)2 | CH3COOH | NaCl | Mn2O7 | SO2 |
| D | KOH | H2S | CaCO3 | CaO | CO |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
10 . 最近,宿城一中在校园内喷洒了“84消毒液”,它能有效杀灭新冠病毒。刘冠宇同学购买了一瓶“84消毒液”,用于自己家院落的消毒,该消毒液包装说明如图:
该“84消毒液”通常稀释100倍(体积之比)后使用。
回答下列问题:
(1)NaClO属于________ 类物质(填字母)
A.酸 B.碱 C.盐 D.氧化物 E.纯净物 F.混合物
(2)该“84消毒液”的物质的量浓度约为________ mol·L-1(保留1位小数)。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是________ (填序号)。

A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.需要称量NaClO固体的质量为143.0 g
C.容量瓶用蒸馏水洗净后,不用烘干便能用于溶液配制
(4)已知“84消毒液”和洁厕灵(主要成分为盐酸)不能混用,否则会产生有毒的黄绿色气体,请写出发生反应的离子方程式________________ 。
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用18.4mol·L-1(质量分数为98%,密度为1.84 g·cm-3)的浓硫酸配制100 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①需用浓硫酸的体积为________ mL。
②为配制上述稀硫酸除烧杯、玻璃棒、胶头滴管、试剂瓶外,还缺少的玻璃仪器是________ 。
③将所配制的稀硫酸进行测定,发现实际浓度大于2.3mol·L-1。会引起所配溶液浓度偏高的操作有________ (填序号)。
A.用量筒量取浓硫酸时,仰视量筒的刻度线
B.容量瓶未干燥就用来配制溶液
C.浓硫酸在烧杯中稀释后,未冷却就立即转移至容量瓶中
D.烧杯中稀溶液往容量瓶中转移时,有少量液体溅出
E.用量筒量取浓硫酸后未洗涤量筒
F.定容时俯视容量瓶刻度线
| 84消毒液 【有效成分】NaClO 【规格】1000mL 【质量分数】25% 【密度】1.19g•cm-3 |
回答下列问题:
(1)NaClO属于
A.酸 B.碱 C.盐 D.氧化物 E.纯净物 F.混合物
(2)该“84消毒液”的物质的量浓度约为
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是

A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.需要称量NaClO固体的质量为143.0 g
C.容量瓶用蒸馏水洗净后,不用烘干便能用于溶液配制
(4)已知“84消毒液”和洁厕灵(主要成分为盐酸)不能混用,否则会产生有毒的黄绿色气体,请写出发生反应的离子方程式
(5)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用18.4mol·L-1(质量分数为98%,密度为1.84 g·cm-3)的浓硫酸配制100 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①需用浓硫酸的体积为
②为配制上述稀硫酸除烧杯、玻璃棒、胶头滴管、试剂瓶外,还缺少的玻璃仪器是
③将所配制的稀硫酸进行测定,发现实际浓度大于2.3mol·L-1。会引起所配溶液浓度偏高的操作有
A.用量筒量取浓硫酸时,仰视量筒的刻度线
B.容量瓶未干燥就用来配制溶液
C.浓硫酸在烧杯中稀释后,未冷却就立即转移至容量瓶中
D.烧杯中稀溶液往容量瓶中转移时,有少量液体溅出
E.用量筒量取浓硫酸后未洗涤量筒
F.定容时俯视容量瓶刻度线
您最近半年使用:0次



