名校
1 . Ⅰ.H2O2被称为绿色氧化剂,对其性质进行研究极其重要。某同学以H2O2分解为例,进行了以下实验:
(1)问题一:设计实验②和③的目的是:_______ 。
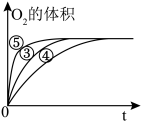
(2)问题二:实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出什么实验结论______ 。
Ⅱ.氮氧化物是主要的大气污染物之一,可用一氧化碳或活性炭还原氮氧化物,减少大气污染。
(3)一定条件下,用CO与NO反应生成CO2和N2,反应的化学方程式:2CO(g)+2NO(g) N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是
N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是______ (填标号)。
(4)两个10L的密闭容器中分别都加入活性炭(足量)和1.0molNO,发生反应:C(s)+2NO(g)  N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:
N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:
①T1时,0~5min内,反应速率v(CO2)=______ mol•L-1•min-1。
②T2时,按表中数据,反应一定达到化学平衡状态的时间段是______ min~10min,此时,容器中CO2的物质的量浓度是______ mo/L。
③两容器中温度关系为T1______ T2(填“>”“<”或“=”)。
| 编号 | 反应物 | 催化剂 | 温度 |
| ① | 20mL2%H2O2溶液+2mLH2O | 无 | 20℃ |
| ② | 20mL5%H2O2溶液+2mLH2O | 无 | 20℃ |
| ③ | 20mL5%H2O2溶液+2mLH2O | 1g粉末状MnO2 | 20℃ |
| ④ | 20mL5%H2O2溶液+2mL1mol/LHCl溶液 | 1g粉末状MnO2 | 20℃ |
| ⑤ | 20mL5%H2O2溶液+2mLH2O | 1g粉末状MnO2 | 40℃ |
(2)问题二:实验③、④、⑤中,测得生成氧气的体积随时间变化如图所示。分析该图能够得出什么实验结论

Ⅱ.氮氧化物是主要的大气污染物之一,可用一氧化碳或活性炭还原氮氧化物,减少大气污染。
(3)一定条件下,用CO与NO反应生成CO2和N2,反应的化学方程式:2CO(g)+2NO(g)
 N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是
N2(g)+2CO2(g)。为提高该反应的速率,下列措施可行的是| A.压缩容器体积 | B.降低温度 |
| C.使用合适催化剂 | D.恒温恒容充入稀有气体 |
 N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:
N2(g)+CO2(g)。实验测得,两容器中在不同温度下NO和N2的物质的量变化见表:| 物质的量/mol | 容器1(T1℃) | 容器2(T2℃) | |||||||
| 0 | 5min | 9min | 10min | 12min | 0 | 5min | 9min | 10min | |
| NO | 1.0 | 0.58 | 0.42 | 0.40 | 0.40 | 1.0 | 0.50 | 0.34 | 0.34 |
| N2 | 0 | 0.21 | 0.29 | 0.30 | 0.30 | 0 | 0.25 | 0.33 | 0.33 |
②T2时,按表中数据,反应一定达到化学平衡状态的时间段是
③两容器中温度关系为T1
您最近一年使用:0次
2023-05-23更新
|
182次组卷
|
4卷引用:广东省湛江市第二十一中学2022-2023学年高一下学期期中考试(选考)化学试题



