名校
1 . 以黄铜矿(主要成分二硫化亚铁铜CuFeS2)为原料,用Fe2(SO4)3溶液作浸取剂提取铜,总反应的离子方程式是CuFeS2+4Fe3+ Cu2++5Fe2++2S。
Cu2++5Fe2++2S。
(1)该反应中,Fe3+体现________ 性。
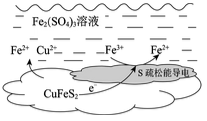
(2)上述总反应的原理如图所示。
负极的电极反应式是________ 。
(3)一定温度下,控制浸取剂pH=1,取三份相同质量黄铜矿粉末分别进行如下实验:
①对比实验I、II,通入空气,Cu2+浸出率提高的原因是________ 。
②由实验III推测,在浸取Cu2+过程中Ag+作催化剂,催化原理是:
ⅰ.CuFeS2+4Ag+=Fe2++Cu2++2Ag2S
ⅱ.Ag2S+2Fe3+=2Ag++2Fe2++S
为证明该催化原理,进行如下实验:
a.取少量黄铜矿粉末,加入少量0.0005mol·L-1Ag2SO4溶液,充分混合后静置。取上层清液,加入稀盐酸,观察到溶液中________ ,证明发生反应i。
b.取少量Ag2S粉末,加入________ 溶液,充分混合后静置。取上层清液,加入稀盐酸,有白色沉淀,证明发生反应ii。
(4)用实验II的浸取液电解提取铜的原理如图所示:
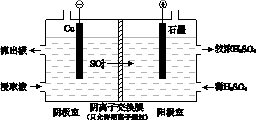
①电解初期,阴极没有铜析出。用电极反应式解释原因是_______________ 。
②将阴极室的流出液送入阳极室,可使浸取剂再生,再生的原理是_____________________ 。
 Cu2++5Fe2++2S。
Cu2++5Fe2++2S。(1)该反应中,Fe3+体现

(2)上述总反应的原理如图所示。
负极的电极反应式是
(3)一定温度下,控制浸取剂pH=1,取三份相同质量黄铜矿粉末分别进行如下实验:
| 实验 | 操作 | 2小时后Cu2+浸出率/% |
| I | 加入足量0.10mol·L-1Fe2(SO4)3溶液 | 78.2 |
| II | 加入足量0.10mol·L-1Fe2(SO4)3溶液,通入空气 | 90.8 |
| III | 加入足量0.10mol·L-1Fe2(SO4)3溶液,再加入少量0.0005mol·L-1Ag2SO4溶液 | 98.0 |
②由实验III推测,在浸取Cu2+过程中Ag+作催化剂,催化原理是:
ⅰ.CuFeS2+4Ag+=Fe2++Cu2++2Ag2S
ⅱ.Ag2S+2Fe3+=2Ag++2Fe2++S
为证明该催化原理,进行如下实验:
a.取少量黄铜矿粉末,加入少量0.0005mol·L-1Ag2SO4溶液,充分混合后静置。取上层清液,加入稀盐酸,观察到溶液中
b.取少量Ag2S粉末,加入
(4)用实验II的浸取液电解提取铜的原理如图所示:

①电解初期,阴极没有铜析出。用电极反应式解释原因是
②将阴极室的流出液送入阳极室,可使浸取剂再生,再生的原理是
您最近一年使用:0次
2017-05-20更新
|
348次组卷
|
5卷引用:宁夏六盘山高级中学2017届高三第四次模拟考试理科综合化学试题
宁夏六盘山高级中学2017届高三第四次模拟考试理科综合化学试题湖北省宜昌市第一中学2018届高三年级适应性训练(二)理综化学试题(已下线)《2020年新高考政策解读与配套资源》模拟试题08-2020年北京新高考化学模拟试题安徽省定远县育才学校2019-2020学年高二下学期期末考试化学试题北京理工大学附属中学2022-2023学年高三上学期12月月考化学试题



