名校
解题方法
1 . 锌铜原电池的装置如图,下列说法正确的是

| A.若用乙醇代替CuSO4溶液,则也能构成原电池 |
| B.铜电极的电极反应式为Cu2++2e-=Cu |
| C.电子由锌电极流出,经电解质溶液传递到铜电极 |
| D.电池工作时,溶液中的Cu2+向锌电极迁移 |
您最近一年使用:0次
2024-03-11更新
|
1222次组卷
|
5卷引用:湖北省A9高中联盟2023-2024学年高二上学期期中联考化学试题
名校
解题方法
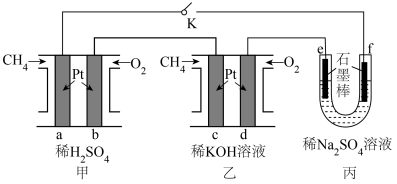
2 . 利用甲烷( )燃料电池电解硫酸钠溶液的装置如图所示。下列说法错误的是
)燃料电池电解硫酸钠溶液的装置如图所示。下列说法错误的是
 )燃料电池电解硫酸钠溶液的装置如图所示。下列说法错误的是
)燃料电池电解硫酸钠溶液的装置如图所示。下列说法错误的是
| A.甲装置、乙装置均为原电池,丙装置为电解池 |
B.b电极的电极反应式为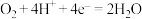 |
C.若甲、乙各消耗 ,向丙中加入 ,向丙中加入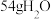 可使丙装置恢复原浓度 可使丙装置恢复原浓度 |
D.当K闭合时,整个电路中电子的流动方向为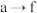 , ,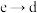 , ,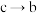 |
您最近一年使用:0次
名校
解题方法
3 . 按下图所示装置连接好仪器,下列相关说法错误的是
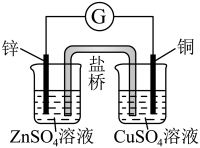

| A.该装置工作时将化学能转化为电能 |
| B.盐桥中阴离子移向锌片 |
C.铜片上的电极反应: |
| D.电子流向:铜片→CuSO4溶液→盐桥→ZnSO4溶液→锌片→导线→铜片 |
您最近一年使用:0次
4 .  是强氧化剂,也是航天航空、水下作业的供氧剂。近几年科学家研制出较锂电池稳定性更高、电压损失更小的“钠—空气电池”。其反应原理是:
是强氧化剂,也是航天航空、水下作业的供氧剂。近几年科学家研制出较锂电池稳定性更高、电压损失更小的“钠—空气电池”。其反应原理是: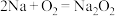 ,装置如图,其中电解液为
,装置如图,其中电解液为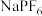 ,可传导
,可传导 。电池放电时,下列说法
。电池放电时,下列说法不正确 的是
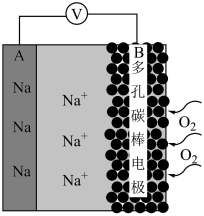
 是强氧化剂,也是航天航空、水下作业的供氧剂。近几年科学家研制出较锂电池稳定性更高、电压损失更小的“钠—空气电池”。其反应原理是:
是强氧化剂,也是航天航空、水下作业的供氧剂。近几年科学家研制出较锂电池稳定性更高、电压损失更小的“钠—空气电池”。其反应原理是: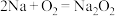 ,装置如图,其中电解液为
,装置如图,其中电解液为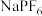 ,可传导
,可传导 。电池放电时,下列说法
。电池放电时,下列说法
| A.A电极为负极,发生氧化反应 |
B. 向 向 电极移动 电极移动 |
C.外电路电流方向为 |
D.当转移电子 时,消耗 时,消耗 (标准状况) (标准状况) |
您最近一年使用:0次
解题方法
5 . 我国科学家发明的一种可控锂水电池的工作原理如图所示。下列有关说法正确的是
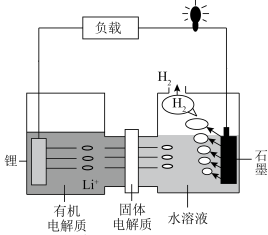
| A.锂为负极,发生还原反应 |
B. 移向正极并在正极得电子 移向正极并在正极得电子 |
| C.电子由锂→有机电解质→固体电解质→水溶液→石墨 |
D.电池工作时的总反应为: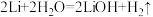 |
您最近一年使用:0次
2024-03-01更新
|
614次组卷
|
2卷引用:广东省广州市天河区2023-2024学年高二上学期期末化学试卷
名校
解题方法
6 . 碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s),下列说法错误的是
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e-=Mn2O3(s)+2OH-(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
您最近一年使用:0次
解题方法
7 . 瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图所示,其中的固体电解质是 ,O2-可以在其中自由移动。下列有关叙述正确的是
,O2-可以在其中自由移动。下列有关叙述正确的是
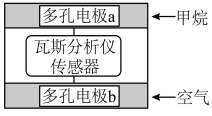
 ,O2-可以在其中自由移动。下列有关叙述正确的是
,O2-可以在其中自由移动。下列有关叙述正确的是
| A.瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a |
| B.电极b是正极,O2-由电极a流向电极b |
C.电极a的反应式为: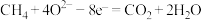 |
| D.当固体电解质中有1mol O2-通过时,电子转移4mol |
您最近一年使用:0次
名校
解题方法
8 . 根据下图,下列说法正确的是
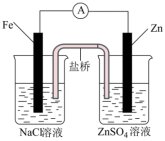 | 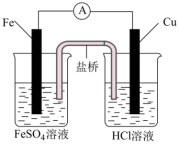 |
| Ⅰ | Ⅱ |
| A.装置Ⅰ和装置Ⅱ中负极反应均是Fe-2e-=Fe2+ |
| B.装置Ⅰ和装置Ⅱ盐桥中的阳离子均向右侧烧杯移动 |
| C.装置Ⅰ和装置Ⅱ中正极反应式均为O2+2H2O+4e-=4OH-, |
| D.放电过程中,装置Ⅰ和装置Ⅱ中正极区溶液的pH均逐渐增大 |
您最近一年使用:0次
9 . 中科大研究构建的宽温氢氯电池如图所示,能在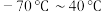 范围内使用并实现多次充放电。下列说法
范围内使用并实现多次充放电。下列说法错误 的是
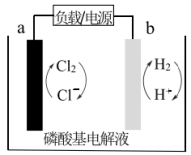
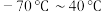 范围内使用并实现多次充放电。下列说法
范围内使用并实现多次充放电。下列说法
| A.磷酸基电解液具有抗冻性 |
B.放电时,电子从 极经导线流向 极经导线流向 极 极 |
| C.电极具有多孔结构,能够实现气体循环使用 |
D.充电时,阳极电极反应式为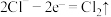 |
您最近一年使用:0次
解题方法
10 . 下图为某铜锌原电池工作装置图,下列叙述不正确的是
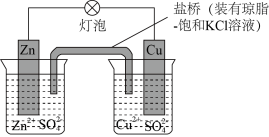

| A.盐桥中的K+移向ZnSO4溶液 |
| B.一段时间后,铜电极增重 |
| C.负极反应为Zn-2e-=Zn2+ |
| D.在外电路中,电子从负极流向正极 |
您最近一年使用:0次



