名校
1 . 最近,南开大学水系电池课题组开发了一种六电子氧化还原I/石墨烯电极可充电电池,其能量密度显著高于传统的水系I基电池,示意图如下。
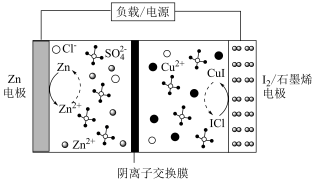
A.放电时, /石墨烯电极消耗 /石墨烯电极消耗 发生还原反应 发生还原反应 |
B.充电时, /石墨烯电极反应式为 /石墨烯电极反应式为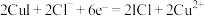 |
C.放电时,电池总反应为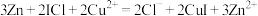 |
| D.石墨烯能增强电极的导电性,放电时阴离子向正极移动 |
您最近一年使用:0次
名校
解题方法
2 . 钇稳定氧化锆浓差电池可用于测定待测环境中的含氧量,在冶金、能源等领域也应用广泛,其原理是利用空气与待测环境中氧气的浓度差对电压的影响,其工作状态如图所示。该电池工作时,下列说法错误的是

| A.空气侧的电极电势高于测量侧的电极电势 |
B. 、 、 移向空气侧 移向空气侧 |
C.电极B发生的反应为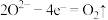 |
| D.若测量侧处于富氧环境中时,电池的正负极可能会发生转换 |
您最近一年使用:0次
3 . 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测,质子交换膜只允许 通过,下列说法错误的是
通过,下列说法错误的是
 通过,下列说法错误的是
通过,下列说法错误的是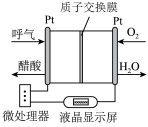
A. 在电池工作时向 在电池工作时向 所在的铂电极移动 所在的铂电极移动 |
B.电子由呼气的铂电极经电解质溶液流向 所在的铂电极 所在的铂电极 |
| C.微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
D.呼气中的酒精分子在 电极被还原为醋酸分子 电极被还原为醋酸分子 |
您最近一年使用:0次
4 . 微生物脱盐池是在微生物燃料电池的基础上发展而来的新兴生物电化学系统,示意图如图所示。下列说法正确的是
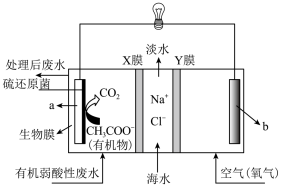
| A.该装置能同时实现海水淡化、化学能转化为电能 |
B.当消耗标况下氧气11.2L时,透过X、Y交换膜的离子总数是 个 个 |
C.负极反应为 |
| D.Y为阴离子交换膜 |
您最近一年使用:0次
名校
解题方法
5 . 一种新型微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示,下列说法正确的是。
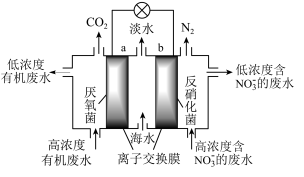
| A.该电池能在高温下工作 |
| B.a极为电池的正极 |
| C.有机废水处理后pH降低 |
D.处理 的电极反应为 的电极反应为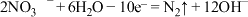 |
您最近一年使用:0次
6 . 离子液体是指在室温或接近室温下呈现液态的、完全由阴阳离子所组成的盐,也称为低温熔融盐。一种以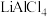 离子液体为电解质溶液的铝—磷酸铁锂二次电池放电时的工作原理如图所示。下列说法正确的是
离子液体为电解质溶液的铝—磷酸铁锂二次电池放电时的工作原理如图所示。下列说法正确的是
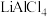 离子液体为电解质溶液的铝—磷酸铁锂二次电池放电时的工作原理如图所示。下列说法正确的是
离子液体为电解质溶液的铝—磷酸铁锂二次电池放电时的工作原理如图所示。下列说法正确的是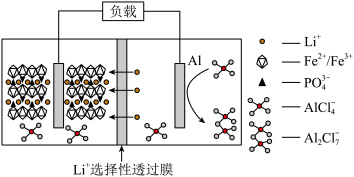
A.充电时,阳极的电极反应式为 |
| B.放电时,磷酸铁锂电极中锂元素被氧化 |
C.放电时,铝为负极,其电极反应式为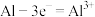 |
| D.充电时,电子由Al电极经离子液体流向磷酸铁锂电极 |
您最近一年使用:0次
7 . 硼化钒(VB2)—空气电池是目前储电能力最高的电池,工作原理如图所示,该电池工作时反应为: 4VB2+11O2 = 4B2O3+2V2O5。不正确 的是
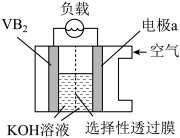
| A.电极a发生还原反应 |
| B.电流由电极a经负载流向VB2极 |
| C.VB2极发生的电极反应为:2VB2 +22OH−-22e−=V2O5+2B2O3 +11H2O |
| D.图中选择性透过膜允许阳离子选择性透过 |
您最近一年使用:0次
解题方法
8 . 中国科学院研制出一种陶瓷基混合导体透氧膜,它允许电子和 同时通过,可实现水连续分解制
同时通过,可实现水连续分解制 。工作时,CO、
。工作时,CO、 分别在透氧膜的两侧反应,工作原理如图所示。下列说法错误的是
分别在透氧膜的两侧反应,工作原理如图所示。下列说法错误的是
 同时通过,可实现水连续分解制
同时通过,可实现水连续分解制 。工作时,CO、
。工作时,CO、 分别在透氧膜的两侧反应,工作原理如图所示。下列说法错误的是
分别在透氧膜的两侧反应,工作原理如图所示。下列说法错误的是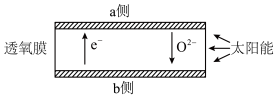
| A.CO在b侧反应 | B.b侧发生还原反应 |
C.a侧发生的电极反应为 | D.该装置实现了太阳能转化为化学能 |
您最近一年使用:0次
名校
解题方法
9 . 化学电源在生产生活中有着广泛的应用,请回答下列问颕:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是___________(填字母,下同)。
(2)电子表和电子计算器中所用的是钮扣式的微型银锌电池,其电极分别为 和Zn,电解液为KOH溶液。工作时电池总反应为:
和Zn,电解液为KOH溶液。工作时电池总反应为: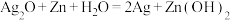 。
。
①工作时电流从___________ 极流向___________ 极(两空均选填“ ”或“Zn”);
”或“Zn”);
②负极的电极反应式为:___________ ;
③工作时电池正极区的pH___________ (选填“增大”“减小”或“不变”);
④外电路中每通过0.2mol电子,锌的质量理论上减少___________ g。
(3)理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“ ”设计一种化学电池(正极材料用石墨棒),回答下列问题:
”设计一种化学电池(正极材料用石墨棒),回答下列问题:
①该电池的负极材料是___________ (填化学式),电解质溶液是___________ (填化学式)溶液。
②正极上发生的电极反应为___________ 。
③若导线上转移的电子为1mol,则消耗的金属铜的质量为___________ 。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是___________(填字母,下同)。
A.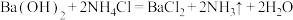 |
B. |
C. |
D. |
 和Zn,电解液为KOH溶液。工作时电池总反应为:
和Zn,电解液为KOH溶液。工作时电池总反应为: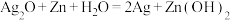 。
。①工作时电流从
 ”或“Zn”);
”或“Zn”);②负极的电极反应式为:
③工作时电池正极区的pH
④外电路中每通过0.2mol电子,锌的质量理论上减少
(3)理论上,任何自发的氧化还原反应都可以设计成原电池。请利用反应“
 ”设计一种化学电池(正极材料用石墨棒),回答下列问题:
”设计一种化学电池(正极材料用石墨棒),回答下列问题:①该电池的负极材料是
②正极上发生的电极反应为
③若导线上转移的电子为1mol,则消耗的金属铜的质量为
您最近一年使用:0次
名校
10 . 钴酸锂电池的结构稳定、比容量高,但成本非常高,常用于小型电子设备中,负极材料是嵌入锂的石墨,可以表示为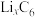 ,正极材料为
,正极材料为 ,放电时的工作原理如图所示(交换膜只允许
,放电时的工作原理如图所示(交换膜只允许 通过)。放电时,下列说法错误的是
通过)。放电时,下列说法错误的是
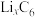 ,正极材料为
,正极材料为 ,放电时的工作原理如图所示(交换膜只允许
,放电时的工作原理如图所示(交换膜只允许 通过)。放电时,下列说法错误的是
通过)。放电时,下列说法错误的是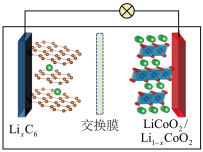
| A.主要将化学能转化为电能 |
B.正极材料中的 变为 变为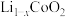 |
C. 经交换膜由左室进入右室 经交换膜由左室进入右室 |
| D.外电路中电流由正极流向负极,内电路中电流由负极流向正极 |
您最近一年使用:0次



