解题方法
1 . 下列是A、B、C、D、E、F、G、H及丙二酸(HOOCCH2COOH)间转化反应的关系图。A是一种链状羧酸,分子式为C3H4O2;F中含有由七个原子构成的环;H是一种高分子化合物。请填写下列空白:
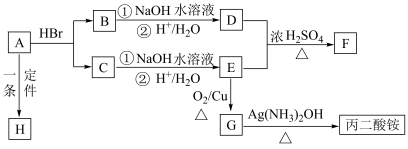
(1)C的结构简式:___________ ;F的结构简式:___________ 。
(2)写出下列反应的化学方程式和反应类型:
①A→H的化学方程式:___________ 。
②B与NaOH溶液反应的化学方程式:___________ 。
③G→丙二酸的化学方程式:___________ ;反应类型:___________ 。

(1)C的结构简式:
(2)写出下列反应的化学方程式和反应类型:
①A→H的化学方程式:
②B与NaOH溶液反应的化学方程式:
③G→丙二酸的化学方程式:
您最近半年使用:0次
名校
解题方法
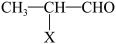
2 . 化合物G(丙酸异丙酯)可用作食品香料。现可通过下列转化制取(部分反应条件略去):
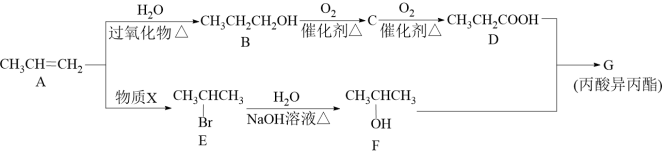
(1)物质X的化学式为_____
(2)化合物G的结构简式是_____ 。
(3)B→C化学方程式为_____
(4)化合物A在一定条件下生成高分子有机物的化学方程式是_____ 。
(5)下列关于化合物B、D的说法正确的是_____。

(1)物质X的化学式为
(2)化合物G的结构简式是
(3)B→C化学方程式为
(4)化合物A在一定条件下生成高分子有机物的化学方程式是
(5)下列关于化合物B、D的说法正确的是_____。
| A.均能和Na反应放出H2 | B.均溶于水 |
| C.均能和O2在一定条件发生氧化反应 | D.均能和NaHCO3反应放出CO2 |
您最近半年使用:0次
3 . 有机官能团之间存在相互转化,阅读并分析以下转化过程,完成填空:
Ⅰ.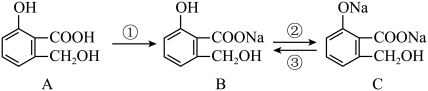
(1)向A中加入溴水,1mol A最多可以与___________ molBr2反应。
(2)为以下转化选择合适的试剂:①反应___________ ,②反应___________ 。
A.Na B. C.NaOH D.
C.NaOH D.
(3)写出③反应的化学反应方程式:___________ 。
Ⅱ.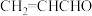
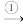

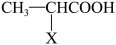

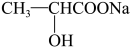
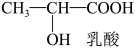
(4)向 中加入酸性
中加入酸性 ,是否可检验其中的碳碳双键?
,是否可检验其中的碳碳双键?___________ 。(填“是”或“否”)
(5)乳酸可在浓硫酸加热条件下生成丙烯酸,写出丙烯酸加聚生成的聚丙烯酸 的结构式:___________ 。
Ⅰ.

(1)向A中加入溴水,1mol A最多可以与
(2)为以下转化选择合适的试剂:①反应
A.Na B.
 C.NaOH D.
C.NaOH D.
(3)写出③反应的化学反应方程式:
Ⅱ.
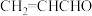


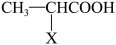

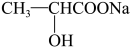
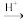
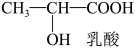
(4)向
 中加入酸性
中加入酸性 ,是否可检验其中的碳碳双键?
,是否可检验其中的碳碳双键?(5)乳酸可在浓硫酸加热条件下生成丙烯酸,写出丙烯酸加聚生成的
您最近半年使用:0次
名校
解题方法
4 . 丙烯二聚体 是合成“人工肺”(EMCO)设备膜丝的重要原料,下列关于丙烯二聚体说法错误的是
是合成“人工肺”(EMCO)设备膜丝的重要原料,下列关于丙烯二聚体说法错误的是
 是合成“人工肺”(EMCO)设备膜丝的重要原料,下列关于丙烯二聚体说法错误的是
是合成“人工肺”(EMCO)设备膜丝的重要原料,下列关于丙烯二聚体说法错误的是| A.加聚产物能使溴水因化学反应而褪色 | B.与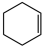 是同分异构体 是同分异构体 |
C.与 完全加成的产物一氯代物有5种 完全加成的产物一氯代物有5种 | D.完全燃烧时的耗氧量与等质量的丙烯相同 |
您最近半年使用:0次
2024-02-11更新
|
185次组卷
|
2卷引用:上海市上海中学2023-2024学年高二上学期期末考试化学试卷
5 . 在实验室利用下列装置,可制备某些气体并验证其化学性质。
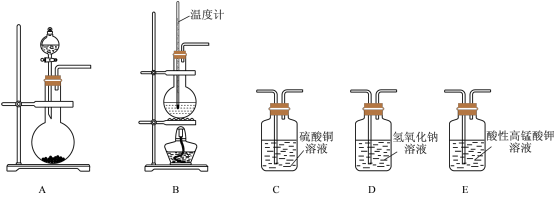
(1)填空,完成下列表格:
(2)工业上用乙烯和氯气为原料,经下列各步合成聚氯乙烯(PVC):反应4的化学方程式是___________ 。
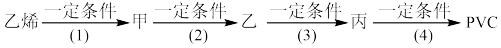
(3)下列说法正确的是___________。
(4)石油被称为“工业血液”。A是从石油中得到的链状烃,相对分子质量为42.以A为原料,利用下述反应合成甘油 (丙三醇),在方框内填上中间体的结构简式。___________ 、___________ 。
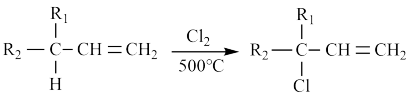


(1)填空,完成下列表格:
| 序号 | 气体 | 装置连接顺(填字母) | 制备反应的化学方程式 |
| ① | 乙烯 | B→D→E | |
| ② | 乙炔 |  |
(2)工业上用乙烯和氯气为原料,经下列各步合成聚氯乙烯(PVC):反应4的化学方程式是
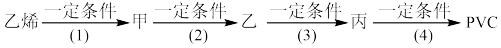
(3)下列说法正确的是___________。
| A.乙烯可以作为植物生长调节剂 | B.PVC不能使酸性高锰酸钾溶液褪色 |
| C.PVC中的官能团是碳碳双键和氯原子 | D.PVC可用作食品包装袋 |
(4)石油被称为“工业血液”。A是从石油中得到的链状烃,相对分子质量为42.以A为原料,利用下述反应合成甘油 (丙三醇),在方框内填上中间体的结构简式。
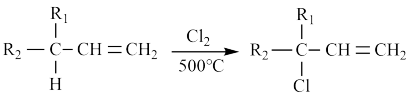

您最近半年使用:0次
6 . 丙烯是一种重要的化工原料、燃料,下列有关丙烯及聚丙烯的说法正确的是
| A.丙烯与等物质的量的氯化氢加成,只生成一种产物 |
| B.1 mol丙烯完全燃烧的耗氧量为4.5 mol |
| C.聚丙烯的链节是−CH2−CH2−CH2− |
| D.1 mol丙烯和1 mol聚丙烯完全燃烧放出CO2的量相同 |
您最近半年使用:0次
名校
解题方法
7 . 烃A与氢气以物质的量 发生加成反应时可以得到多种产物,以下是其中两种产物的结构简式:
发生加成反应时可以得到多种产物,以下是其中两种产物的结构简式:
(1)A的结构简式:________ (不考虑立体异构)。
(2)鉴别A与其属于芳香烃的同分异构体的试剂是________ (写化学式)。
(3)已知环外双键活泼性高于环内双键,写出产物②反应生成高分子化合物的方程式________________ 。
(4)以产物①为原料通过反应可以转化为2-氯-3-乙基-1,4-环己二醇(结构简式如图)。请写出合成路线___________ 。
合成路线常用的表示方式为: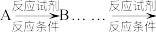 目标产物
目标产物
 发生加成反应时可以得到多种产物,以下是其中两种产物的结构简式:
发生加成反应时可以得到多种产物,以下是其中两种产物的结构简式:产物 | ① | ② |
结构简式 |
|
|
(1)A的结构简式:
(2)鉴别A与其属于芳香烃的同分异构体的试剂是
(3)已知环外双键活泼性高于环内双键,写出产物②反应生成高分子化合物的方程式
(4)以产物①为原料通过反应可以转化为2-氯-3-乙基-1,4-环己二醇(结构简式如图)。请写出合成路线
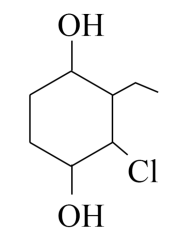 2-氯-3-乙基-1,4-环己二醇 2-氯-3-乙基-1,4-环己二醇 |
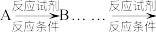 目标产物
目标产物
您最近半年使用:0次
解题方法
8 . 下列反应的离子方程式书写正确的是
A. 溶液中滴加稀硝酸: 溶液中滴加稀硝酸: |
B.向 溶液中加入 溶液中加入 至溶液呈中性的离子方程式: 至溶液呈中性的离子方程式: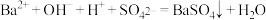 |
C. 在水中的电离方程式: 在水中的电离方程式: |
D.丙烯发生加聚反应生成聚丙烯: |
您最近半年使用:0次
名校
9 . 现有下列几种有机物:① ,②
,② ,③
,③ ,④乙烯,⑤
,④乙烯,⑤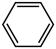 ,⑥
,⑥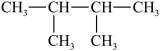 ,⑦丙烯。请根据上述物质回答下列问题。
,⑦丙烯。请根据上述物质回答下列问题。
(1)2.2 g相对分子质量为44的烃完全燃烧消耗标准状况下的氧气的体积是_________ 。(原子量:C:12 H:1)
(2)与③互为同分异构体的是___________ (填序号,下同),与①互为同系物的有___________ 。
(3)用来衡量一个国家石油化工发展水平的物质是___________ ,该物质具有较为活泼的化学性质,可与很多物质发生反应,写出下列物质发生反应的化学方程式。
①与水反应:___________ ;
②与HCl反应:___________ 。
(4)聚丙烯(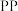 )可制成薄膜、包装材料等,⑦在催化剂条件下合成聚丙烯的化学方程式是
)可制成薄膜、包装材料等,⑦在催化剂条件下合成聚丙烯的化学方程式是___________ 。
(5)工业制④的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应: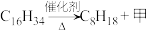 ,
,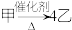 ,则甲的分子式为
,则甲的分子式为___________ ,乙的结构简式为___________ 。
(6)⑤能在一定条件下合成苯乙烯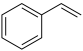 ,苯乙烯的分子式为
,苯乙烯的分子式为___________ ,与溴的四氯化碳溶液反应的化学方程式是___________ ,苯乙烯在一定条件下可发生反应生成高分子化合物反应方程式为___________ 。
 ,②
,② ,③
,③ ,④乙烯,⑤
,④乙烯,⑤ ,⑥
,⑥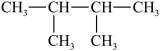 ,⑦丙烯。请根据上述物质回答下列问题。
,⑦丙烯。请根据上述物质回答下列问题。(1)2.2 g相对分子质量为44的烃完全燃烧消耗标准状况下的氧气的体积是
(2)与③互为同分异构体的是
(3)用来衡量一个国家石油化工发展水平的物质是
①与水反应:
②与HCl反应:
(4)聚丙烯(
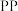 )可制成薄膜、包装材料等,⑦在催化剂条件下合成聚丙烯的化学方程式是
)可制成薄膜、包装材料等,⑦在催化剂条件下合成聚丙烯的化学方程式是(5)工业制④的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:
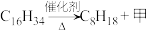 ,
,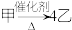 ,则甲的分子式为
,则甲的分子式为(6)⑤能在一定条件下合成苯乙烯
 ,苯乙烯的分子式为
,苯乙烯的分子式为
您最近半年使用:0次
名校
解题方法
10 . Ⅰ.工业上,利用正丁烷通过分解可以获得乙烯、丙烯等。主要反应如下:
反应1:
反应2:
(1)产物中CH4与 C2H6互为___________ (填“同系物”或“同分异构体”,下同);丙烯与CH2=CH2互为___________ 。
(2)丙烯发生加聚反应的方程式为:___________ 。
(3)工业上,乙烯的用途之一是制备环氧乙烷(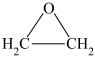 ),已知下面两种制备路径:
),已知下面两种制备路径:
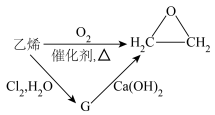
①已知G 有两种官能团,且分子量比乙烯大52.5,则G的结构简式为___________ 。
②请从绿色化学角度评价上述两种制备方案___________ 。
Ⅱ.某化学兴趣小组的同学为探究正丁烷分解产物中CH4和C2H6的比例关系,设计如图所示实验:
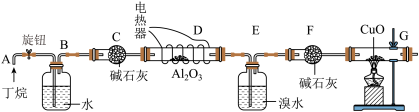
注:CuO能将烃氧化成CO2和H2O;Al2O3是丁烷分解的催化剂,G 后面装置已省略。如图连接好装置后(部分夹持装置已略去),需进行的实验操作有:①给 D、G 装置加热;②检查整套装置的气密性;③排尽装置中的空气。
(4)这三步操作的先后顺序依次是___________ 。
(5)假设丁烷完全分解,流经各装置中的气体能完全反应。当 E 和 F 装置的总质量比反应前增加了 4.9g,G 装置中固体质量减少了 14.4g,则丁烷的分解产物: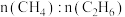
_______ 。
Ⅲ. 若正丁烷中混有异丁烷,会影响裂解反应的产率。
(6)实验室中,利用蒸馏的方式分离正丁烷与异丁烷。从蒸馏装置中先被分离出来的应为___________ (填“正丁烷”或“异丁烷”)。
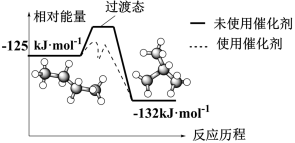
(7)正丁烷和异丁烷之间转化的能量变化如图所示,下列有关催化剂的叙述正确的是___________(填标号)。
反应1:

反应2:

(1)产物中CH4与 C2H6互为
(2)丙烯发生加聚反应的方程式为:
(3)工业上,乙烯的用途之一是制备环氧乙烷(
 ),已知下面两种制备路径:
),已知下面两种制备路径:
①已知G 有两种官能团,且分子量比乙烯大52.5,则G的结构简式为
②请从绿色化学角度评价上述两种制备方案
Ⅱ.某化学兴趣小组的同学为探究正丁烷分解产物中CH4和C2H6的比例关系,设计如图所示实验:

注:CuO能将烃氧化成CO2和H2O;Al2O3是丁烷分解的催化剂,G 后面装置已省略。如图连接好装置后(部分夹持装置已略去),需进行的实验操作有:①给 D、G 装置加热;②检查整套装置的气密性;③排尽装置中的空气。
(4)这三步操作的先后顺序依次是
(5)假设丁烷完全分解,流经各装置中的气体能完全反应。当 E 和 F 装置的总质量比反应前增加了 4.9g,G 装置中固体质量减少了 14.4g,则丁烷的分解产物:
Ⅲ. 若正丁烷中混有异丁烷,会影响裂解反应的产率。
(6)实验室中,利用蒸馏的方式分离正丁烷与异丁烷。从蒸馏装置中先被分离出来的应为
(7)正丁烷和异丁烷之间转化的能量变化如图所示,下列有关催化剂的叙述正确的是___________(填标号)。

| A.能改变反应活化能 | B.能降低反应焓变 |
| C.能增大平衡常数 | D.能加快反应速率 |
您最近半年使用:0次





